Document
アブスキー社、事業の最新情報と2025年第3四半期の財務・業績について発表
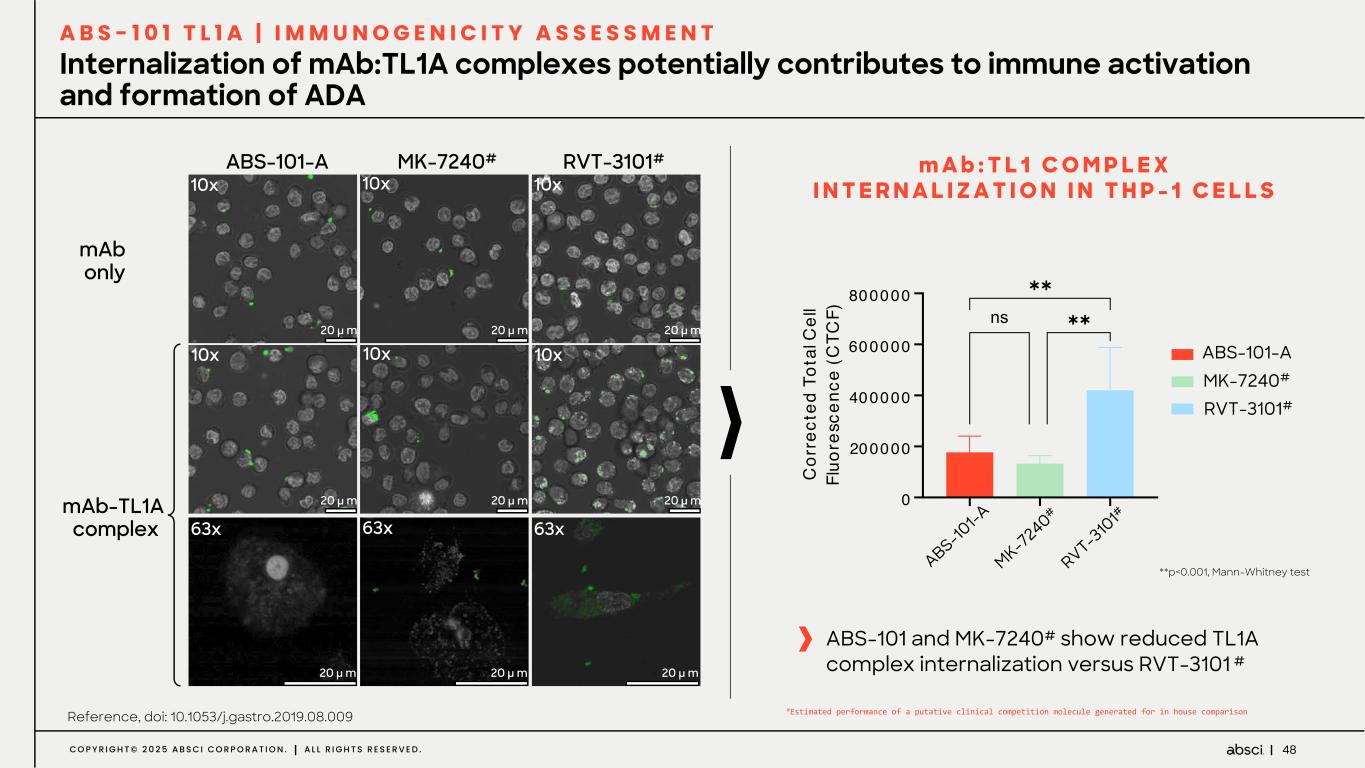
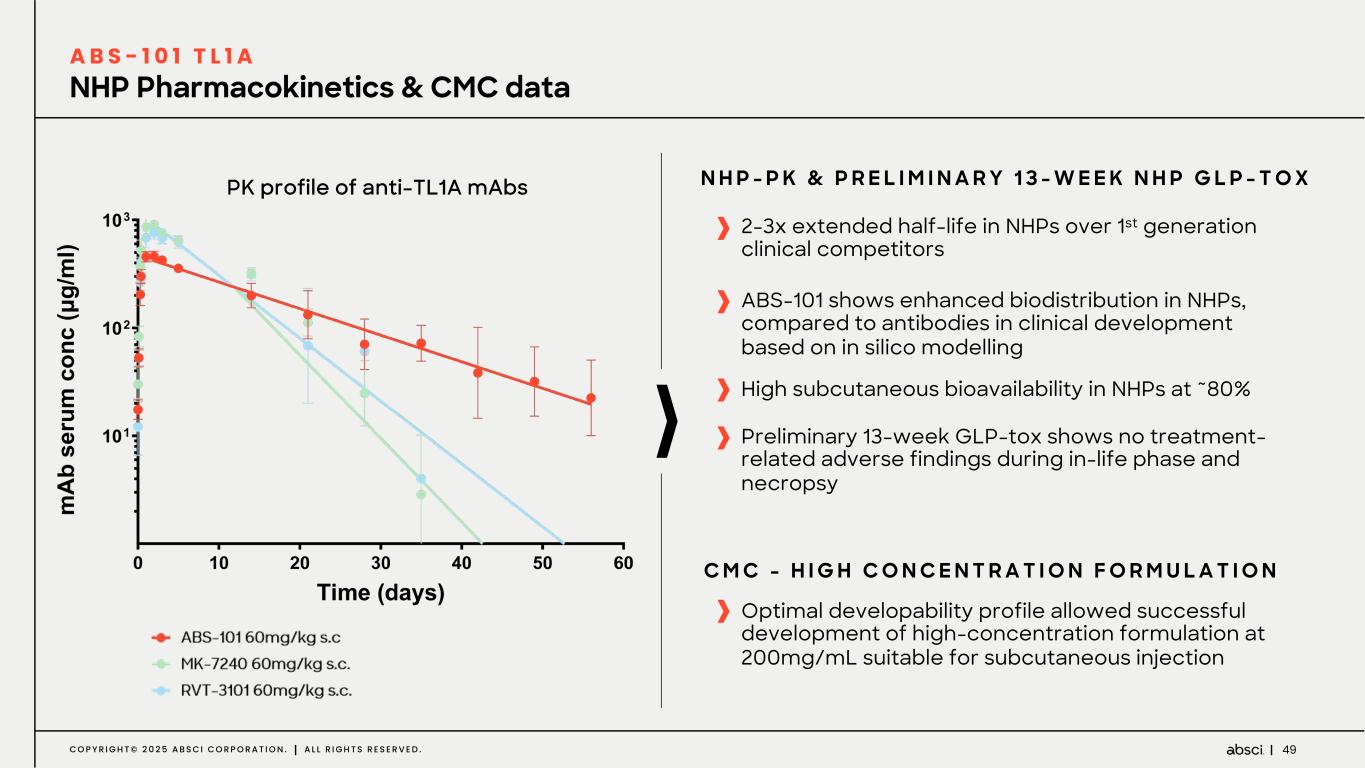
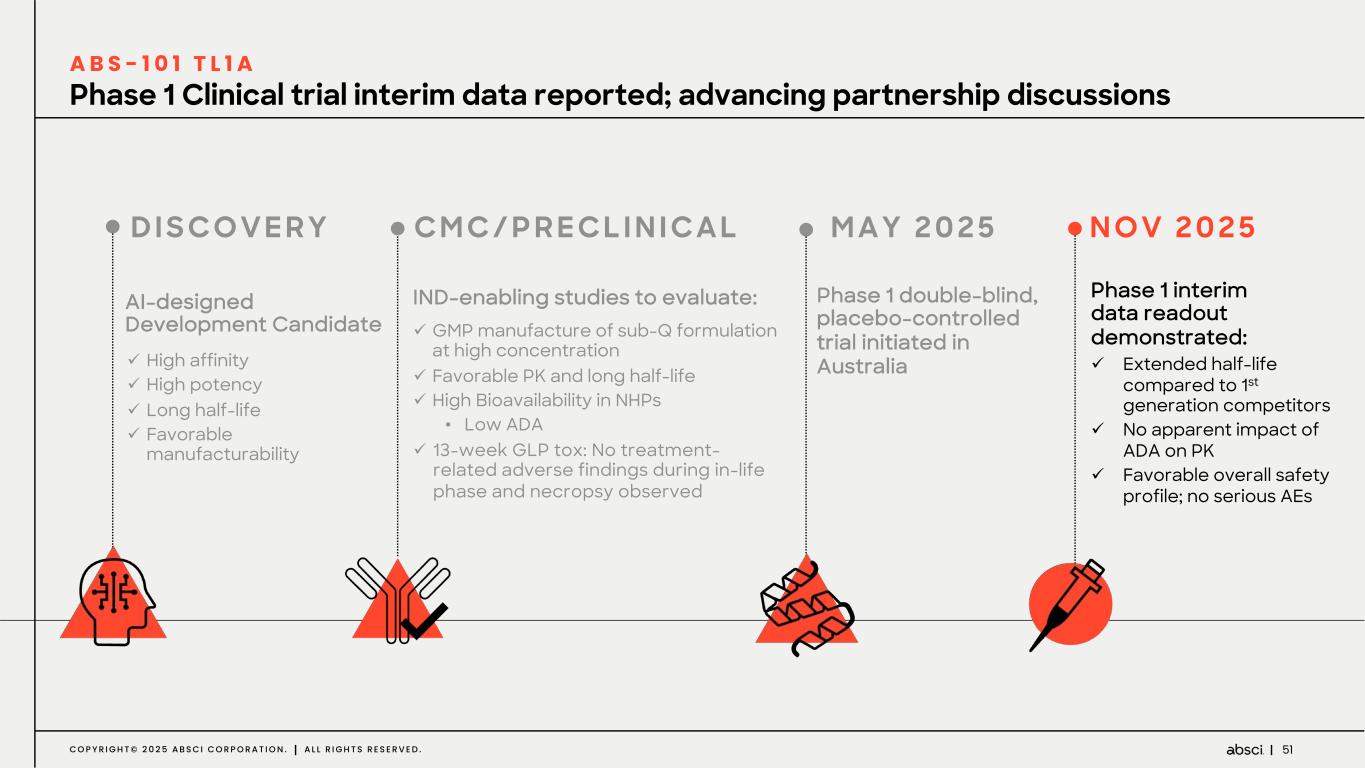
ABS-101(抗TL1A薬)の臨床第1相試験の中間結果を発表)
ABS-201(男性型脱毛症治療薬抗PRLR)のPh1/2a試験を12月に開始予定、12月11日にKOLセミナーを開催
ABS-201戦略を拡大し、子宮内膜症を新たな適応症として追求、2026年第4四半期に第2相臨床試験の開始を見込む
2028年前半までの事業運営に十分な現金、現金同等物および有価証券
米国ワシントン州ヴァンクーバーおよびニューヨーク発、2025年11月12日 - AI(人工知能)を活用した画期的な治療薬の開発を進める臨床段階のバイオ医薬品企業アブシー・コーポレーション(Nasdaq: ABSI)は本日、2025年9月30日に終了した四半期の財務および営業成績を発表した。
「創業者兼 CEO のショーン・マクレインは、次のように述べています。「今期は、ABS-201 に焦点を絞り、強力な生物学的根拠とアンメットニーズの高い 2 つの適応症でこのプログラムを推進することで、ABS-201 が Absci 社にとって極めて重要な転換点となることを意味します。「アンドロゲン性脱毛症および子宮内膜症におけるPRLRメカニズムにリソースを再配分することで、患者さんにとって意義のある影響をもたらすと同時に、株主の皆様にとっても最大の利益をもたらすことができるようになります。当社の戦略は、規律ある実行と、画期的な治療薬を提供するジェネレーティブAIタンパク質設計の力に対する自信を反映しています。"
Recent Highlights
-ABS-101(抗TL1A薬)の臨床第1相試験の中間結果を報告。第一世代の抗TL1A薬競合プログラムに比べて半減期が延長され、重篤な有害事象は報告されなかった。Absci 社は、当社の事業戦略に沿って、本資産に関する提携および導出の可能性を引き続き検討する。
-ABS-201(男性型脱毛症に対する抗PRLR薬)のPh1/2a試験の開始を2025年12月に早め、2026年後半に中間的な有効性を読み出す可能性。Absci 社は、12 月 11 日にバーチャル KOL セミナーを開催し、予想される臨床試験パス、差別化されたプロ ファイル、ABS-201 の市場可能性など、本プログラムの最新状況と進展について説明します。
-ABS-201戦略を拡大し、子宮内膜症を新たな適応症として追求。Absci 社は、2026 年第 4 四半期に子宮内膜症を対象とした第 2 相臨床試験を開始し、2027 年下半期に概念実証を行う可能性を見込んでいる。
社内パイプラインの最新情報、予想されるプログラムの進捗状況、2025年の見通し
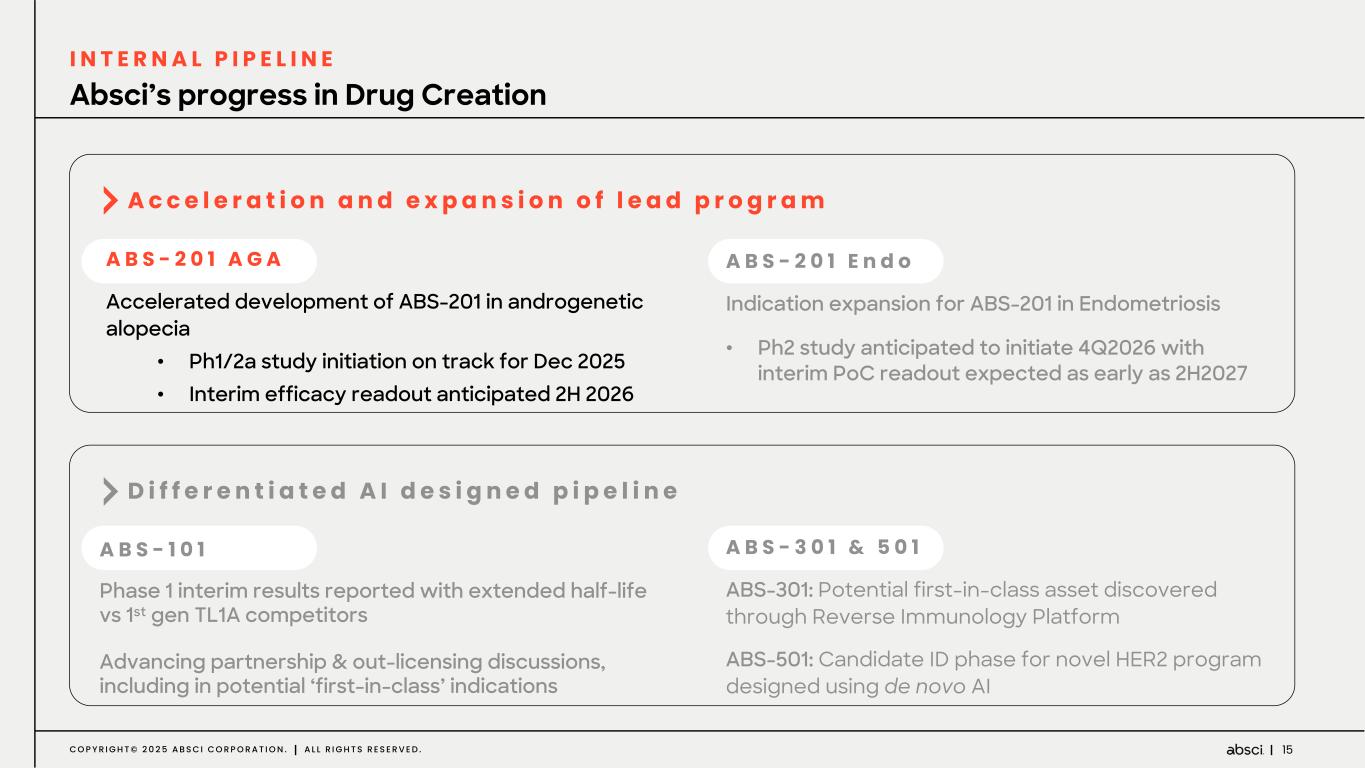
-ABS-101(抗TL1A抗体):ABS-101 の第 1 相臨床試験の中間データでは、競合する第 1 世代の抗 TL1A 抗体に比べて半減期が延長され、ADA による PK への明らかな影響は認められず、安全性プロファイルも良好で、重篤な有害事象は報告されなかった。このデータにより、ABS-101は当社の事業戦略に沿って提携や導出の可能性を追求するとともに、ファースト・イン・クラスの適応拡大の可能性も検討していく。ABS-101の後期開発試験については、現時点では社内で実施しないという戦略的決定を行った。その代わりに、ABS-201のアンメット・メディカル・ニーズと市場機会が高い子宮内膜症における臨床開発の拡大・加速に向けて資本とリソースを配分する。
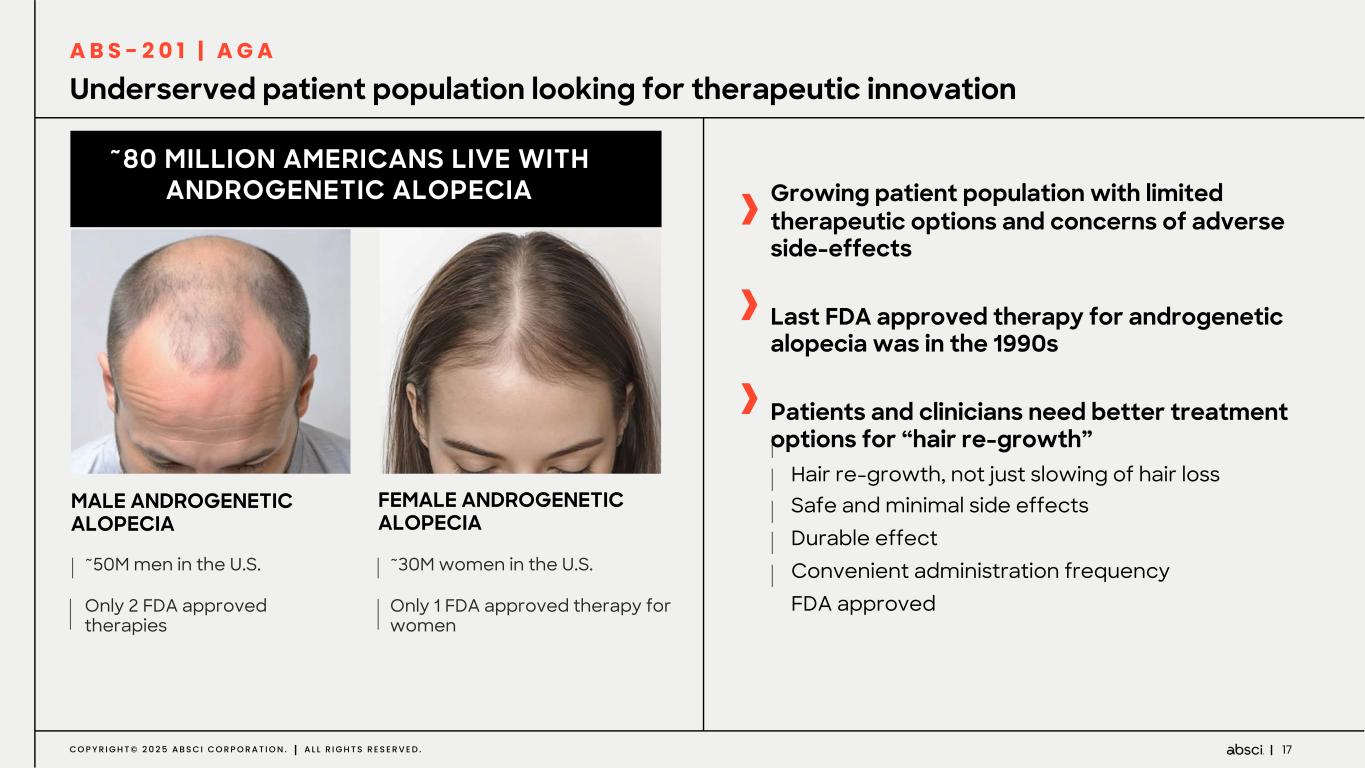
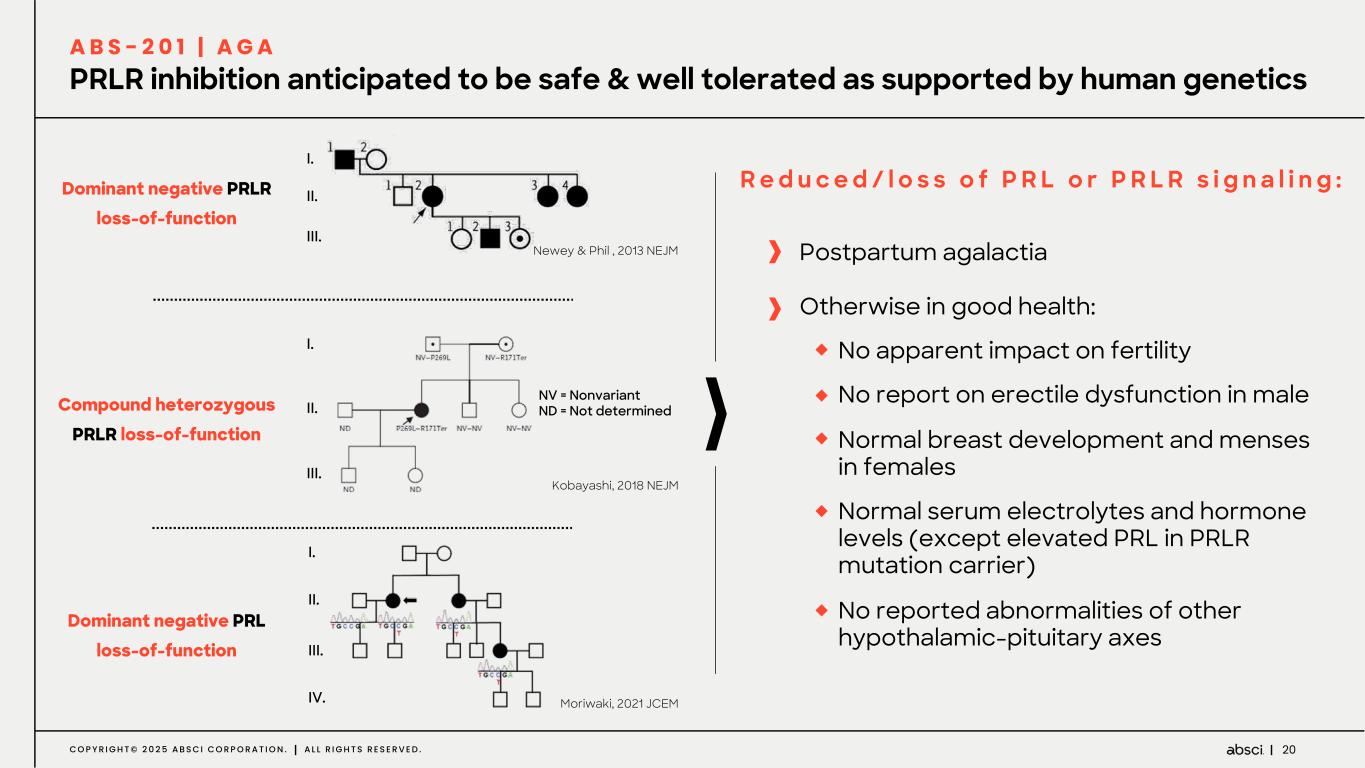
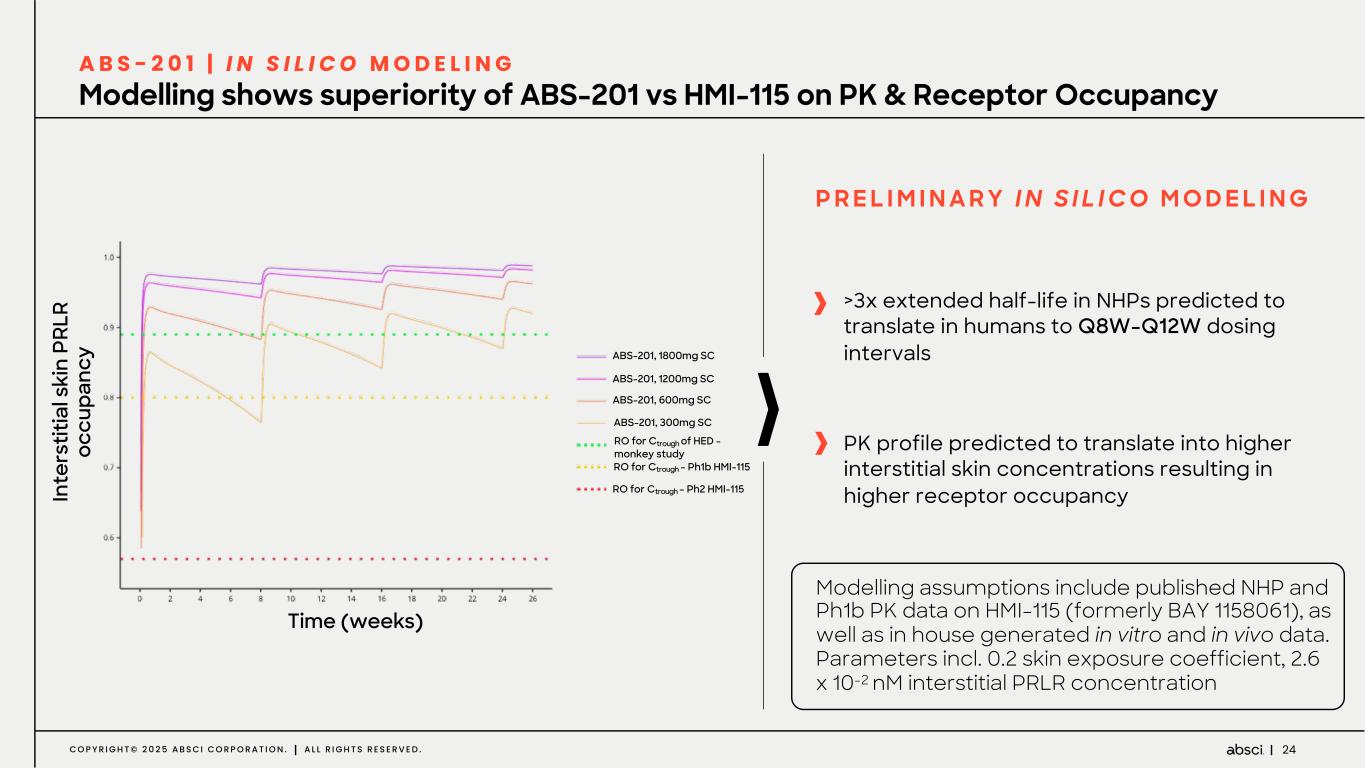
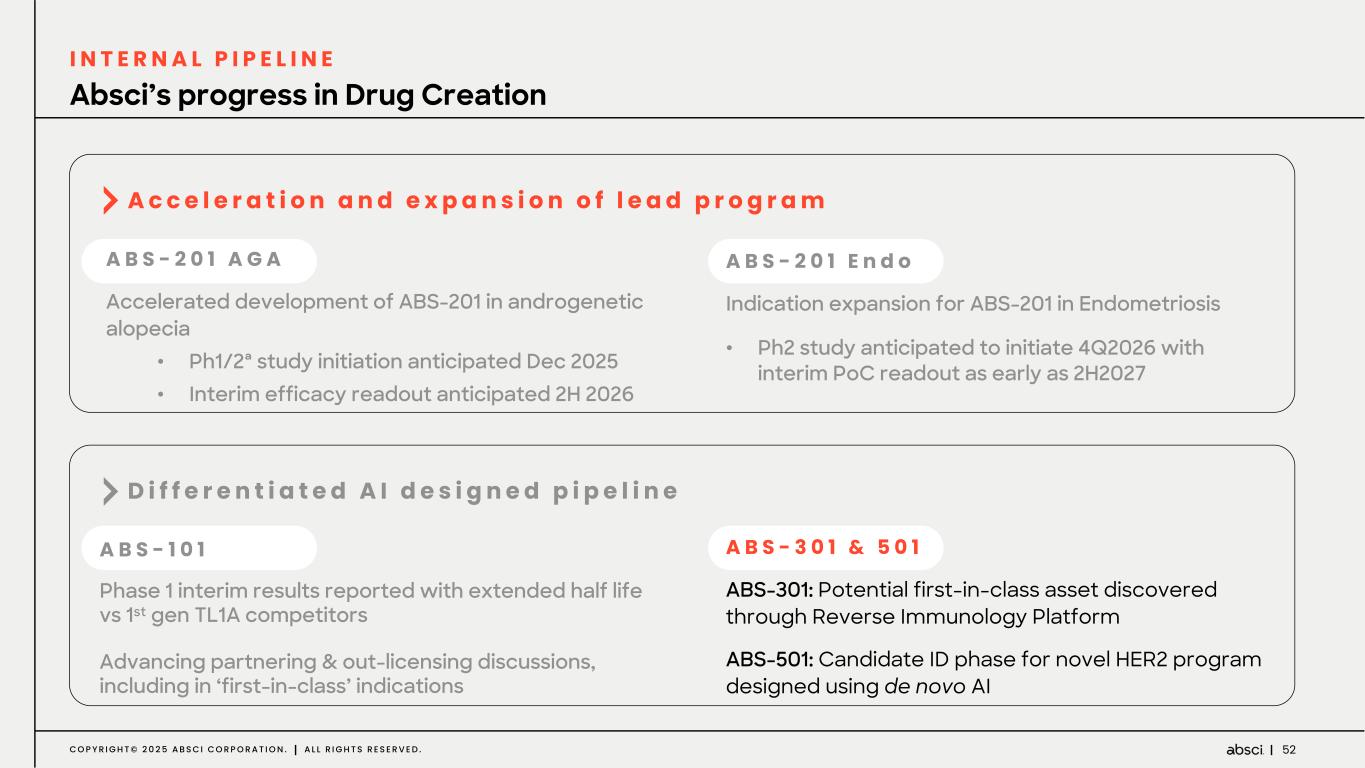
-ABS-201(抗PRLR抗体)は、男性型脱毛症を適応症として開発中です:ABS-201は、男性型脱毛症を適応症として開発中のクラス最高の抗PRLR抗体で、アンメット・クリニカル・ニーズが高く、米国だけでも約8,000万人の患者さんがいる可能性があります。Absci社は、高い親和性と効力、良好な安全性と免疫原性、投与頻度が少なく便利な半減期の延長、優れた開発性と製造性を示唆する前臨床プロファイルを有する開発候補品のIND可能化試験を完了しつつあります。ABS-201は、現在の標準治療と比較して、より効果的で、便利で、耐久性があり、安全な選択肢を提供する可能性があります。ABS-201は、2025年12月に男性型脱毛症を対象とした第1/2a相臨床試験を開始し、2026年後半に中間的な有効性を確認する予定です。
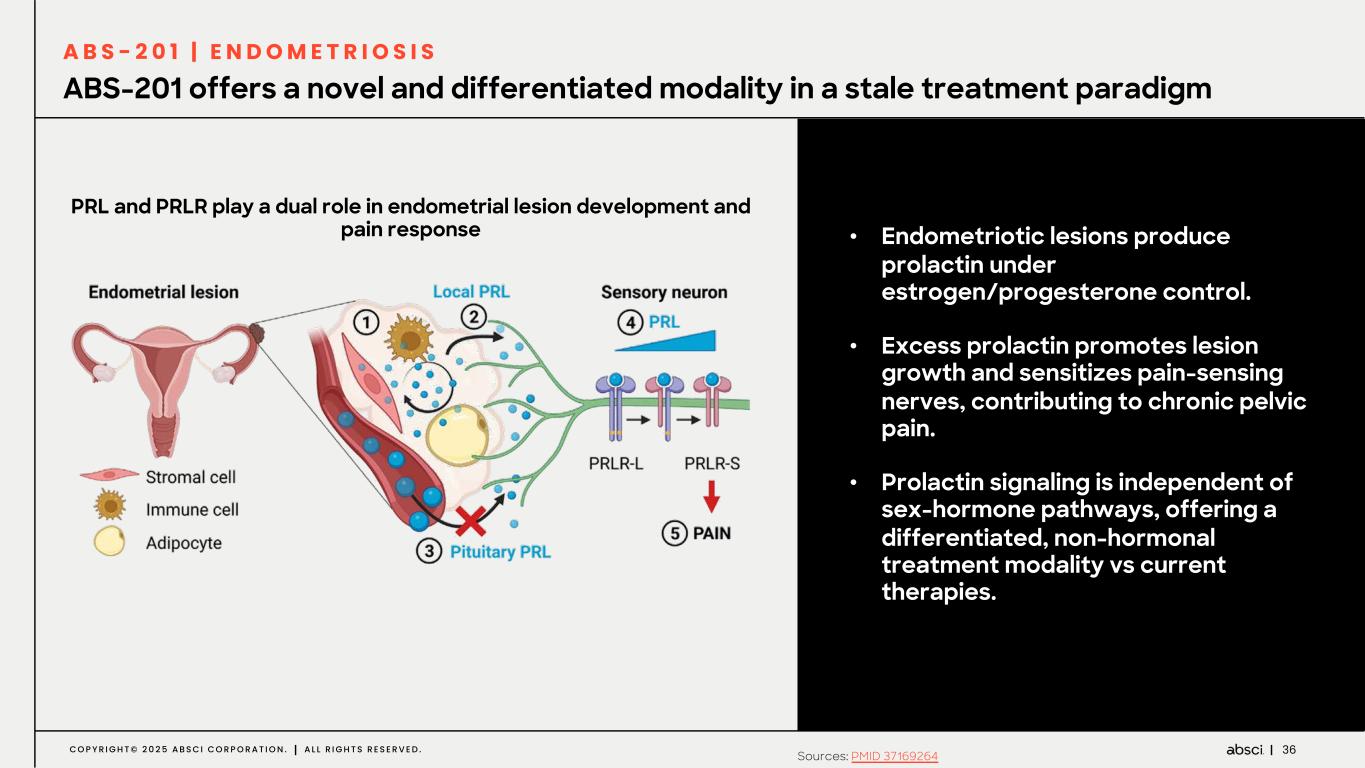
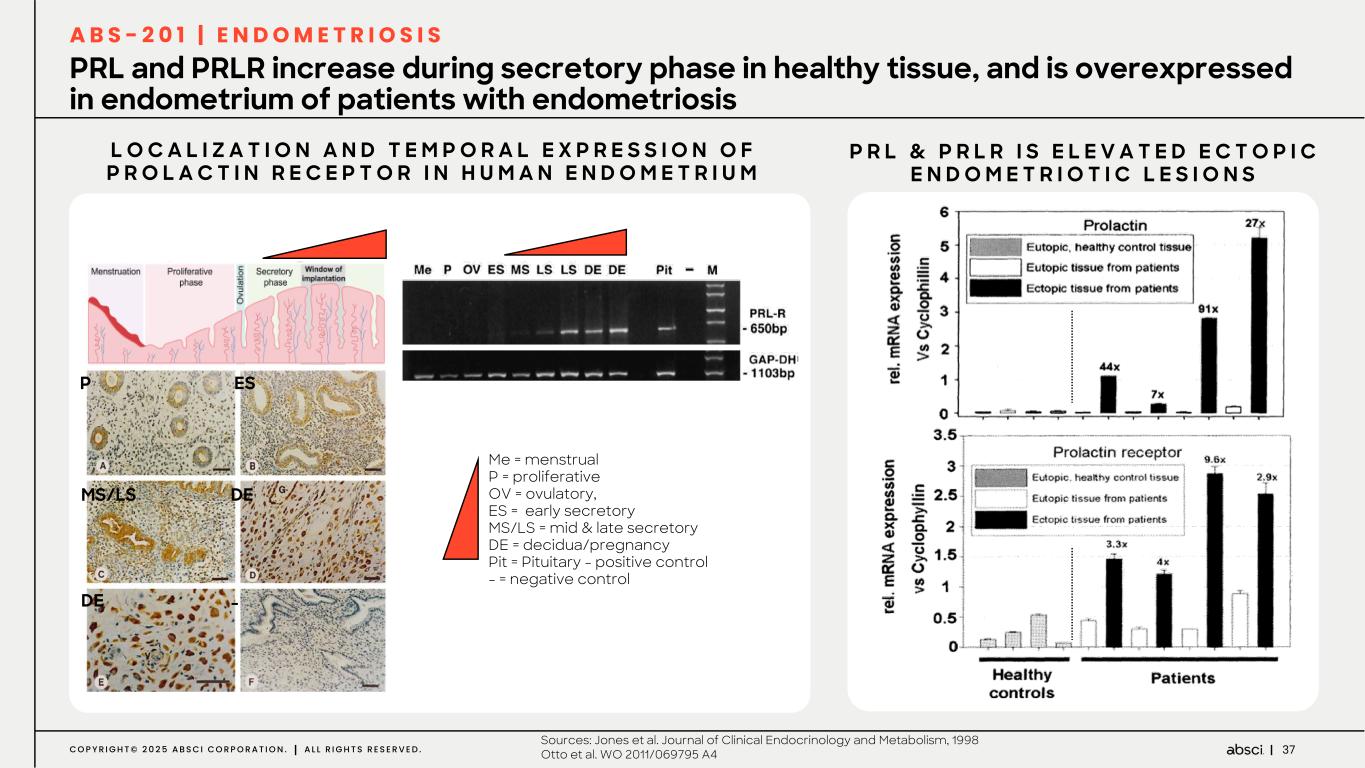
-ABS-201(抗 PRLR 抗体)の子宮内膜症への適応についてアブッシ社は本日、ABS-201 抗体の追加適応症として、アンメット・メディカル・ニーズが高く、標準治療が十分でない大規模な未治療市場である子宮内膜症を追求すると発表した。子宮内膜症は、米国では推定900万人の女性を含め、世界中の女性の最大10%が罹患しており、現在のところ、内科的または外科的治療法はありません。Absci社は、2026年第4四半期に子宮内膜症を対象とした第2相臨床試験を開始し、2027年後半に概念実証を行う予定である。
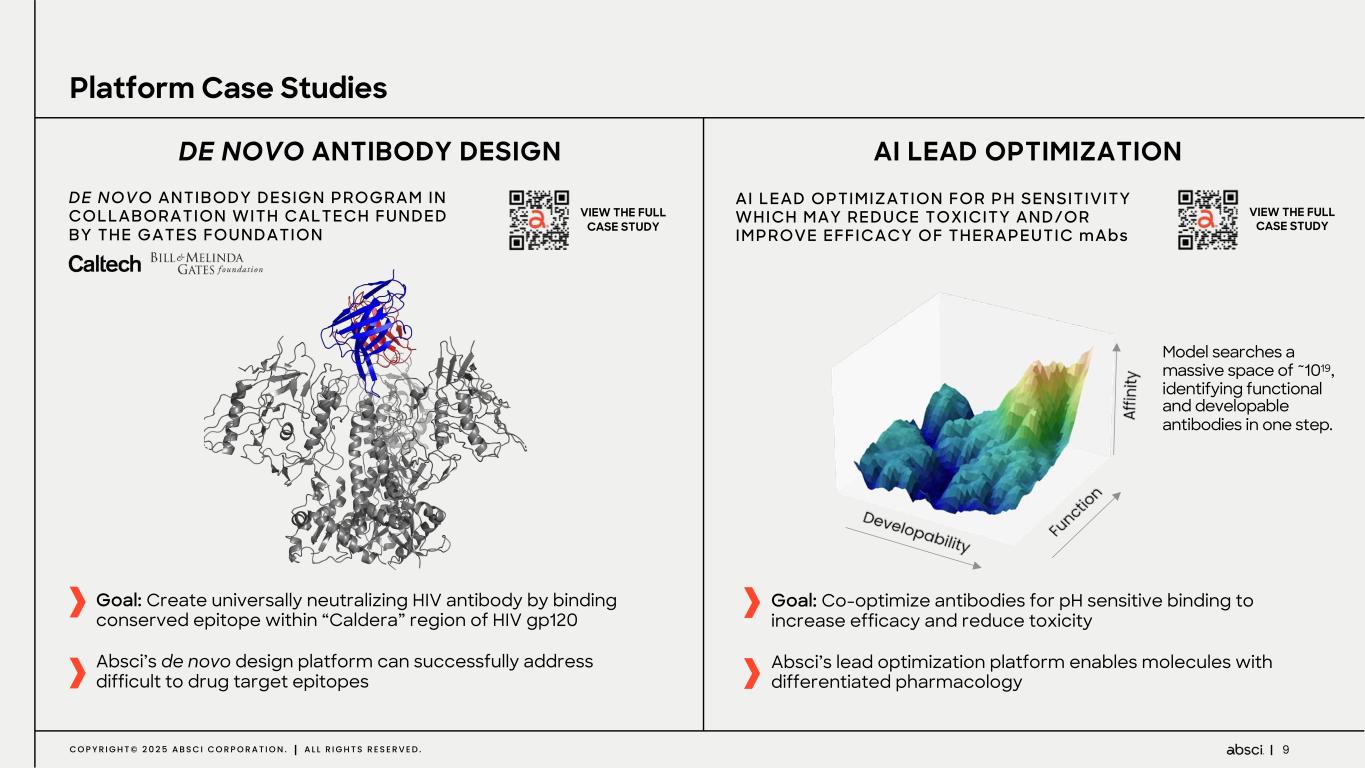
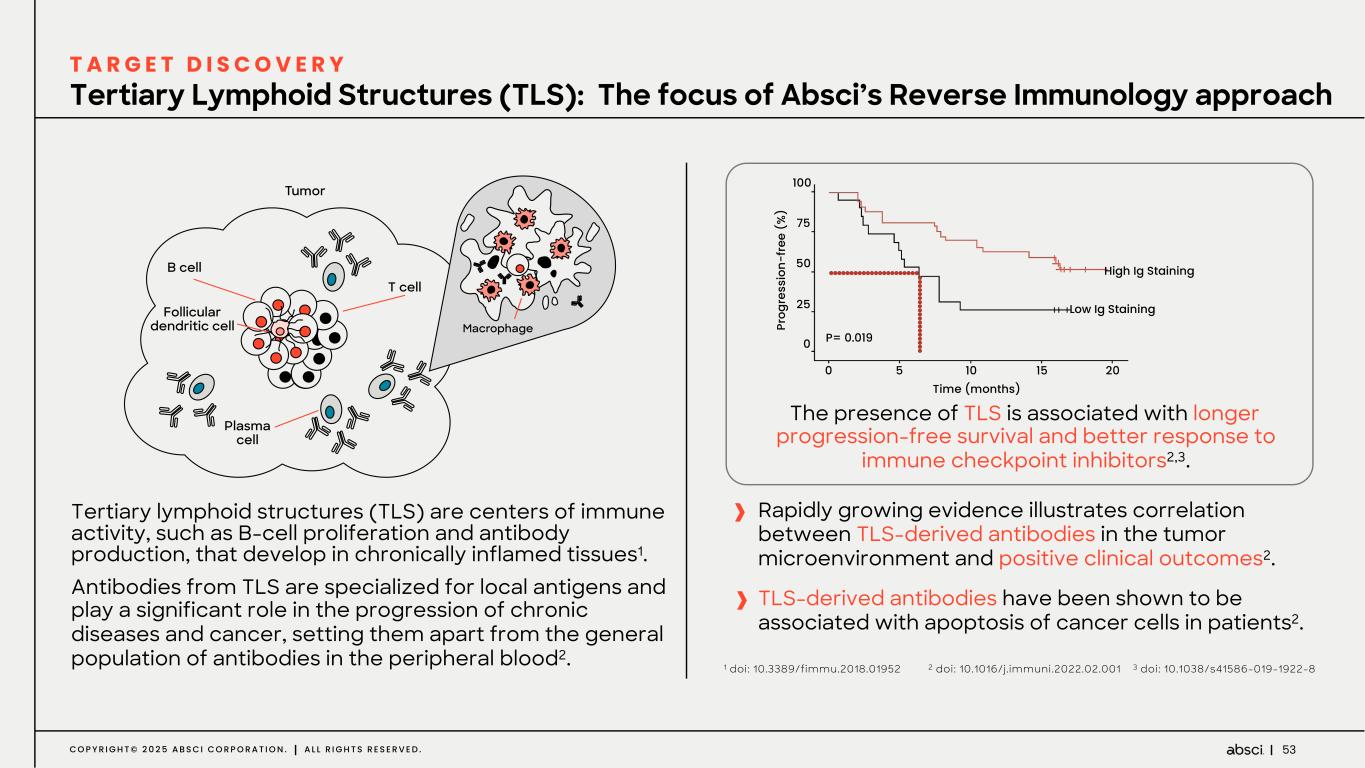
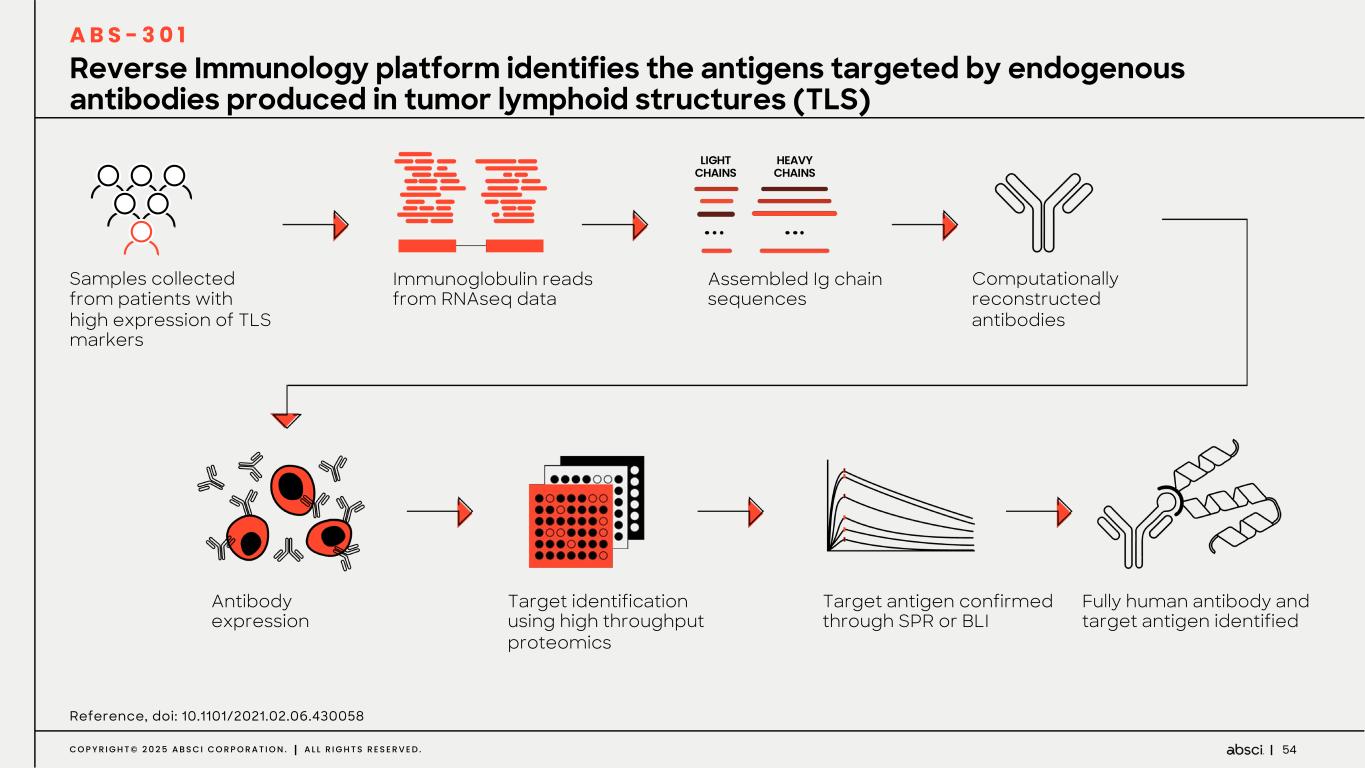
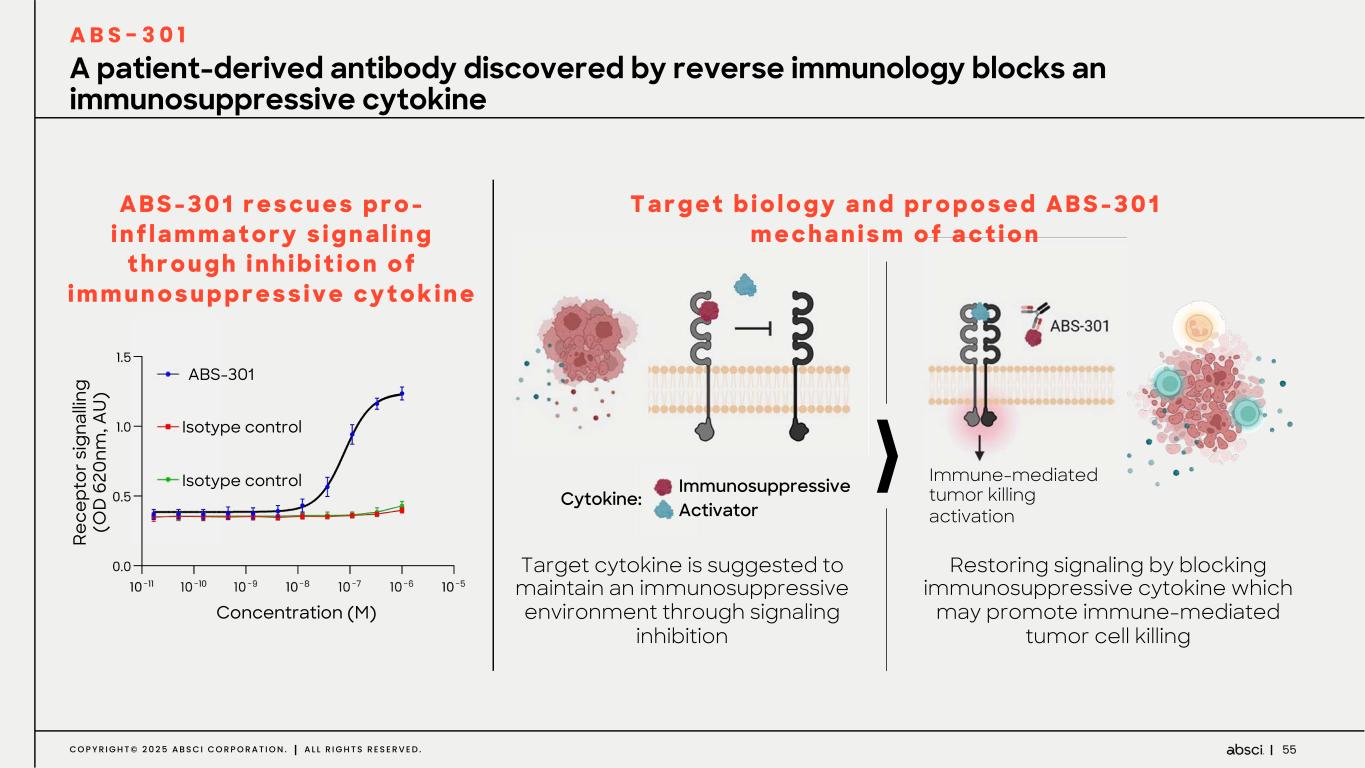
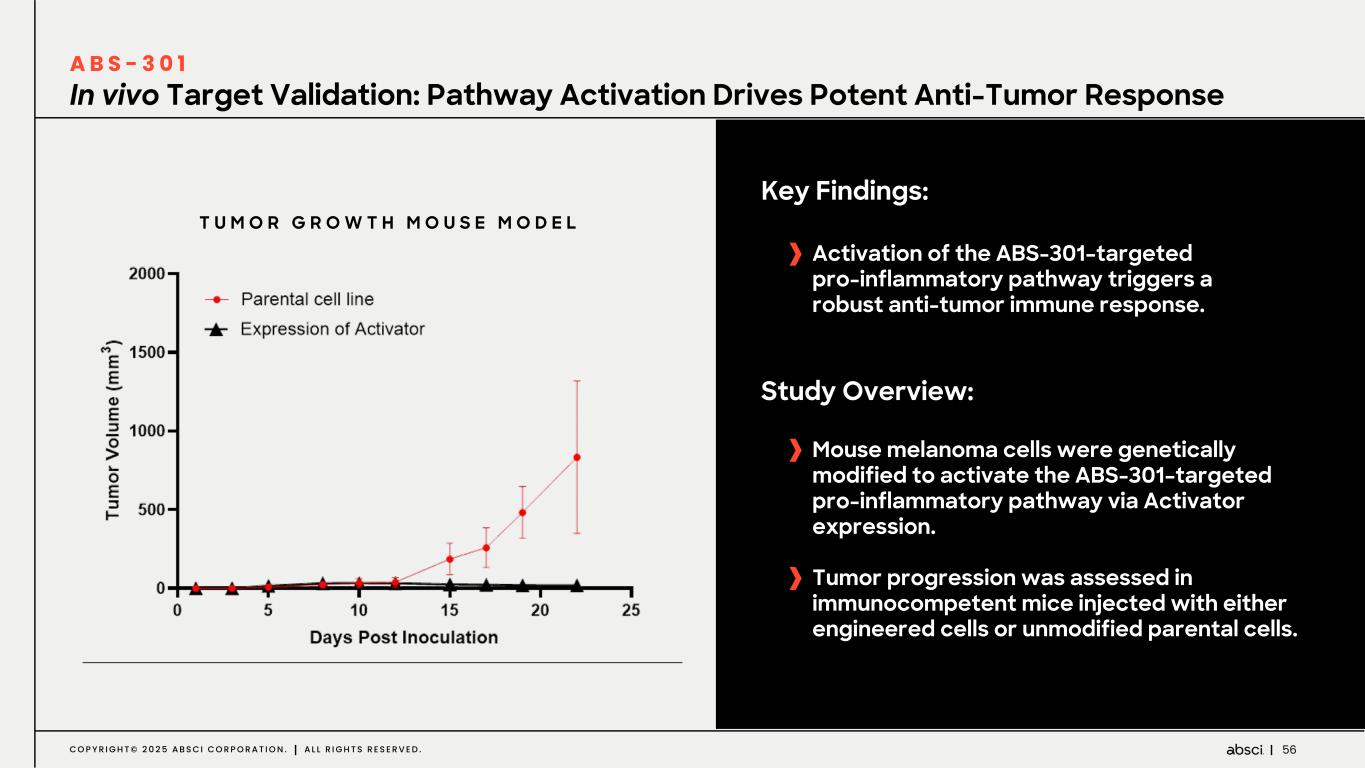
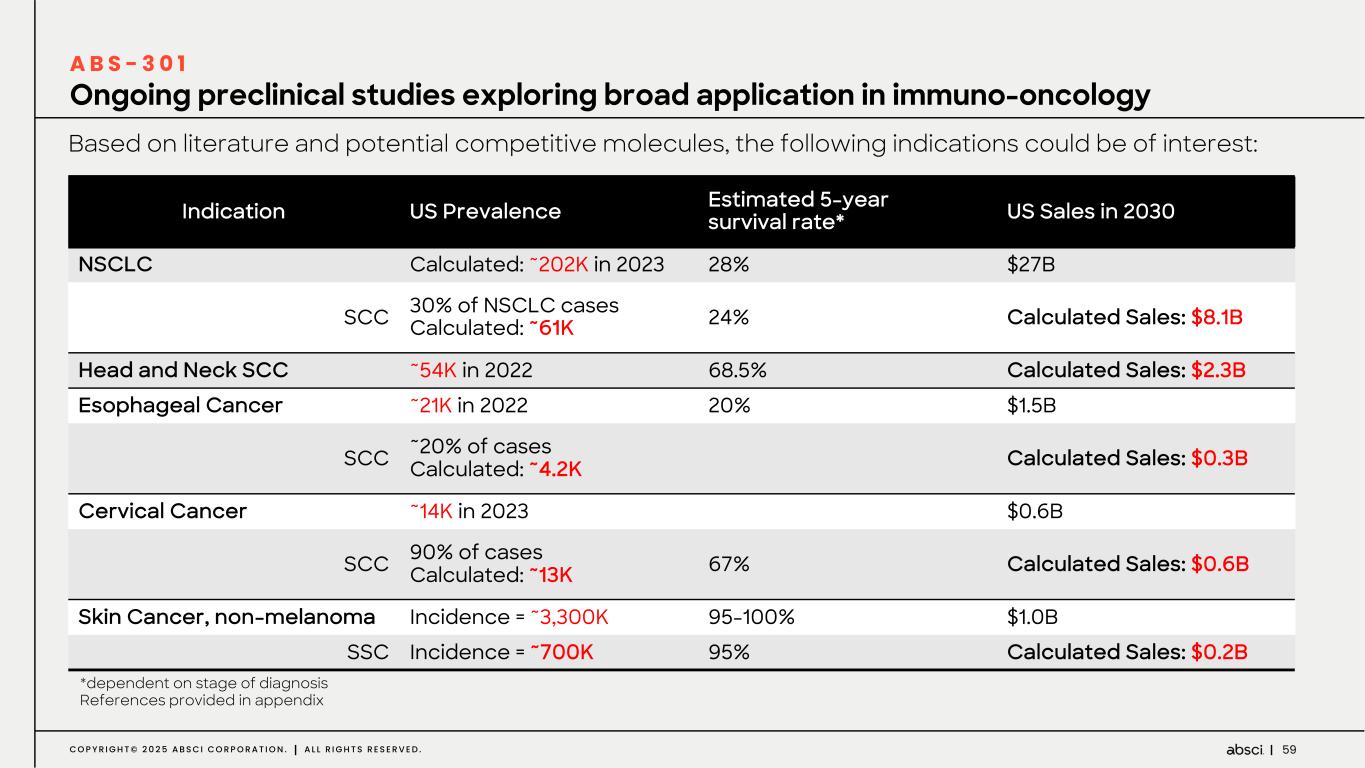
-ABS-301(未発表の免疫腫瘍学的標的に対するファースト・イン・クラス抗体の可能性):ABS-301は、AbsciのReverse Immunologyプラットフォームにより発見された新規ターゲットに結合するようデザインされた完全ヒト抗体である。ABS-301の標的の発現は、扁平上皮癌をはじめとする幅広い可能性を示唆している。このプログラムにおいて、Absciは高い親和性と効力を持つ抗体リードを最適化し、最初のin vivo標的検証試験を成功裏に完了した。この試験で得られた知見から、この経路を介したシグナル伝達が強力な抗腫瘍反応を引き起こすことが示され、ABS-301のin vivo有効性試験を進める強力な根拠となった。これらの結果は、前臨床開発を継続し、ABS-301の治療の可能性をさらに追求することを支持するものである。
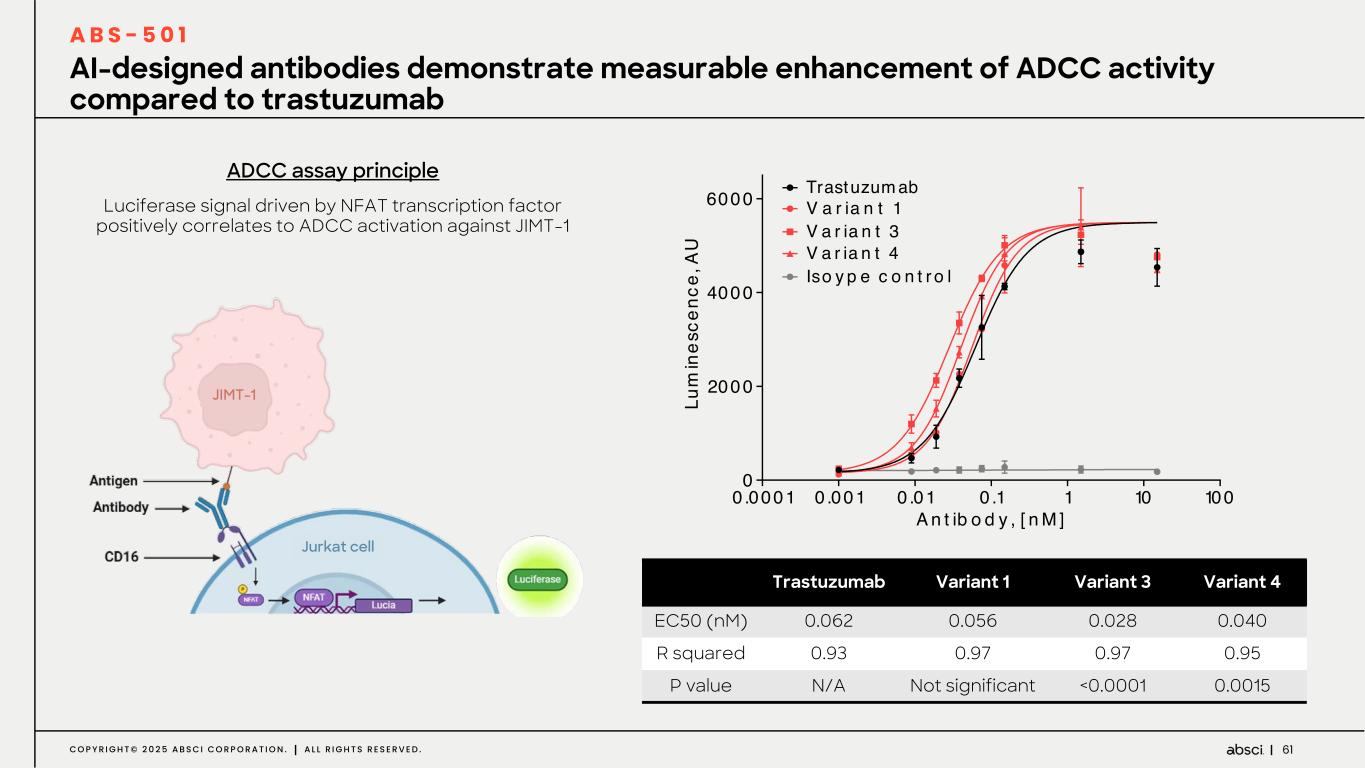
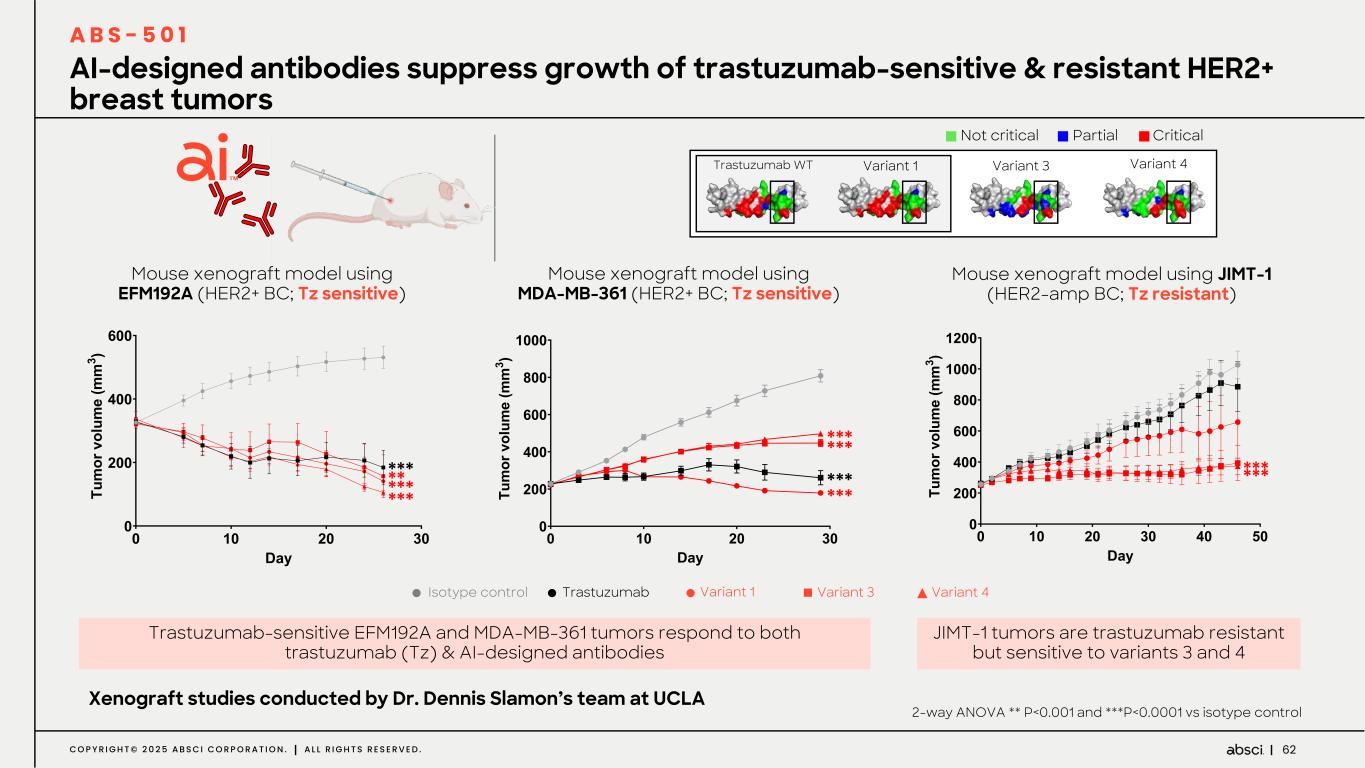
-ABS-501(新規AI設計抗HER2抗体):本プログラムにおいてアブシ社は、ゼロショット de novo AI 技術を用いて、新規エピトープ相互作用、前臨床におけるトラスツズマブに対する親和性の向上または同等、トラスツズマブ抵抗性異種移植腫瘍に対する有効性、良好な開発可能性といった特徴を有する抗体リードを同定しました。
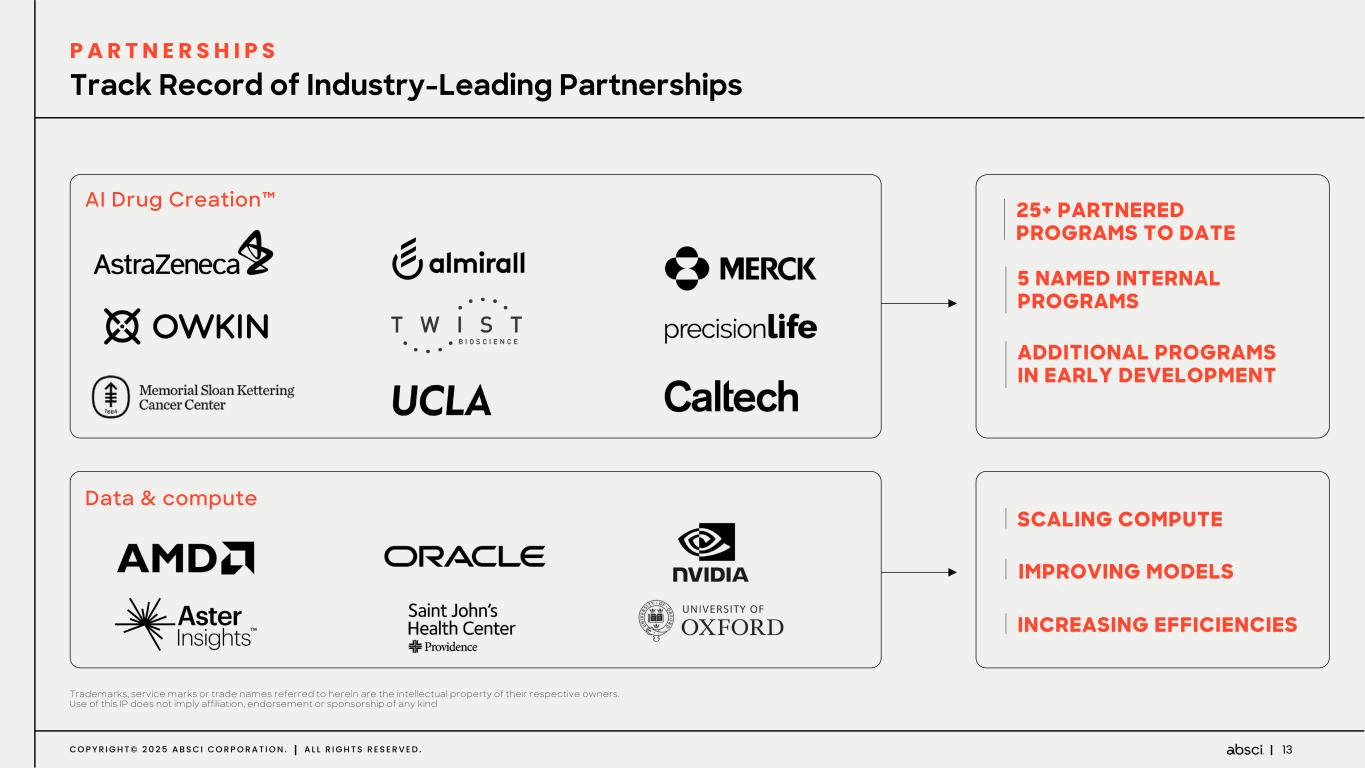
-創薬パートナーシップ:Absciは既存の創薬パートナーシップをさらに進展させ、2025年には大手製薬会社を含む1つ以上のパートナーシップを締結する予定である。
Absci社は、現在および将来の提携プログラムとともに、社内のパイプライン・プログラムの推進に投資と事業の焦点を当て続け、同時に継続的なプラットフォームの改善と事業の効率化を達成する。現在の計画では、現預金、現金同等物、有価証券は2028年前半までの事業運営に必要な資金として十分であると考えている。
2025年第3四半期決算
2025年9月30日に終了した3ヵ月間の収益は0.4百万ドルであったのに対し、2024年9月30日に終了した3ヵ月間は1.7百万ドルであった。
研究開発費は、2024年9月30日に終了した3ヵ月間が1,800万ドルであったのに対し、2025年9月30日に終了した3ヵ月間は1,920万ドルであった。この増加は主に、外部での前臨床および臨床開発に関連する直接費用を含むアブッシの社内プログラムの進展によるものである。
販売費・一般管理費は2024年9月30日に終了した3ヵ月間が930万ドルであったのに対し、2025年9月30日に終了した3ヵ月間は840万ドルであった。この減少は主に人件費の減少によるものである。
2025年9月30日に終了した3ヵ月間の純損失は2,870万ドル(2024年9月30日に終了した3ヵ月間は2,740万ドル)であった。
2025年9月30日現在の現金、現金同等物および有価証券は、2025年6月30日現在の1億1750万ドルに対し、1億5250万ドルであった。
Webcast Information
アブシティは、2025年第3四半期の業績および財務・業績に関する電話会議を、米国東部時間11月12日(水)午後4時30分(太平洋標準時)より開催します。カンファレンス・コールのウェブキャストはinvestors.absci.comでご覧いただけます。ウェブキャストはアーカイブされ、イベント終了後少なくとも90日間は再生可能です。
About Absci
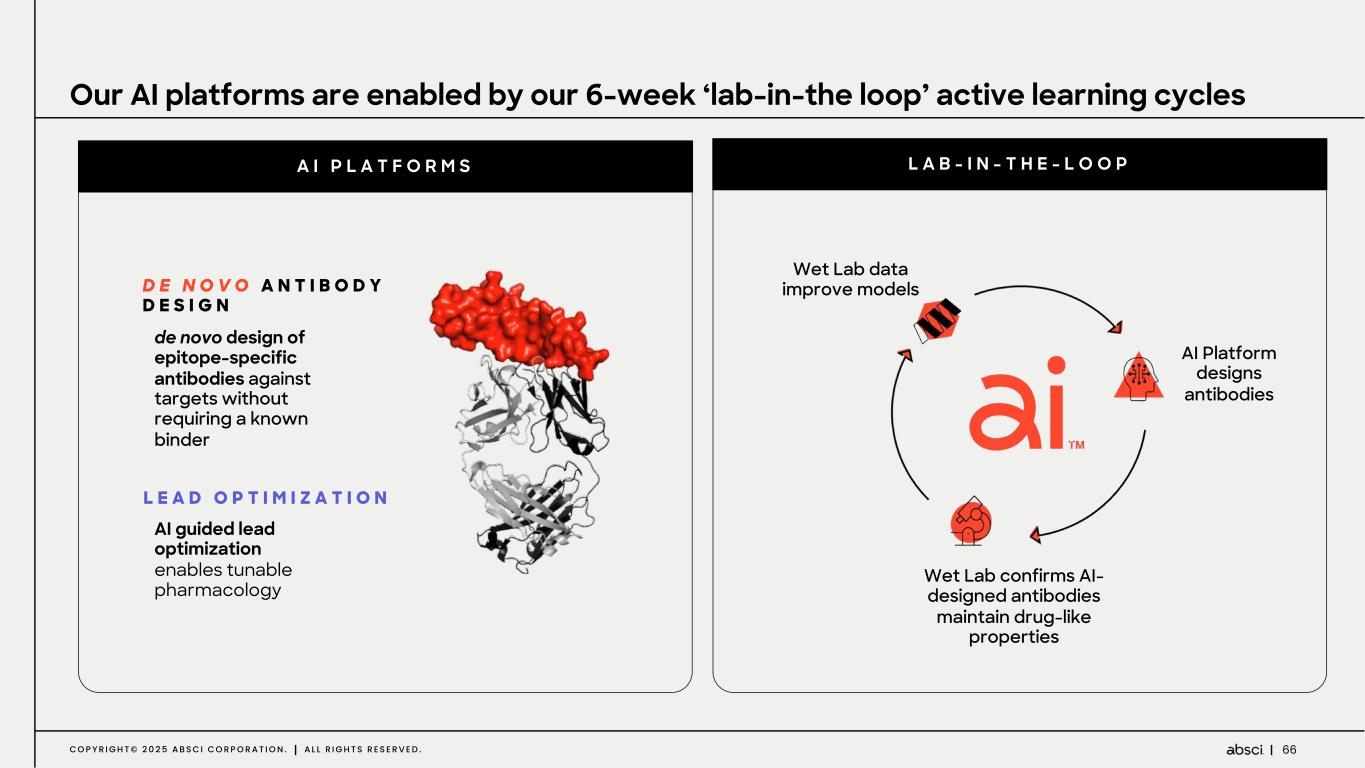
アブシティは、より優れた生物製剤をより早く患者さんのために創製するために、ジェネレーティブ・デザインを用いて創薬の未来を進めています。当社のIntegrated Drug Creation™プラットフォームは、最先端のAIモデルと合成生物学データエンジンを組み合わせ、困難な治療ターゲットに対応する革新的な治療薬の迅速な設計を可能にします。Absciのアプローチは、高度なAIアルゴリズムとウェットラボでの検証の間の継続的なフィードバックループを活用しています。サイクルを繰り返すごとにデータが洗練され、モデルが強化されるため、迅速なイノベーションが促進され、治療デザインの精度が向上します。ABS-201は、男性型および女性型脱毛症として知られる男性型脱毛症の治療の可能性を再定義する画期的な発毛剤です。また、ABS-201は、アンメット・メディカル・ニーズが高く、市場参入の可能性がある子宮内膜症に対する「クラス最高の」治療薬となる可能性も検討されている。Absci社は、ワシントン州バンクーバーに本社を置き、ニューヨークにAI研究所、スイスにイノベーションセンターを構えている。詳細はwww.absci.com、LinkedIn(@absci)、X(@Abscibio)、YouTubeでフォローしてください。
Forward-Looking Statements
本プレスリリースに記載されている、過去の事実ではない事項に関する記述は、1995年米国私募証券訴訟改革法(Private Securities Litigation Reform Act of 1995)の定義における「将来の見通しに関する記述」です。このような記述はリスクや不確実性を伴うため、実際の結果はこのような将来見通しに関する記述によって明示的または黙示的に示されたものとは大きく異なる可能性があります。このような記述には、以下のいずれかまたはすべてに関する記述が含まれますが、これらに限定されるものではありません:(i) Absciの前臨床試験、臨床試験、提携プログラムおよび自社開発プログラム(製造能力、当該試験および臨床試験の状況、データ、安全性および有効性に関する一般的な期待を含むがこれらに限定されない)、(ii) 上記の口頭発表に含まれるデータ、ならびに進行中および計画中の臨床試験から得られたデータをさらなる臨床試験の計画および開始に使用する能力;(iii)Absci社の戦略、目標、予想される財務実績および現金資源の十分性、(iv)規制当局への申請および認可(予想される規制当局の決定に関するスケジュールおよび予想を含む)、(v)パートナーとの共同研究から期待される利益、(vi)抗体療法およびその他の技術の治療価値、開発および商業的可能性。
将来予想に関する記述の不確実性をもたらすリスクには、Absci Corporationの最新の年次報告書(フォーム10-K)およびAbsci Corporationが米国証券取引委員会に提出したその他の書類の「リスク要因」の見出しに記載されているリスクや不確実性が含まれますが、これらに限定されるものではありません。既存の投資家および将来の投資家は、これらの将来見通しに関する記述を過度に信頼しないようご注意ください。当社は、本プレスリリースに含まれる将来見通しに関する記述を更新または修正する義務または約束を、法律で義務付けられている場合を除き、一切否認します。
Investor Contact:
Alex Khan
財務・IR担当副社長
investors@absci.com
Media Contact:
press@absci.com
absci@methodcommunications.com
Absci Corporation
未監査の要約四半期連結損益計算書
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
9月30日に終了した3ヵ月間, |
|
9月30日に終了した9ヵ月間, |
|
| (単位:千米ドル、ただしシェアおよび1株当たりのデータを除く) |
|
2025 |
|
2024 |
|
2025 |
|
2024 |
|
|
|
|
|
|
|
|
|
|
|
| Partner program revenue |
|
$ |
378 |
|
|
$ |
1,701 |
|
|
$ |
2,150 |
|
|
$ |
3,869 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| 営業費用 |
|
|
|
|
|
|
|
|
|
| 研究開発費 |
|
19,249 |
|
|
17,985 |
|
|
56,071 |
|
|
45,482 |
|
|
| 販売費及び一般管理費 |
|
8,441 |
|
|
9,256 |
|
|
26,441 |
|
|
27,346 |
|
|
| 減価償却費および償却費 |
|
2,842 |
|
|
3,355 |
|
|
8,914 |
|
|
10,155 |
|
|
|
|
|
|
|
|
|
|
|
|
| 営業費用合計 |
|
30,532 |
|
|
30,596 |
|
|
91,426 |
|
|
82,983 |
|
|
| Operating loss |
|
(30,154) |
|
|
(28,895) |
|
|
(89,276) |
|
|
(79,114) |
|
|
| Other income (expense) |
|
|
|
|
|
|
|
|
|
| 支払利息 |
|
(45) |
|
|
(130) |
|
|
(180) |
|
|
(456) |
|
|
| その他の収益(純額) |
|
1,597 |
|
|
1,664 |
|
|
4,066 |
|
|
5,496 |
|
|
| Total other income, net |
|
1,552 |
|
|
1,534 |
|
|
3,886 |
|
|
5,040 |
|
|
| 税引前損失 |
|
(28,602) |
|
|
(27,361) |
|
|
(85,390) |
|
|
(74,074) |
|
|
| 法人税等 |
|
(104) |
|
|
(37) |
|
|
(231) |
|
|
(49) |
|
|
| 純損失 |
|
$ |
(28,706) |
|
|
$ |
(27,398) |
|
|
$ |
(85,621) |
|
|
$ |
(74,123) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| 1株当たり当期純損失:基本的および希薄化後 |
|
$ |
(0.20) |
|
|
$ |
(0.24) |
|
|
$ |
(0.65) |
|
|
$ |
(0.68) |
|
|
|
|
|
|
|
|
|
|
|
|
| 加重平均発行済み普通株式:基本的および希薄化後 |
|
143,769,552 |
|
|
113,613,488 |
|
|
132,114,850 |
|
|
108,665,095 |
|
|
|
|
|
|
|
|
|
|
|
|
Absci Corporation
未監査の要約連結貸借対照表
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
September 30, |
|
December 31, |
| (単位:千米ドル、ただしシェアおよび1株当たりのデータを除く) |
|
2025 |
|
2024 |
| 資産 |
|
|
|
|
| 流動資産: |
|
|
|
|
| 現金および現金同等物 |
|
$ |
9,476 |
|
|
$ |
41,213 |
|
| 制限付き現金 |
|
16,342 |
|
|
15,947 |
|
| 市場性のある有価証券 |
|
142,999 |
|
|
71,212 |
|
| 売掛金(純額) |
|
1,000 |
|
|
— |
|
| 前払費用およびその他の流動資産 |
|
5,177 |
|
|
5,459 |
|
| 流動資産合計 |
|
174,994 |
|
|
133,831 |
|
| オペレーティング・リース使用権資産 |
|
3,190 |
|
|
3,968 |
|
| 有形固定資産(純額) |
|
23,016 |
|
|
29,167 |
|
| Intangibles, net |
|
42,356 |
|
|
44,883 |
|
| Restricted cash, long-term |
|
1,053 |
|
|
1,054 |
|
|
|
|
|
|
| Other long-term assets |
|
383 |
|
|
705 |
|
| 資産合計 |
|
$ |
244,992 |
|
|
$ |
213,608 |
|
| 負債および株主資本 |
|
|
|
|
| 現在の負債: |
|
|
|
|
| 買掛金 |
|
$ |
4,586 |
|
|
$ |
3,529 |
|
| 未払費用 |
|
8,229 |
|
|
6,842 |
|
| Contingent consideration |
|
12,750 |
|
|
12,750 |
|
| 長期債務 |
|
1,306 |
|
|
2,733 |
|
| Operating lease obligations |
|
1,754 |
|
|
1,608 |
|
| Financing lease obligations |
|
2 |
|
|
78 |
|
| 繰延収益 |
|
1,081 |
|
|
1,116 |
|
| 流動負債合計 |
|
29,708 |
|
|
28,656 |
|
| 長期借入債務(1年以内返済予定分を除く |
|
65 |
|
|
1,257 |
|
| オペレーティング・リース債務(1年以内返済予定分を含む |
|
3,093 |
|
|
4,429 |
|
|
|
|
|
|
|
|
|
|
|
| Deferred revenue, long-term |
|
|
|
— |
|
| その他の固定負債 |
|
1,786 |
|
|
133 |
|
| 負債合計 |
|
34,652 |
|
|
34,475 |
|
|
|
|
|
|
| 株主資本 |
|
|
|
|
| 優先株式 |
|
— |
|
|
— |
|
| 普通株式 |
|
15 |
|
|
12 |
|
| 資本準備金 |
|
805,047 |
|
|
688,726 |
|
| 累積赤字 |
|
(595,222) |
|
|
(509,601) |
|
| その他の包括利益(損失)累計額) |
|
500 |
|
|
(4) |
|
| 株主資本合計 |
|
210,340 |
|
|
179,133 |
|
| 負債および株主資本合計 |
|
$ |
244,992 |
|
|
$ |
213,608 |
|
|
|
|
|
|


















































 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン