Document
Exhibit 99.1
ミルーム・ファーマシューティカルズ社、2024年製品売上高および現金残高の速報値(未監査)と企業最新情報を発表
–2024 製品売上高は約3億3,600万ドルとなり、ガイダンス範囲の上限を上回る。
–2025 全世界での製品売上高は4億2,000万ドルから4億3,500万ドルと予想
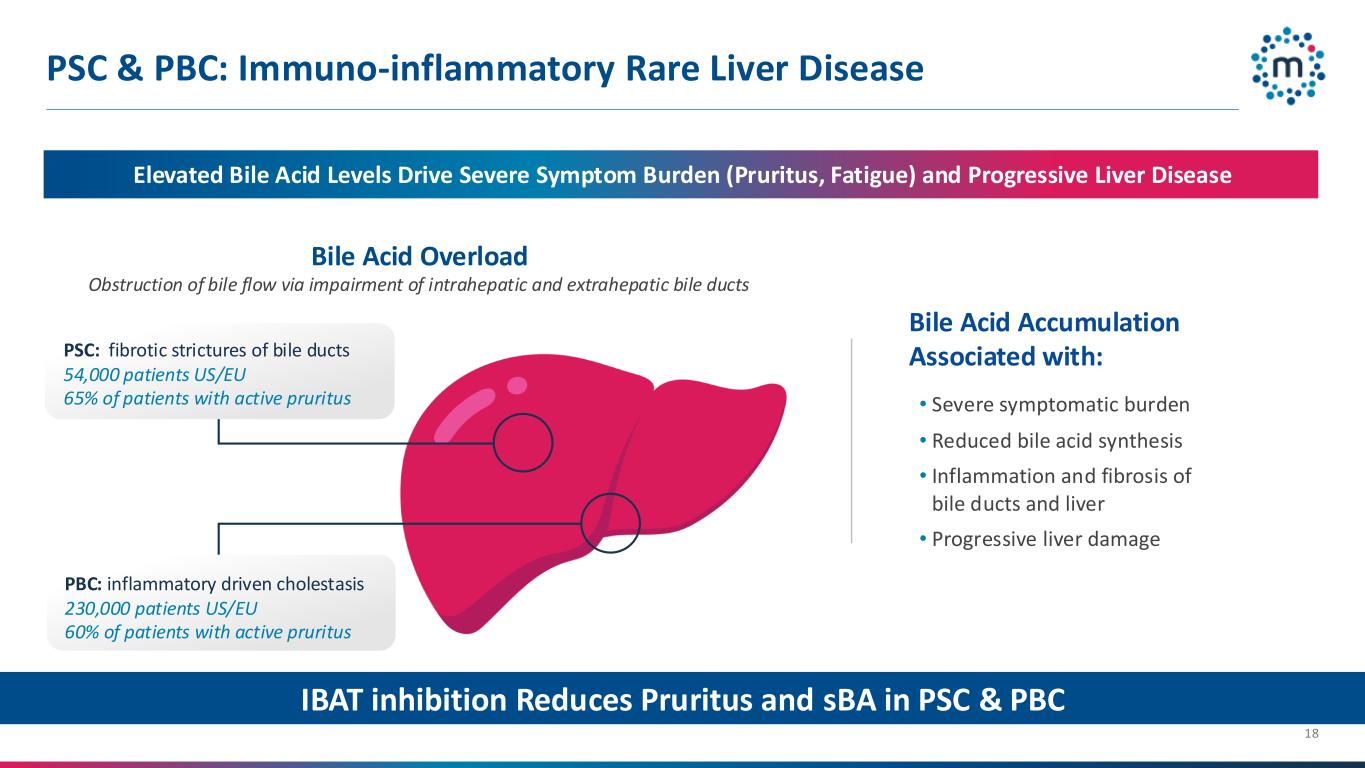
–原発性硬化性胆管炎を対象としたvolixibatのVISTAS試験は2025年後半に登録完了の見込み、トップラインデータは2026年の見込み
カリフォルニア州フォスターシティ発-2025年1月13日-ミルーム・ファーマシューティカルズ・インク(Nasdaq: MIRM)は本日、2024年通年の製品売上高、期末現金残高、企業の最新情報、2025年通年の見通しについて、予備的かつ未監査の見込みを発表した。
「ミラム社のクリス・ピーツ最高経営責任者(CEO)は、「2024年はミラム社にとって重要な年となりました。「LIVMARLIの適応拡大、PSCおよびPBCにおけるvolixibatの良好な中間解析により、胆汁うっ滞性疾患におけるリーダーシップを継続しました。さらに、チェノジオールの新薬承認申請とフラジャイルX症候群に対するMRM-3379の導入により、希少遺伝性神経領域での取り組みを前進させました。超希少疾患における実証済みの商業的実行力と、より大きな適応症における魅力的なパイプラインにより、当社は今後数年間、持続的な成長に向けて十分な態勢を整えられると確信しています」。
Future Expectations and Milestones
-2025年のガイダンス:全世界での製品純売上高が約4億2000万ドルから4億3500万ドルとなり、営業キャッシュフローがプラスとなることから、継続的な収益成長を見込む
-原発性硬化性胆管炎(PSC)を対象としたVolixibat VISTAS試験は2025年後半に登録完了の見込み、トップラインデータは2026年の見込み
-原発性胆汁性胆管炎(PBC)を対象としたVolixibat VANTAGE試験は2026年に登録完了の見込み
-LIVMARLI EXPAND 稀な胆汁うっ滞性疾患におけるそう痒症を対象としたフェーズ3試験 2026年に登録完了予定
-脳腱性黄色腫症(CTX)に対するチェノジオールのFDA処方薬ユーザーフィー法(PDUFA)期限は2025年3月28日
-フラジャイルX症候群(FXS)を対象としたMRM-3379のフェーズ2試験を2025年に開始予定
2024 Highlights
コマーシャル肝疾患と遺伝性神経学のフランチャイズで希少疾患におけるリーダーシップを継続
-2024年のLIVMARLI製品の推定売上高は約2億1300万ドル、CHOLBAMおよびCHENODAL製品の推定売上高は約1億2300万ドル
-LIVMARLIの売上高約6,400万ドル、CHOLBAMおよびCHENODALの売上高約3,500万ドルを含む、2024年第4四半期の推定製品売上高合計約9,900万ドル
-欧州4大市場での償還交渉と上市の成功を含め、30カ国で商業アクセスが可能に。
規制とパイプライン:複数の希少疾患と大規模な希少疾病におけるMirum社のリーダーシップの拡大
-VISTAS PSCおよびVANTAGE PBC試験におけるボリキシバットの中間解析結果が良好である。
-米国食品医薬品局(FDA)よりPBCにおける胆汁うっ滞性そう痒症の治療薬としてボリキシバットの画期的治療薬指定を受ける
-ボリキシバットがPBCにおける胆汁うっ滞性そう痒症の治療薬としてFDAより希少疾病用医薬品指定を受ける
-LIVMARLIがFDAより12ヵ月以上の進行性家族性肝内胆汁うっ滞(PFIC)患者における胆汁うっ滞性そう痒症の適応で承認
-LIVMARLIが欧州で生後3ヵ月以上のPFIC治療薬として承認
-希少な胆汁うっ滞性疾患におけるそう痒症を対象としたLIVMARLI EXPANDフェーズ3試験を開始
-CTXにおけるチェノジオールの新薬承認申請について
-FXSに対するPDE4D阻害剤MRM-3379の全世界におけるライセンス供与
企業および財務:持続的な財務力
-2024年第3四半期に営業キャッシュフローが黒字化
-2023年12月31日時点の2億8630万ドルに対し、2024年12月31日時点では約2億8700万ドルの現金、現金同等物および投資。
-ジョアン・クアン医学博士のチーフ・メディカル・オフィサー就任を発表
2024年12月31日現在の財政状態および経営成績をより完全に理解するためには、追加の情報および開示が必要である。2024年12月31日現在の財政状態および経営成績をより完全に理解するためには、追加的な情報および開示が必要となる。
ミルーム社は、2025年1月15日(水)午前9時45分(PT)よりサンフランシスコで開催される第43回J.P.モルガン・ヘルスケア・カンファレンスでプレゼンテーションを行う。このプレゼンテーションと質疑応答はウェブキャストで生中継され、ミルム社ウェブサイトの投資家およびメディアセクションからアクセスできます。ウェブキャストの再生は30日間可能である。
livmarli®(マラリキシバット)内用液について
LIVMARLI®(一般名:maralixibat)内用液は、回腸型胆汁酸トランスポーター(IBAT)阻害剤であり、小児の胆汁うっ滞性肝疾患の治療薬として米国食品医薬品局(FDA)より承認されています。米国では生後3カ月以上のアラジール症候群(ALGS)患者の胆汁うっ滞性そう痒症の治療薬として、欧州では生後2カ月以上の患者に対して承認されています。また、米国では生後12カ月以上の進行性家族性肝内胆汁うっ滞(PFIC)患者における胆汁うっ滞性そう痒症の治療薬として、欧州では生後3カ月以上のPFIC患者の治療薬として承認されています。米国在住の方は、LIVMARLI.comをご覧ください。
LIVMARLIは、ALGSおよびPFICタイプ2で画期的治療薬(Breakthrough Therapy)の指定を受け、ALGSおよびPFICで希少疾病用医薬品(Orphan Therapy)の指定を受けています。LIVMARLIは現在、第3相EXPAND試験において、胆汁うっ滞性そう痒症を追加適応として評価されています。現在進行中のLIVMARLIの臨床試験の詳細については、当社ウェブサイトの臨床試験セクションをご覧ください。
IMPORTANT SAFETY INFORMATION
使用制限:LIVMARLIは、胆汁酸塩輸出ポンプ(BSEP)タンパク質に重度の欠損を有するPFIC2型患者には使用できません。
livmarliは、以下のような副作用を引き起こす可能性があります。:
肝障害。ある種の肝機能検査値の変化はアラジール症候群やPFICの患者によくみられますが、治療中に悪化することがあります。これらの変化は肝障害の徴候かもしれません。PFICの場合、これは深刻で、肝移植や死に至る可能性があります。医療提供者は、治療開始前および治療中に血液検査や身体検査を行い、肝機能をチェックする必要があります。吐き気や嘔吐、皮膚や白目の部分が黄色くなる、尿が濃いまたは茶褐色になる、胃の右側(腹部)が痛む、胃のあたりが膨らむ、食欲がなくなる、出血やあざができやすくなるなど、肝臓障害の徴候や症状が現れたら、すぐに医療従事者に伝えてください。
胃や腸(胃腸)の問題。LIVMARLIは下痢や胃痛を含む胃や腸の問題を引き起こす可能性があります。医療提供者は、胃痛、下痢、血便または嘔吐を含む胃の問題の新規または悪化を観察するよう助言することがあります。これらの症状が通常よりも頻繁に、またはひどく現れた場合は、すぐに医療従事者に伝えてください。
体脂肪に蓄積される特定のビタミン(ビタミンA、ビタミンD、ビタミンE、ビタミンK)の量が少ないために起こる脂溶性ビタミン(FSV)欠乏症と呼ばれる状態は、アラジール症候群やPFICの患者によくみられますが、治療中に悪化することがあります。医療従事者は、治療開始前および治療中に血液検査を行い、一般的な副作用として報告されている骨折や出血を監視することがあります。
US Prescribing Information
EU SmPC
Canadian Product Monograph
About Volixibat
Volixibatは、回腸胆汁酸トランスポーター(IBAT)を選択的に阻害するように設計された経口低吸収薬である。Volixibatは、IBATを阻害することにより胆汁酸の再利用を阻害し、全身および肝臓内の胆汁酸を減少させることで、成人胆汁うっ滞性疾患の治療に新たなアプローチを提供する可能性がある。Volixibatは現在、原発性硬化性胆管炎(VISTAS試験)および原発性胆汁性胆管炎(VANTAGE試験)を対象としたフェーズ2b試験で評価されている。6月、ミルーム社は、VANTAGE試験(フェーズ2b試験)の中間結果について、ボリキシバットを投与された患者において、そう痒症が統計学的に有意に改善し、血清胆汁酸が有意に減少し、疲労感が改善したことを発表した。
新たな安全性シグナルは認められず、最も一般的な有害事象は下痢で、全例が軽度から中等度であった。
コールバン®(コール酸)カプセルについて
FDAは2015年3月、CHOLBAM®(コール酸)カプセルを、単一酵素欠損による胆汁酸合成障害の小児および成人患者、ならびにペルオキシソーム生合成障害-Zellwegerスペクトラム障害の患者の併用治療薬として初めて承認した。CHOLBAM®の有効性は、胆汁酸合成障害およびペルオキシソーム生合成障害の併用療法を対象とした臨床試験で実証されています。現在、推定200~300人の患者が治療の候補となっている。
CHOLBAM® (cholic acid) Indication
CHOLBAMは次のような胆汁酸である。
-単一酵素欠損による胆汁酸合成障害の治療。
-ゼルウィガースペクトラム障害を含むペルオキシソーム障害の補助的治療:肝疾患、脂肪性下痢、脂溶性ビタミンの吸収低下による合併症の症状を示す患者。
LIMITATIONS OF USE
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミア
会社開示情報をすべてご覧になるには株探プレミアムの登録が必
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレ
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報を
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めて
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施
会社開示情報をすべてご覧になるには株探プレミアムの登録が必
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要で
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30
会社開示情報をすべてご覧になるには株探プレミアムの登録
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧
Investor Contacts:
Andrew McKibben
ir@mirumpharma.com
Media Contact:
Erin Murphy
media@mirumpharma.com