Document
Exhibit 99.1
ゼンタリス製薬、2023年第3四半期決算と事業に関する最新情報を発表
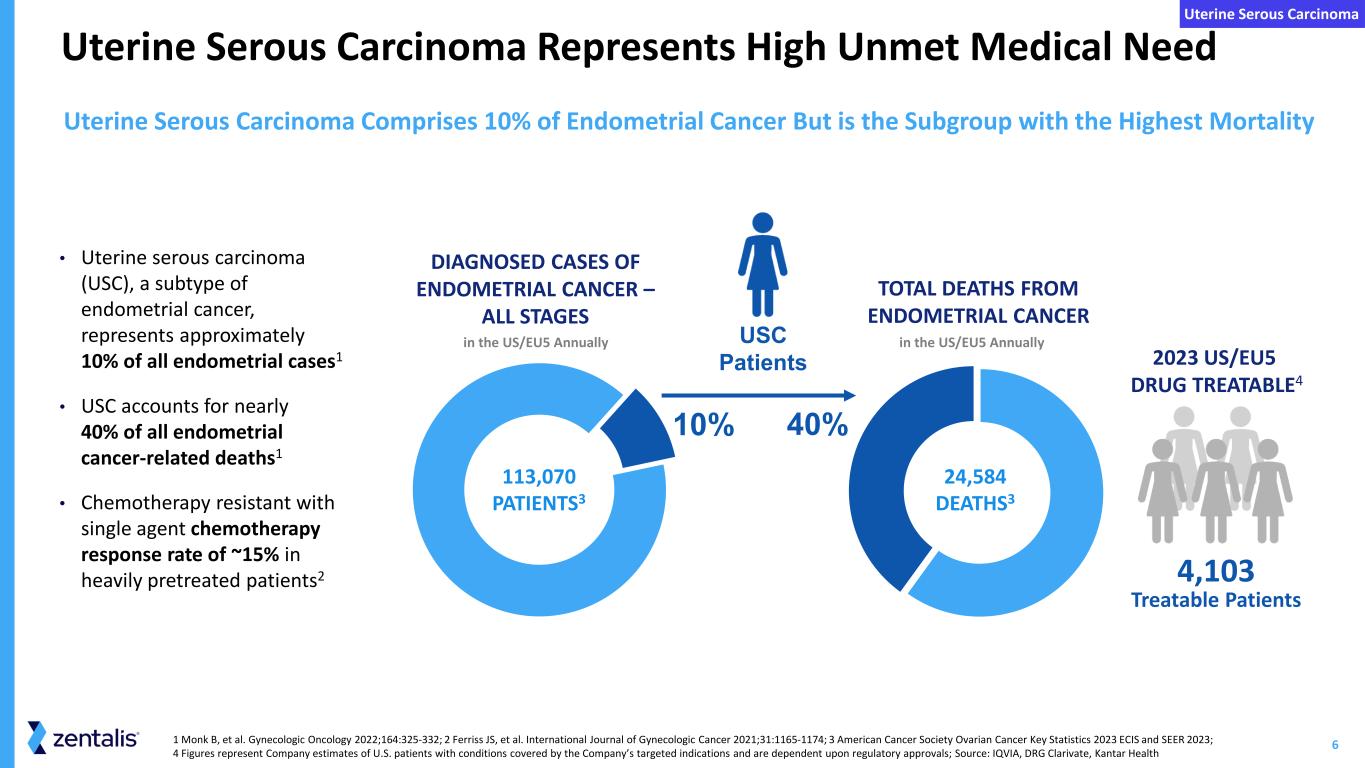
重度前治療歴のある卵巣がんおよび子宮漿液性がん患者を対象としたアゼノセルチブ単剤療法の更新試験で、追跡期間が延長され、ORR37%、mPFS6.5カ月というデータが得られた
アゼノセルチブ・プログラム、2026年の婦人科悪性腫瘍での最初の新薬承認申請に向けて順調に進展
アゼノセルチブとZN-d5の2026年までの主要臨床マイルストーンを共有
2023年9月30日現在の現金残高5億1,700万ドル。
共同創立者ケビン・バンカー博士の後任として、チーフ・トランスレーショナル・オフィサーのマーク・ラックナー博士がチーフ・サイエンティフィック・オフィサーに就任。
ニューヨークおよびサンディエゴ-2023年11月6日-がんの基本的な生物学的経路を標的とした臨床的に差別化された低分子治療薬の発見・開発を行う臨床段階のバイオ医薬品企業であるゼンタリス®・ファーマシューティカルズ・インク(Nasdaq: ZNTL)は本日、2023年9月30日に終了した四半期決算を発表し、最近の企業業績を強調しました。
「ゼンタリス社の最高経営責任者であるキンバリー・ブラックウェル医学博士は、「当社は、ファースト・イン・クラスかつベスト・イン・クラスのWEE1阻害剤であるアゼノセルチブの早期市場投入戦略を実行しており、同時に、複数の腫瘍型にまたがるアゼノセルチブのフランチャイズ・オポチュニティに向けた基礎固めも行っています。「アゼノセルチブは、卵巣癌と子宮漿液癌の両方において、単剤療法で非常に有望な抗腫瘍活性、安全性、忍容性を示し続けています。私たちは、卵巣がんと子宮漿液性がんの患者さんにこの有望な資産をできるだけ早く提供し、WEE1阻害が患者さんの転帰を改善する可能性のある他の適応症に拡大するために、臨床戦略を実行しています。当社のチームとリソースをアゼノセルチブの前進に集中させることにより、ゼンタリス社は婦人科悪性腫瘍におけるアゼノセルチブの最初の新薬承認申請を2026年に提出することを目標としています。"
「今期は、最高科学責任者(CSO)の引継ぎ計画も実行しており、最高トランスレーショナル責任者(CSO)であるマーク・ラックナーが、共同設立者であるケビン・バンカーの後を引き継ぐことになります。「有望な癌治療薬の発見に対するケビンの情熱は、当社の企業文化の礎であり、アゼノセルチブを含む4つの製品候補が臨床に進むことにつながりました。彼のゼンタリス社への多大な貢献と、私たちがサービスを提供する癌患者への貢献に感謝します。"
「昨年ゼンタリス社に入社して以来、マークは有能なトランスレーショナルチームを編成し、アゼノセルチブのバイオマーカー濃縮戦略の陣頭指揮を執ってきました。「マークがチーフ・サイエンティフィック・オフィサーに任命されたことで、我々のトランスレーショナルとディスカバリーの取り組みが一つの傘下に収まることになり、強固な前臨床創薬活動をサポートしながら、アゼノセルチブの臨床開発を進めていく上で、我々は強い立場に立つことができます。
Program Updates and Highlights
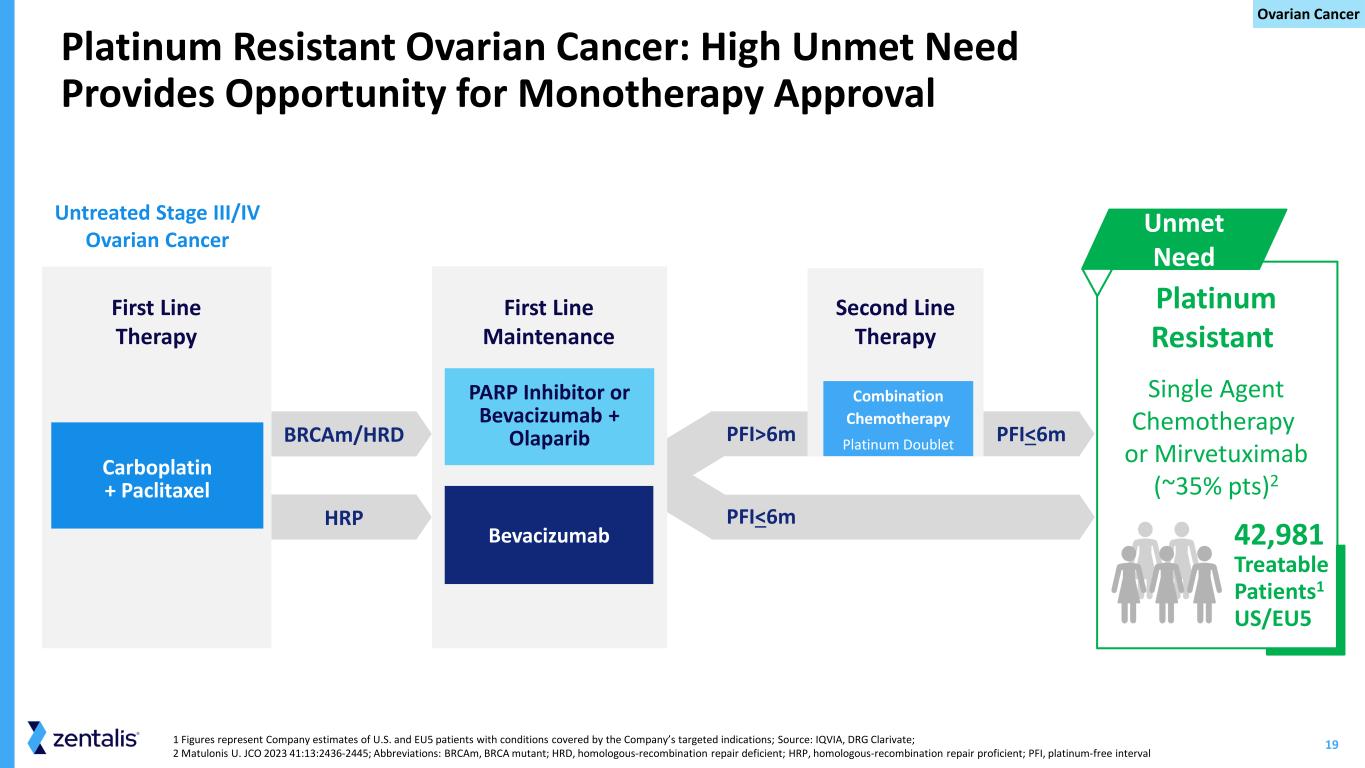
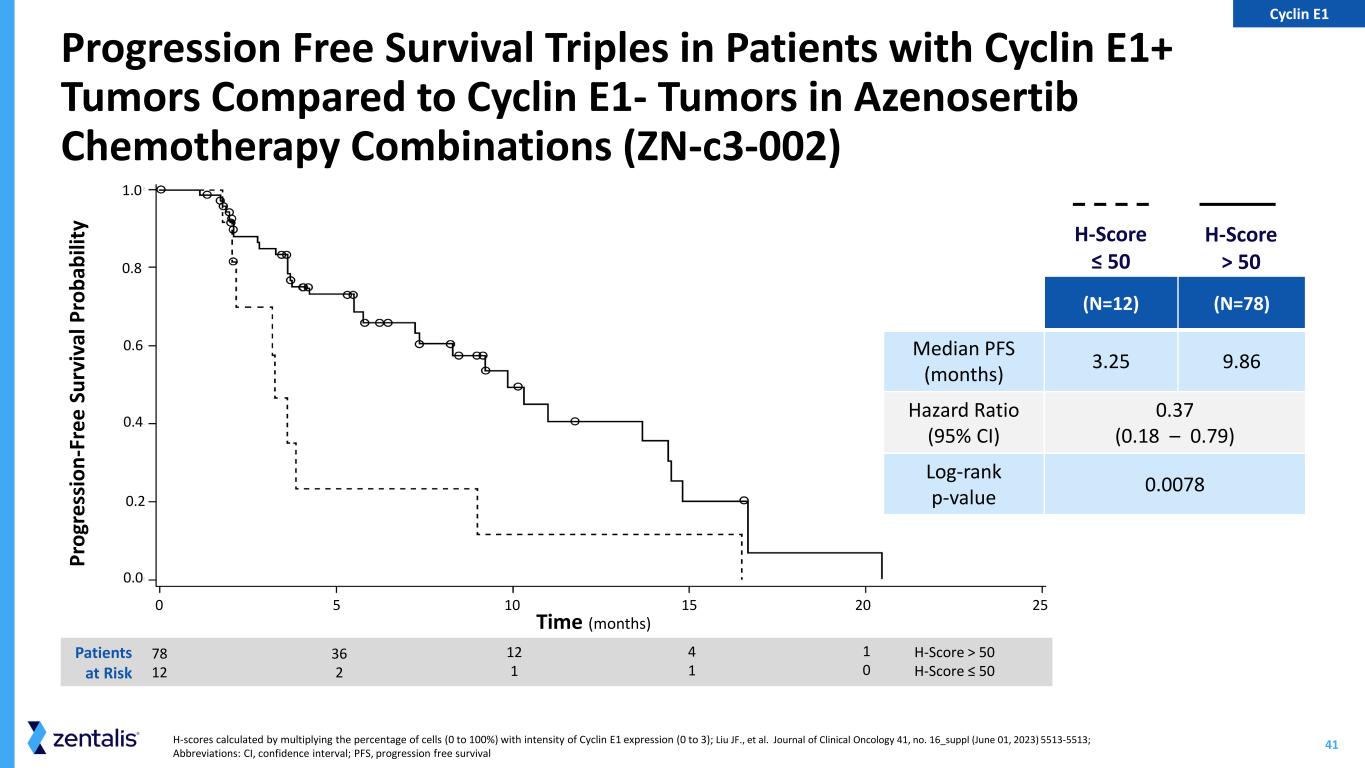
-アゼノセルチブ単剤療法プログラム当社は本日、固形がんを対象としたアゼノセルチブ単剤療法の第 1 相臨床試験(ZN-c3-001)の最新解析結果を発表しました。2023年6月6日に報告したデータと同じプラチナ製剤抵抗性または難治性の卵巣がんおよび子宮漿液がん(USC)患者19人において、客観的奏効率(ORR)は37%であった。
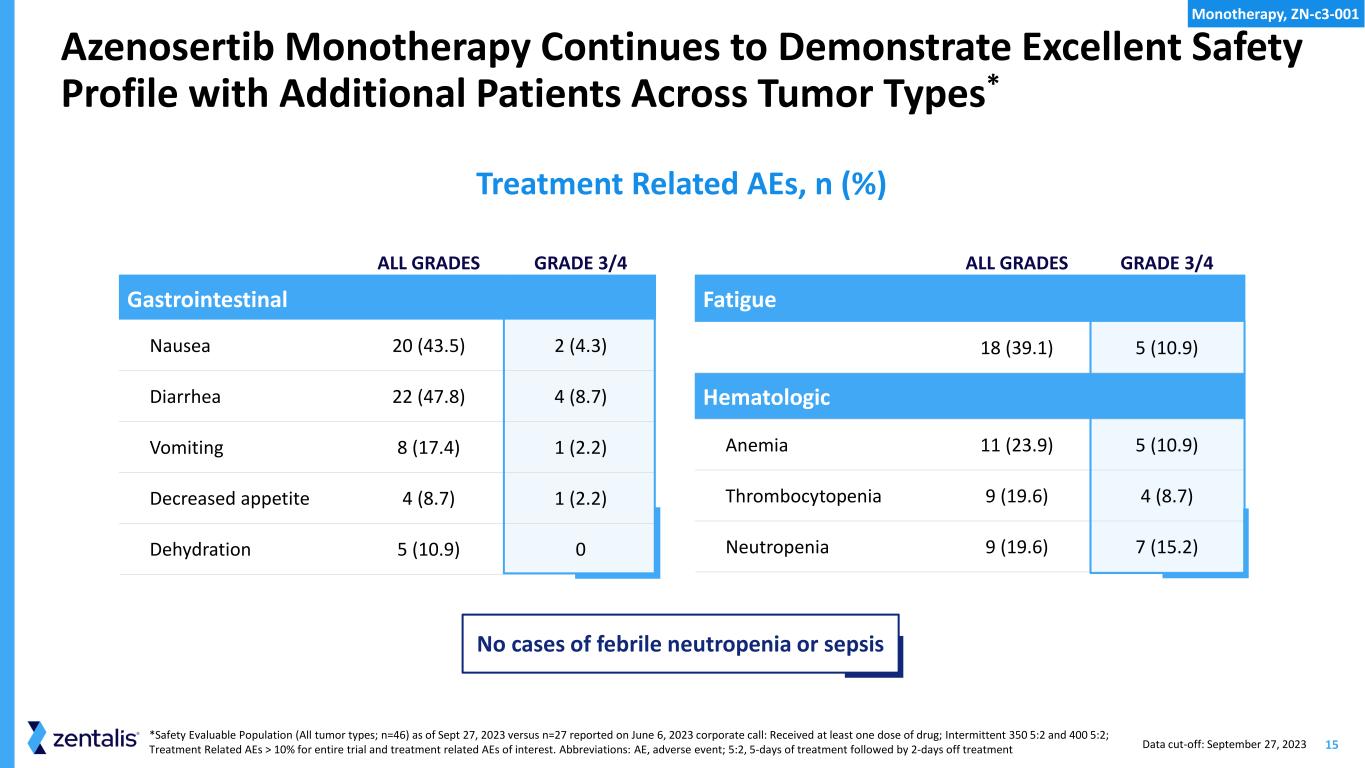
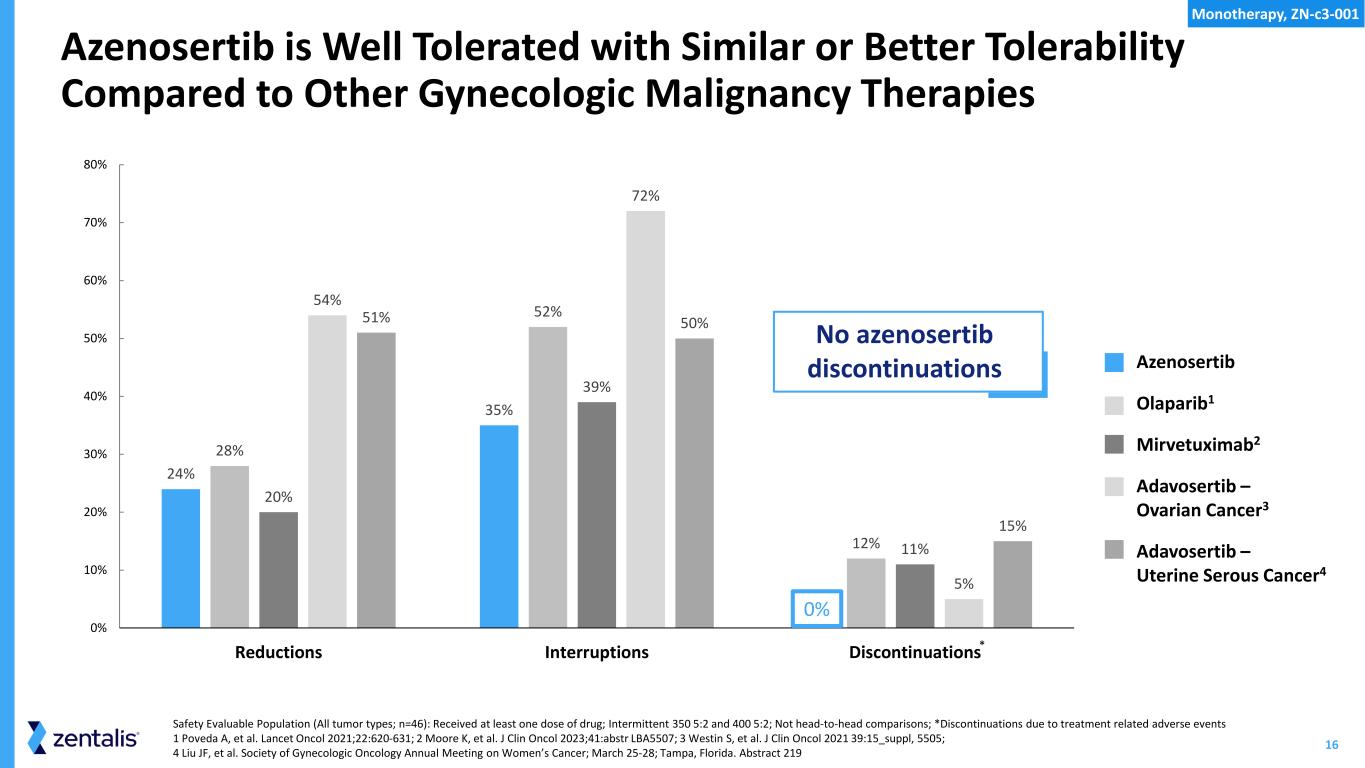
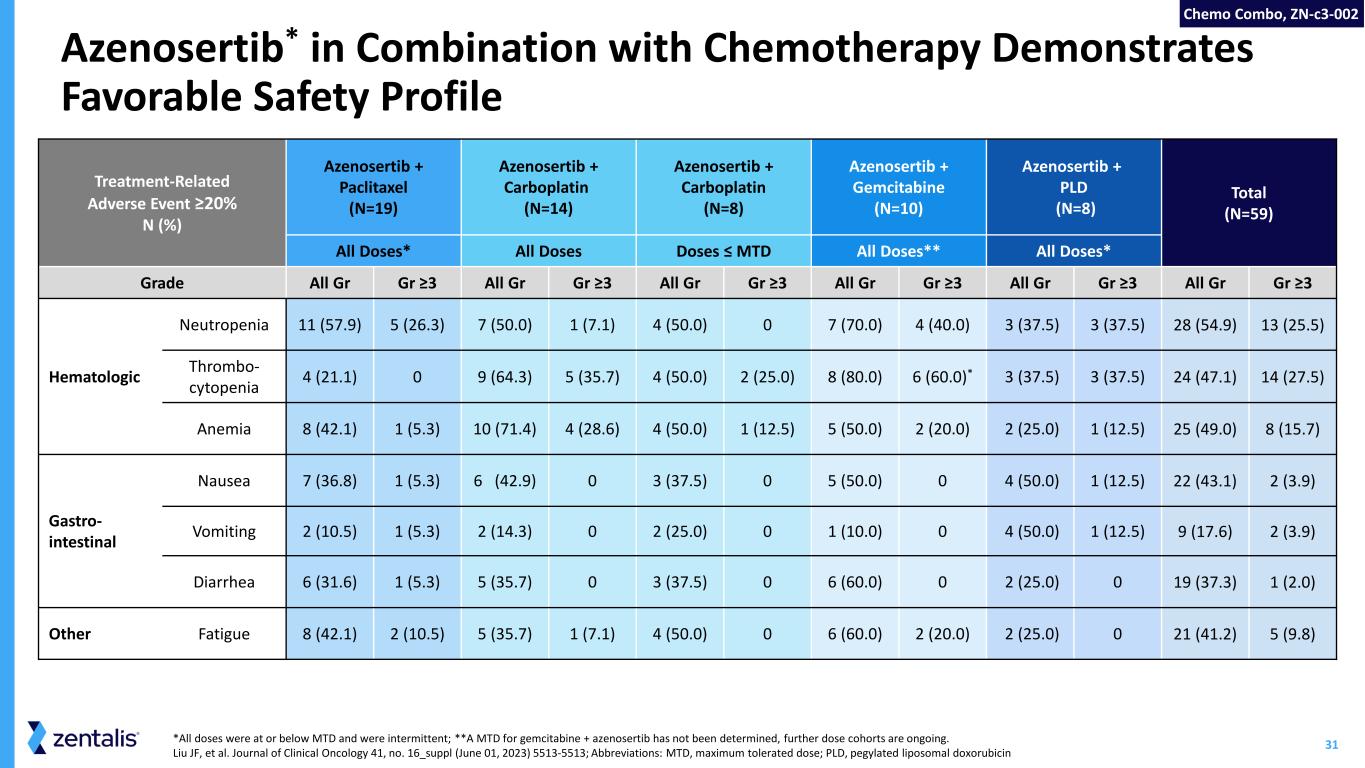
追跡調査期間の中央値は5カ月近く延長し、無増悪生存期間(mPFS)の中央値は6.5カ月に延長した。安全性評価対象症例が追加され、6月以降の追跡調査により、アゼノセルチブは引き続き、承認済みの卵巣がん治療薬と同等以上の良好な安全性および忍容性プロファイルを示しており、本薬の継続的な前進を支持しています。
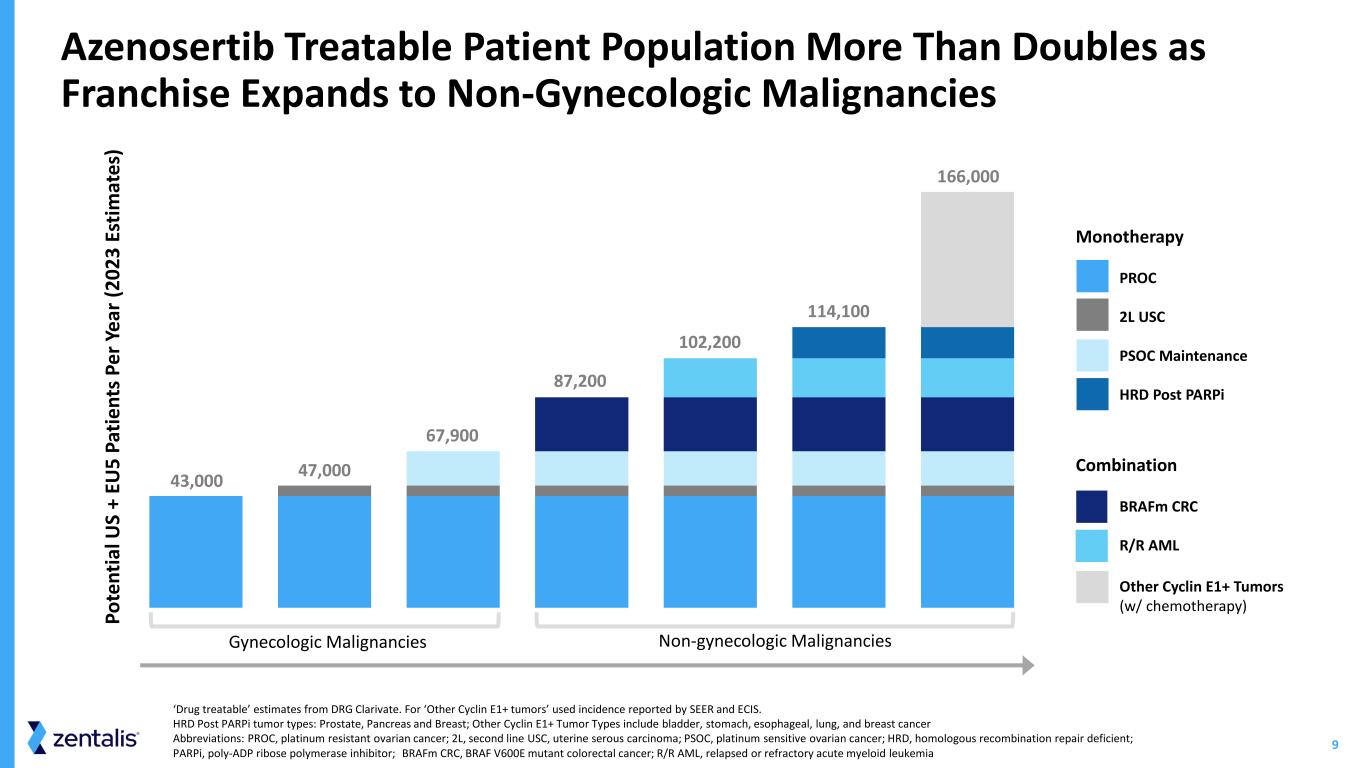
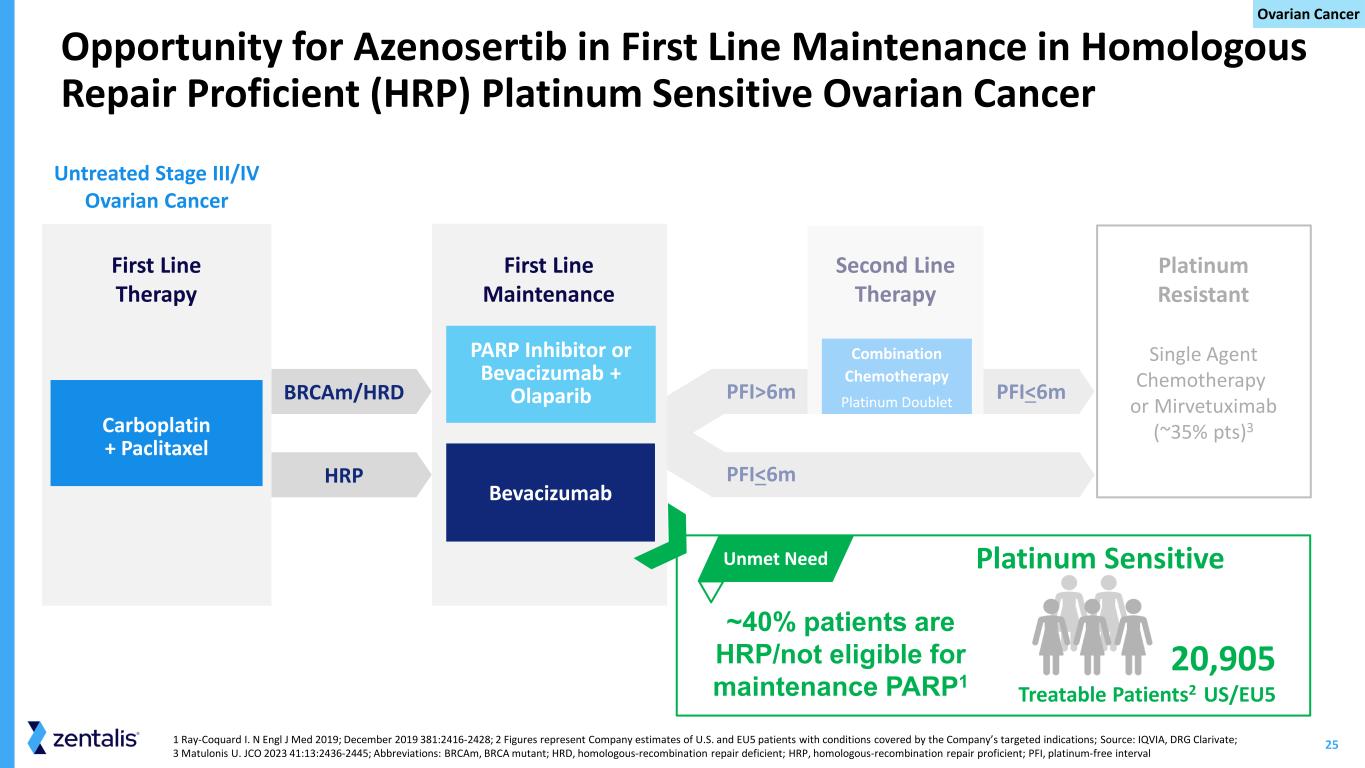
-アゼノセルチブの開発戦略アゼノセルチブは現在、10以上の進行中および計画中の臨床試験において、単剤療法として、また幅広い腫瘍型において説得力のある科学的根拠のある併用療法として評価されている。当社は、婦人科悪性腫瘍におけるアゼノセルチブの最初の新薬承認申請(NDA)を2026年に提出する予定である。当社は、プラチナ製剤感受性卵巣がん(PSOC)における戦略を見直し、PSOCにおけるアゼノセルチブの評価を、臨床におけるファーストライン(1L)維持療法で行う予定である。この戦略により、より多くの卵巣がん患者に利益をもたらし、1L維持療法における標準治療が進化し、選択肢が少なくなっているため、治療パラダイムのギャップを埋める機会を得ることができます。当社は2024年後半に本試験の詳細を発表する予定であり、2025年に登録を開始する予定である。
-米国癌研究協会(AACR)特別会議にて発表:卵巣がん当社は、10月にボストンで開催されたAACR Special Conferenceにおいて、「Cyclin E1 Positive Staining Is Frequent and Independent of Prior Platinum Treatment in High Grade Serous Ovarian Cancer」と題するポスター発表を行った:ボストンで開催されたAACR Special Conference: Ovarian Cancerで発表された。データの詳細については、こちらをクリックしてください。
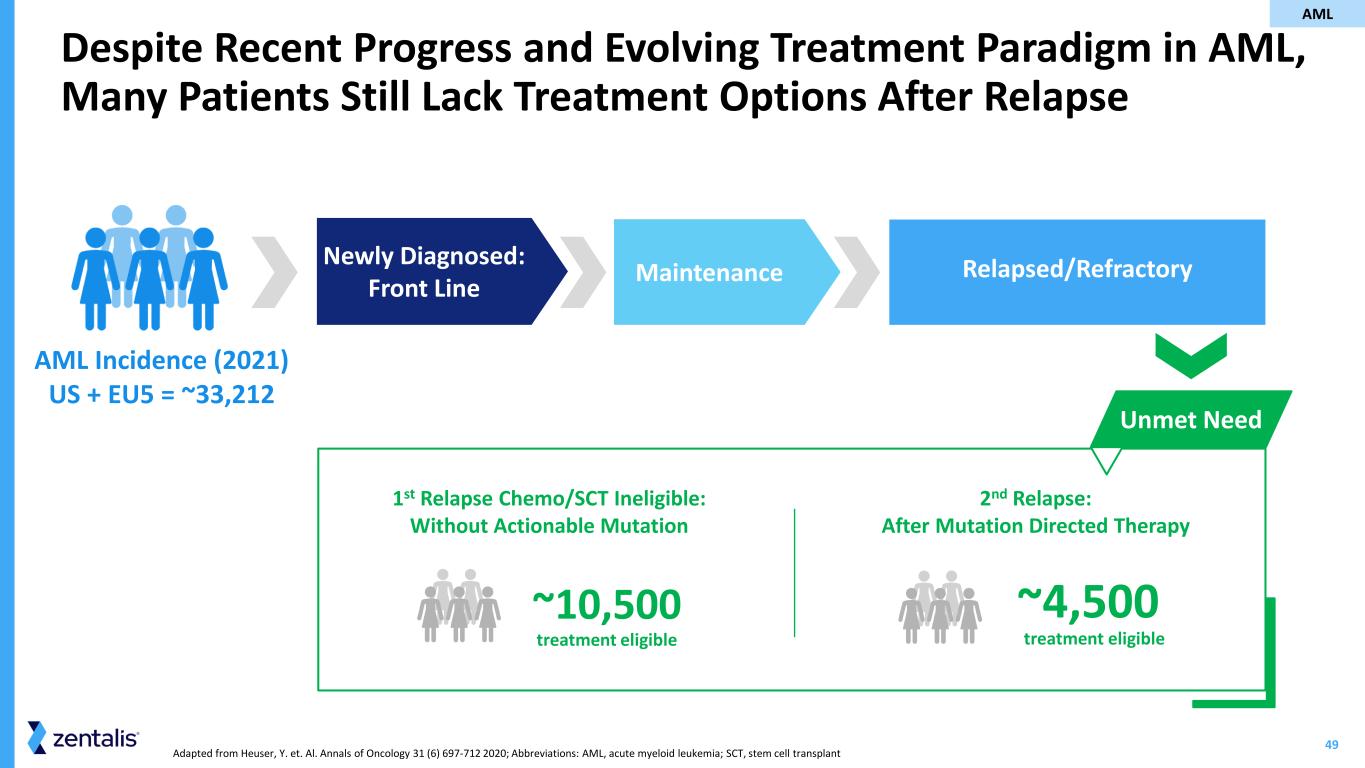
-再発または難治性の急性骨髄性白血病(R/R AML)に対するZN-d5+アゼノセルチブ。ゼンタリス社は、WEE1阻害剤であるアゼノセルチブとBCL-2阻害剤であるZN-d5の両方を臨床開発中である唯一の企業である。当社は、これらの有望な製品候補の併用による高い相乗的抗白血病活性を示す強力な前臨床データに基づき、重篤な前治療歴のあるR/R AML患者を対象とした第1/2相試験で、これらの製品候補の併用を評価している。当社は、本試験の初期データを共有するガイダンスを2024年後半に更新した。
-再発または難治性の軽鎖アミロイドーシス(R/R ALアミロイドーシス)に対するZN-d5。R/R型ALアミロイドーシスを対象としたZN-d5単剤療法の第1相試験において、用量漸増が完了した。R/R型ALアミロイドーシス患者において、ZN-d5を1日400mg以上投与した患者の血液学的奏効率は40%であり、予備的な有効性のシグナルが観察された。ZN-d5の忍容性は良好で、治療に関連した有害事象はほとんど認められなかった。ZN-d5の単剤療法での投与量は1日800mgとされている。当社は、アゼノセルチブ+ZN-d5併用療法を含むアゼノセルチブ・フランチャイズにリソースを集中させるため、この適応症でのZN-d5のさらなる開発を計画していない。
Corporate Highlight
-当社は本日、バイオマーカー戦略担当のチーフ・トランスレーショナル・オフィサーであるマーク・ラックナー博士が、共同設立者であるケビン・バンカー博士の後任として、本年末をもってチーフ・サイエンティフィック・オフィサーに就任することを発表しました。バンカー博士は、引継ぎ後も顧問として当社への貢献を継続する。ラックナー博士は2022年10月にゼンタリスに入社した。ゼンタリス社入社以前は、IDEAYA Biosciences社で生物学およびトランスレーショナル・サイエンス部門の責任者である上級副社長を務め、3つの低分子化合物の開発候補に貢献する生物学的研究を成功裏に導くとともに、強力なトランスレーショナル・チームを設立し、新規の併用バイオマーカー戦略の発見に導いた。それ以前は、ジェネンテック社に10年以上勤務し、複数の責任ある職務を歴任した後、ジェネンテック社オンコロジーアーリーステージバイオマーカーグループの責任者を務めた。この在職中に、複数の
研究チームは、臨床試験の全フェーズにわたって予測バイオマーカー戦略を開発・導入し、標的治療薬、免疫腫瘍薬、抗体薬物複合体を網羅する多様なバイオマーカー・ポートフォリオを管理している。
Anticipated Upcoming Milestones
-1H 2024
骨肉腫を対象としたアゼノセルチブ+化学療法(ゲムシタビン)第 1 相試験の最終結果(ZN-c3-003)
-2H 2024
固形がんを対象としたアゼノセルチブ単剤療法フェーズ1b試験の最終結果(ZN-c3-001)
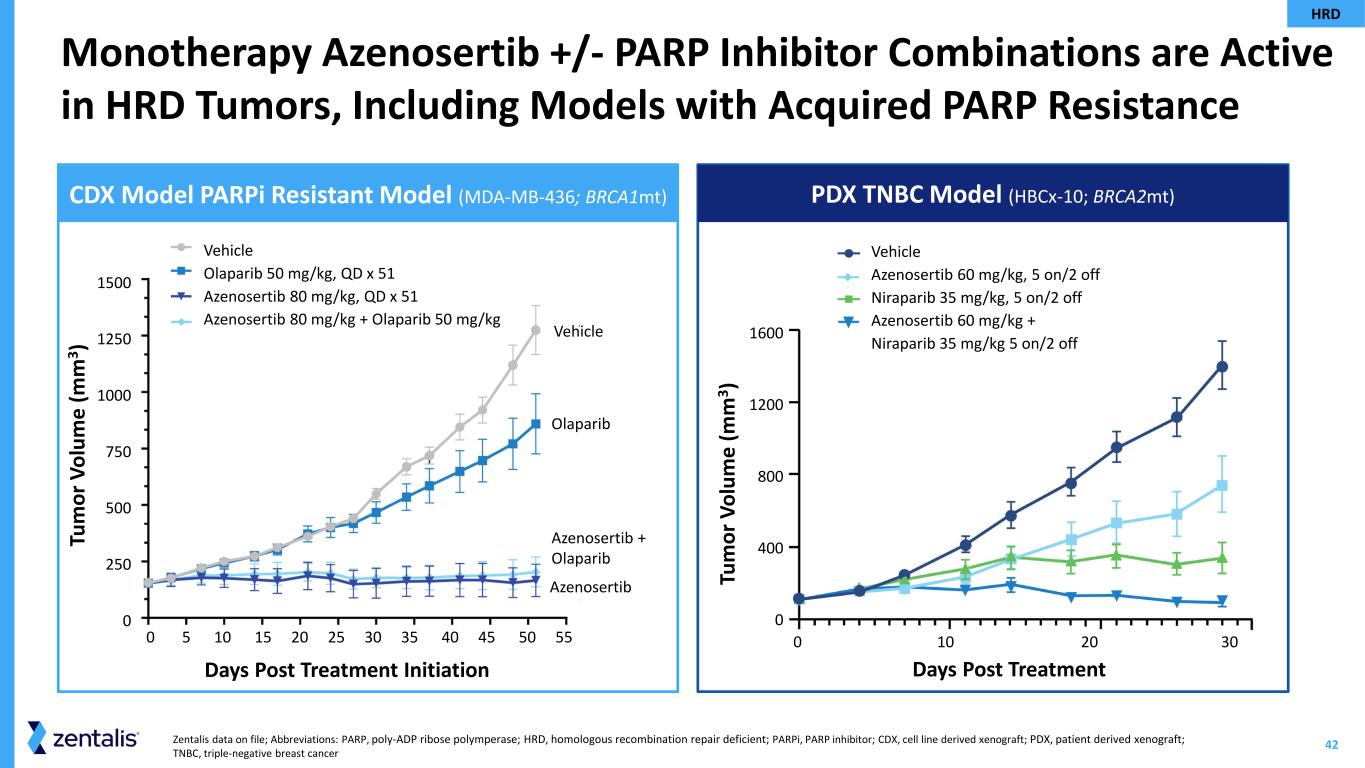
GSK社との提携によるプラチナ製剤抵抗性卵巣がんを対象としたアゼノセルチブ+PARP阻害剤(ニラパリブ)およびアゼノセルチブ単剤療法の第1/2相試験のトップラインデータ(MAMMOTH、ZN-c3-006)
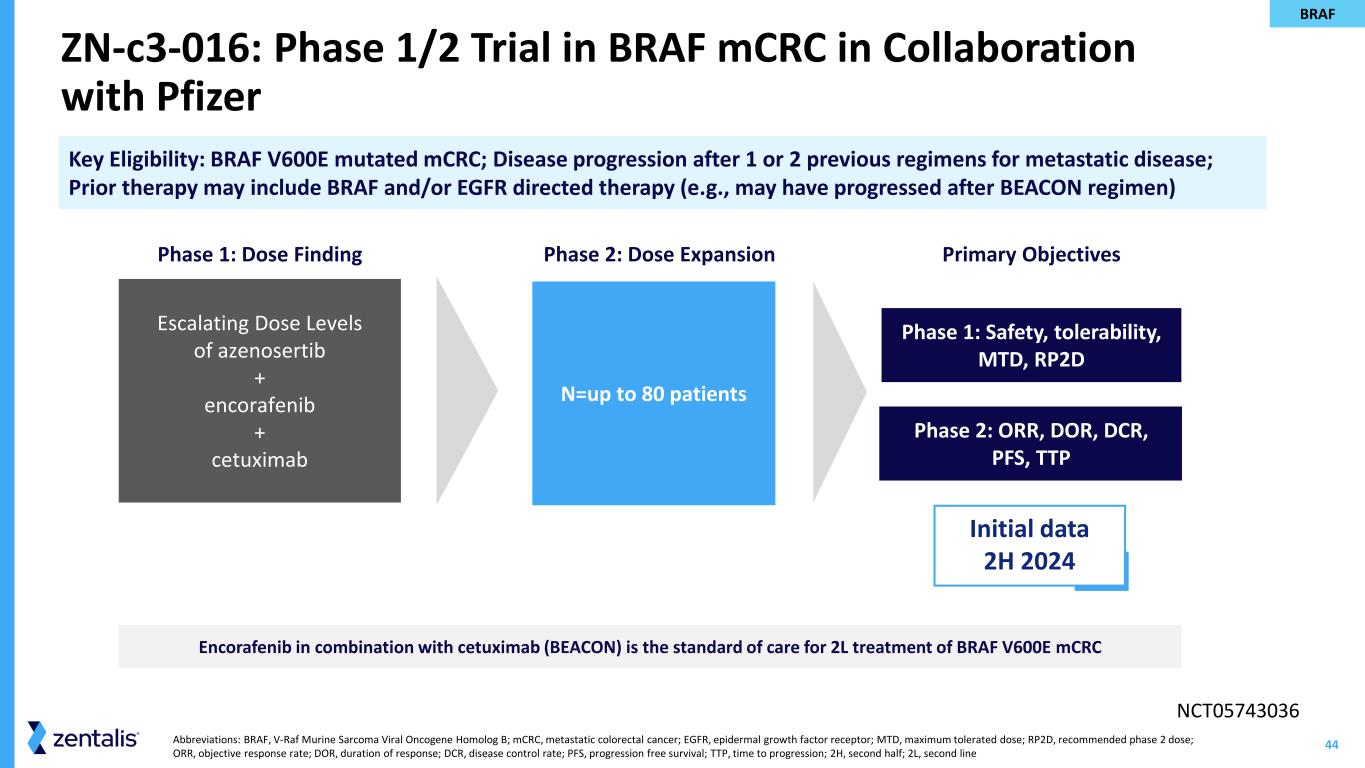
ファイザー社との提携によるBRAF遺伝子変異転移性大腸がんを対象としたアゼノセルチブ+BEACONレジメン(エンコラフェニブ+セツキシマブ)第Ⅰ相試験の初期データ(ZN-c3-016)
R/R型AMLを対象としたアゼノセルチブ+ZN-d5試験の第1相データ(ZN-d5-004C)
PSOC を対象としたアゼノセルチブの 1L 維持療法における臨床試験に関する追加情報 ◦ PSOC を対象としたアゼノセルチブの 1L 維持療法における臨床試験に関する追加情報
-1H 2025
プラチナ製剤抵抗性の高悪性度漿液性卵巣がんを対象としたアゼノセルチブ単剤療法の第 2 相試験のトップラインデータ (DENALI, ZN-c3-005)
-2H 2025
再発または持続性USCを対象としたアゼノセルチブ単剤療法の第Ⅱ相試験(TETON、ZN-c3-004)のトップラインデータ
-2025
PSOCにおけるアゼノセルチブの1L維持療法の臨床試験を開始する。
-2026
婦人科悪性腫瘍におけるアゼノセルチブの最初の新薬承認申請 ◦婦人科悪性腫瘍におけるアゼノセルチブの最初の新薬承認申請
2023年第3四半期決算のお知らせ
-現金および有価証券のポジション:2023年9月30日現在、ゼンタリス社は5億1,660万ドルの現金、現金同等物および有価証券を保有している。当社は、2023年9月30日現在の現金、現金同等物および有価証券は、2026年までの営業費用および資本支出に必要な資金を賄うのに十分であると考えている。
-研究開発費:2023年9月30日に終了した四半期の研究開発費(R&D)は、2022年9月30日に終了した四半期の4,220万ドルに対し、4,680万ドルであった。460万ドルの増加は主に、前期にゼンテラ社と共有した費用の320万ドル、人件費関連の260万ドルの増加(うち140万ドルは現金支出を伴わない株式ベースの報酬費用関連)、コンサルティング費用関連の0.8百万ドルによるものです。これらの増加は、施設費が130万ドル、臨床費用が0.7百万ドルそれぞれ減少したことにより一部相殺された。
-一般管理費:2023年9月30日に終了した四半期の一般管理費(G&A)は、2022年9月30日に終了した四半期の1,200万ドルに対し、1,600万ドルであった。この400万ドルの増加は主に人件費の290万ドルの増加によるもので、うち220万ドルは現金支出を伴わない株式報酬費用に関連するものであり、施設および外部サービスに関連する110万ドルの増加であった。
About Azenosertib
アゼノセルティブは、癌治療薬として開発中のファースト・イン・クラスおよびベスト・イン・クラスの低分子WEE1阻害剤である。DNA損傷応答キナーゼであるWEE1を阻害すると、がん細胞は損傷を受けたDNAを修復できないまま有糸分裂に移行し、細胞死に至る。現在、FDAが承認しているWEE1阻害剤はなく、アゼノセルチブは優れた選択性と薬物動態特性を持つように設計されている。アゼノセルチブは、アンメットニーズの高い治療領域で開発されており、単剤療法、化学療法との併用療法、分子標的薬との併用療法が評価されている。
About Zentalis Pharmaceuticals
は、がんの基本的な生物学的経路を標的とした臨床的に差別化された低分子治療薬の発見と開発を行う臨床段階のバイオ医薬品企業である。当社の主要製品候補であるアゼノセルチブ(ZN-c3)は、進行性固形癌および血液悪性腫瘍に対するファースト・イン・クラスおよびベスト・イン・クラスのWEE1阻害剤となる可能性がある。Azenosertibは、複数の臨床試験において単剤および併用療法として評価されており、幅広いフランチャイズポテンシャルを有している。臨床試験において、アゼノセルチブは良好な忍容性を示し、複数の腫瘍型における単剤療法および複数の化学療法との併用療法で抗腫瘍活性を示した。アゼノセルチブ臨床開発プログラムの一環として、当社はサイクリンE1陽性腫瘍や相同組換え欠損腫瘍など、ゲノム不安定性の高い腫瘍を標的とした濃縮戦略を模索している。また、癌生物学と創薬化学にわたる豊富な経験と能力を活用し、タンパク質分解剤の研究を進めている。ゼンタリス社はニューヨークとサンディエゴに拠点を置いている。
詳細はwww.zentalis.com。X/Twitterでは@ZentalisP、LinkedInではwww.linkedin.com/company/zentalis-pharmaceuticals。
Forward-Looking Statements
本プレスリリースには、1995年米国私募証券訴訟改革法の意味における将来予想に関する記述が含まれています。本プレスリリースに含まれる記述のうち、過去の事実に関するもの以外は、すべて将来の見通しに関する記述とみなされます。これには、アゼノセルチブがファースト・イン・クラスおよびベスト・イン・クラスになる可能性に関する記述、当社がアゼノセルチブの早期市場投入戦略を実行する可能性に関する記述、アゼノセルチブに関する有意義なフランチャイズを構築する可能性に関する記述、アゼノセルチブに関する機会に関する記述が含まれます;アゼノセルチブに関する有意義なフランチャイズを構築する可能性、複数の腫瘍型にわたるアゼノセルチブの機会、婦人科悪性腫瘍におけるアゼノセルチブの新薬承認申請計画およびその時期、PSOCにおけるアゼノセルチブの臨床における1L維持療法での評価計画およびその時期;アゼノセルチブがより多くの卵巣がん患者に利益をもたらし、治療パラダイムのギャップを埋める可能性、アゼノセルチブおよびZN-d5を含む当社製品候補の開発に関する計画、臨床試験の開始およびデータの公表に関する計画およびその時期、ならびにその他の重要なマイルストンを達成する当社の能力;アゼノセルチブの潜在的利益(その設計の潜在的利益、資産の潜在的価値、患者の転帰を改善する可能性を含む)、当社の最高科学責任者の後継者計画の実行計画、および当社の資金繰り。予想」、「確信」、「継続」、「設計」、「マイルストーン」、「予定通り」、「機会」、「計画」、「可能性」、「予測」、「有望」、「戦略」、「支援」、「目標」、「~する」、「予定」および類似の言及は、将来の見通しに関する記述を識別することを意図していますが、すべての将来の見通しに関する記述がこれらの識別語を含むわけではありません。
これらの記述は約束でも保証でもありませんが、既知および未知のリスク、不確実性、およびその他の重要な要因を含んでおり、当社の実際の結果、業績、または実績が、将来の見通しに関する記述によって明示または暗示される将来の結果、業績、または実績と大きく異なる可能性があります:当社の営業実績が限られているため、現在の事業を評価し、将来の成功と実行可能性を予測することが困難である可能性があること、多額の損失を計上しており、今後も発生する見込みであること、追加資金が必要であるが、調達できない可能性があること、診断ツールの開発計画(その費用を含む)、当社の主力製品候補の成功に大きく依存していること;前臨床試験および初期臨床試験の結果は、その後の臨床試験の成功を予測できない可能性があること、追加の製品候補を同定できず、市場性のある製品を開発または商品化できないこと、臨床試験中に予期せぬ事象が発生し、遅延またはその他の不利な結果を招く可能性があること、規制当局の承認プロセスまたは継続的な規制上の義務に関するリスク、米国での承認取得の失敗、米国での承認取得の失敗、米国での承認取得の失敗、米国での承認取得の失敗、米国での承認取得の失敗、米国での承認取得の失敗、米国での承認取得の失敗。S.当社の製品候補が重篤な副作用を引き起こす可能性、提携関係を維持できない、または提携関係が破綻する可能性、第三者への依存、大規模な競合の影響、システム障害またはセキュリティ侵害の可能性、知的財産に関するリスク;当社の有能な人材を惹きつけ、維持し、意欲を高める能力、経営陣の交代に関連するリスク、公開企業として運営する結果生じる多額のコスト、および当社が最近提出したForm 10-KまたはForm 10-Qに関する定期報告書、およびそれ以降に米国証券取引委員会(SEC)に提出した書類に記載されている「リスク要因」の見出しで説明されているその他の重要な要因。米国証券取引委員会(SEC)およびその他のSEC提出書類に記載されている「リスク要因」の見出しで説明されているその他の重要な要因。このような将来の見通しに関する記述はすべて、本プレスリリースの日付時点における経営陣の推定を表しています。当社は将来のある時点でかかる将来予想に関する記述を更新することを選択する可能性がありますが、たとえ後発事象により当社の見解が変更されたとしても、当社はその義務を一切負いません。
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアム
Katie Beach Oltsik
Evoke Canale
Katherine.Beach@evokegroup.com
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方に
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報を














































 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン