Document
Exhibit 99.1
アキュメン・ファーマシューティカルズ、2024年第2四半期決算と業績ハイライトを発表
-初期アルツハイマー病治療薬sabirnetug(ACU193)を検討するフェーズ2試験ALTITUDE-ADに被験者を積極的に登録中
-2024年7月にサビルネツグの皮下投与を支持する第1相試験で最初の被験者を投与し、2025年第1四半期にトップライン結果が予想される。
-2024年6月30日現在の現金、現金同等物および有価証券は2億8,140万ドルで、2027年前半まで現在の臨床および事業活動を支えることができる見込み。
-本日午前8時(米国東部時間)より、電話会議とウェブキャストを行なう。
マサチューセッツ州ニュートン、2024年8月13日 - アルツハイマー病(AD)治療薬として毒性の可溶性アミロイドβオリゴマー(AβOs)を標的とする新規治療薬を開発する臨床段階のバイオ医薬品企業であるアキュメン・ファーマシューティカルズ・インク(NASDAQ:ABOS)(以下、「アキュメン」または「当社」)は本日、2024年第2四半期の業績を報告し、事業の最新情報を提供しました。
「私たちのチームは2024年の実行に非常に集中しており、上半期の進捗に非常に満足しています。今春開始したグローバル第2相ALTITUDE-AD試験では、被験者を積極的に登録しています。アキュメンの最高経営責任者(CEO)であるダニエル・オコネルは、次のように語っている。「sabirnetugの作用機序に対する治験担当医師や患者の関心の高さが、我々の予想を上回る速さで被験者登録が進んでいることに非常に勇気づけられました。「ALTITUDE-ADの進展に加え、7月にはsabirnetugの皮下投与を支持する第1相薬物動態比較試験の開始を発表しました。この健康ボランティア試験のトップライン結果は2025年第1四半期に出る予定です。当社の臨床プログラムの勢いとsabirnetugの毒性アミロイドβオリゴマーに対する明確な選択性により、当社は早期アルツハイマー病に対する次世代の治療薬を提供できる可能性があると確信しています。"
最近のハイライトと今後のマイルストーン
-2024年5月、サビルネツグの早期AD治療に対する臨床的有効性と安全性を検討するフェーズ2試験であるALTITUDE-ADにおいて、最初の患者への投与を発表。
-現在、米国、カナダ、英国、EUで50以上のサイトが稼動している。
-2024年7月、当社はフェーズ1薬物動態(PK)比較試験において、最初の被験者にsabirnetugの皮下製剤を投与したと発表した。本試験では、健常人を対象にsabirnetugの皮下投与と静脈内投与のPKプロファイルを比較する。
-トップライン結果は2025年第1四半期に期待される。
-2024年7月、当社はアルツハイマー病協会国際会議(AAIC®)年次総会において、早期ADを対象としたフェーズ1試験であるINTERCEPT-AD試験から得られた患者体験に関する知見に加え、バイオマーカーおよびターゲット関与に関する追加解析を発表した。
-この研究では、将来の臨床試験開発に役立つ臨床試験における患者の経験、サビルネツグの作用機序を裏付けるバイオマーカーデータ、および、血液から脳内に入るモノクローナル抗体の量が通常少量であることを考慮した、脳脊髄液(CSF)中のサビルネツグのレベルを検出する超高感度な方法が強調されている。研究の詳細はこちら
-当社は2024年10月2日にバーチャルR&Dデーを開催し、sabirnetugの科学的根拠、第1相臨床結果、第2相臨床計画について深く掘り下げる予定です。参加登録の詳細は開催前にお知らせします。
2024年第2四半期決算
-現金残高。2024年6月30日現在、現金、現金同等物および有価証券の合計は2億8,140万ドルで、2023年12月31日現在の現金、現金同等物および有価証券の合計は3億610万ドルであった。現金の減少は、進行中の事業の資金調達に関連している。現金は、2027年前半まで現在の臨床および事業活動を支えることができると予想される。
-研究開発費。研究開発費は、2023年6月30日に終了した3カ月間の910万ドルに対し、2024年6月30日に終了した3カ月間は1,950万ドルでした。研究開発費の増加は主に、ALTITUDE-ADに関連する開発業務受託機関およびその他の臨床試験費用の増加、ならびに人件費、ライセンス契約、出荷・梱包費用の増加によるものです。
-一般管理費。2024 年 6 月 30 日に終了した 3 ヶ月間の一般管理費は、2023 年 6 月 30 日に終了した 3 ヶ月間の 430 万ドルに対し、480 万ドルであった。G&A費の増加は主に人件費の増加によるものである。
-営業損失。営業損失は、前年同期の 1,350 万ドルに対し、2024 年 6 月 30 日に終了した 3 ヶ月間は 2,440 万ドルとなった。この増加は、研究開発費および販売管理費が前年同期より増加したことによるものである。
-純損失。2024年6月30日に終了した3ヵ月間の純損失は2,050万ドルであった(2023年6月30日に終了した3ヵ月間は1,160万ドル)。
Conference Call Details
アキュメンは本日8月13日午前8時(米国東部時間)より、電話会議およびライブ音声ウェブキャストを開催する。
ライブ電話会議に参加するには、このリンクから登録してください。登録後、PINを含むダイヤルイン番号をお知らせします。前日までにご登録ください。
ウェブキャストの音声はこのリンクから入手できる。
ウェブキャストのアーカイブ版は、当社ウェブサイトの投資家向けセクション(www.acumenpharm.com)にて少なくとも30日間ご覧いただけます。
About Sabirnetug (ACU193)
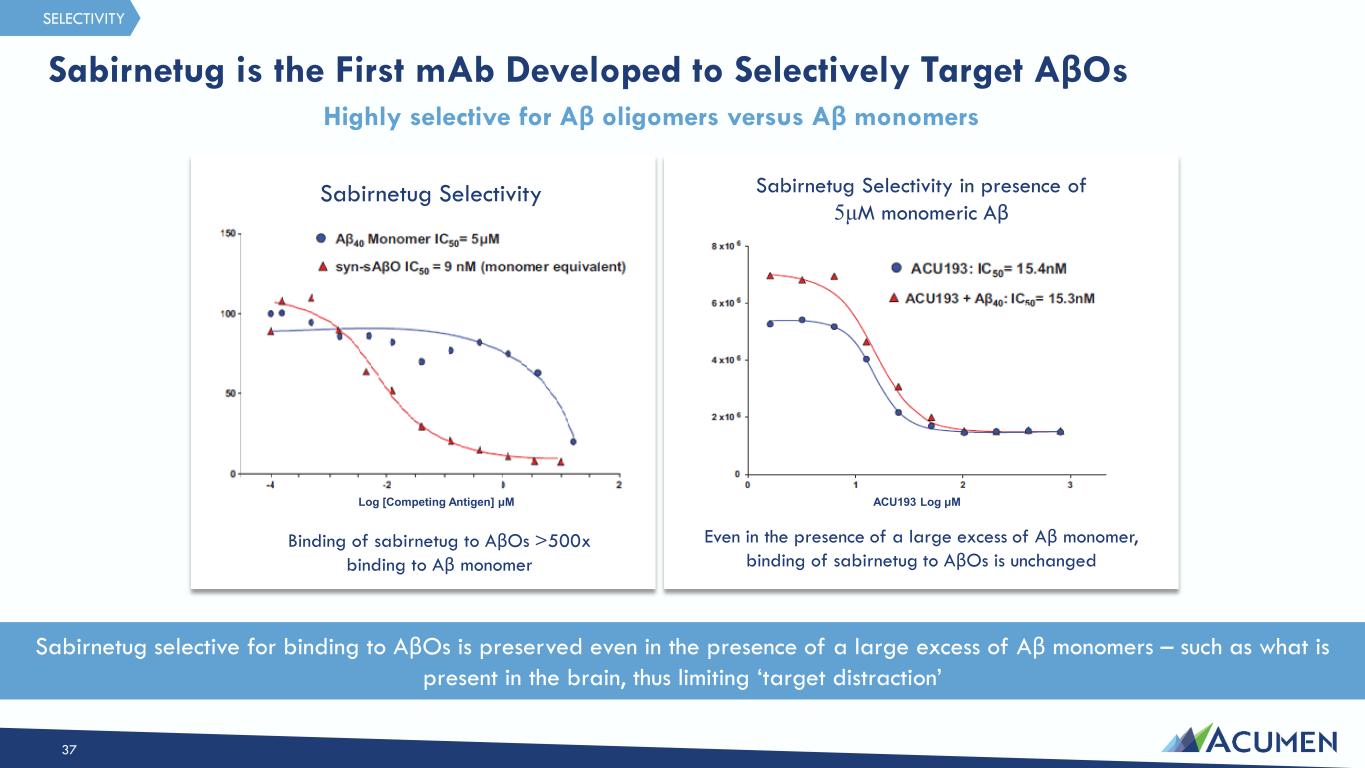
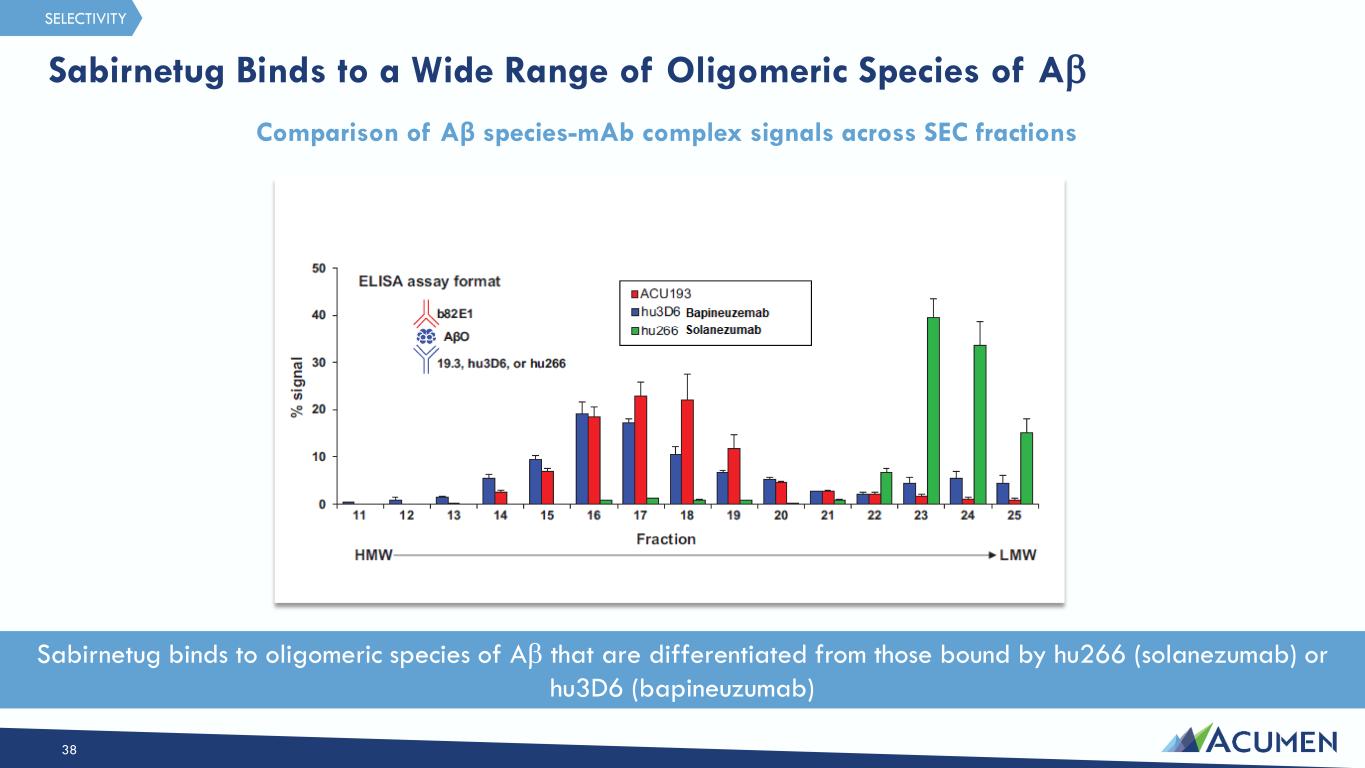
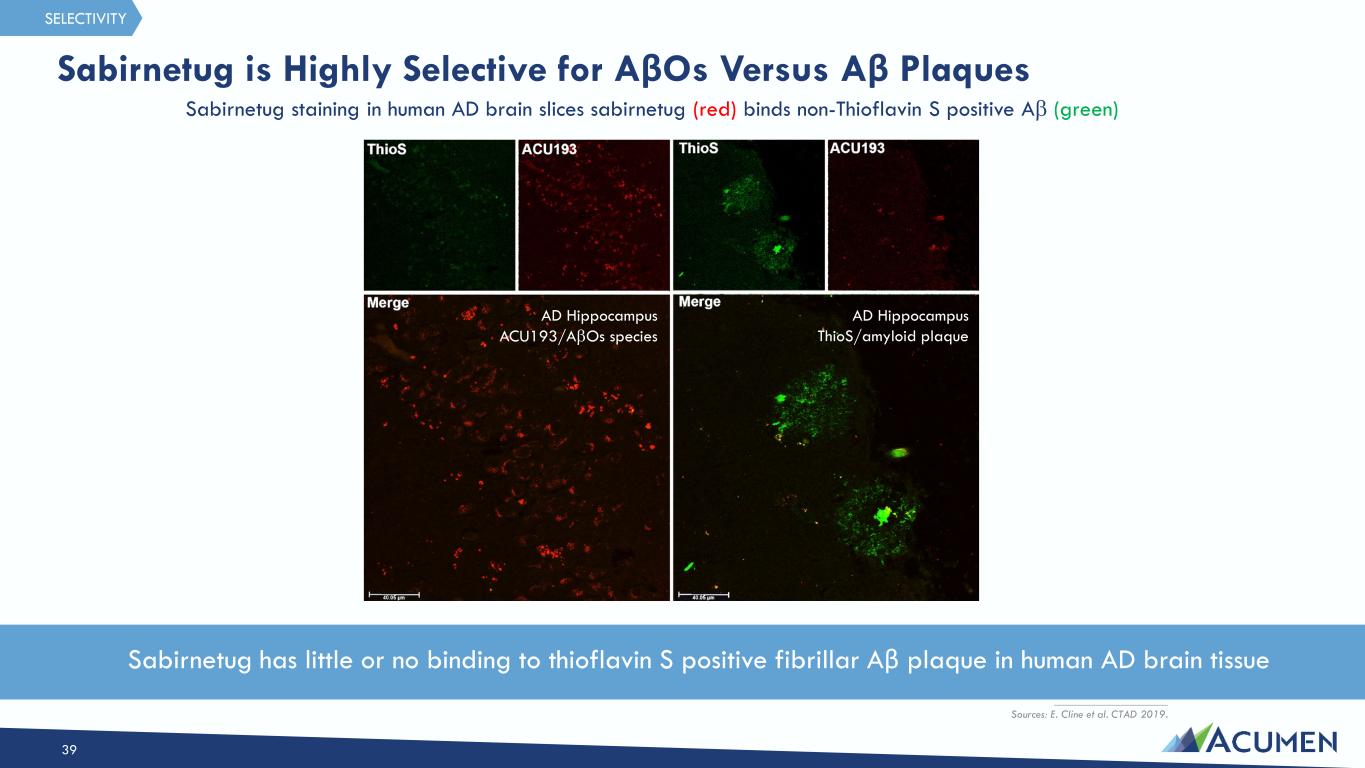
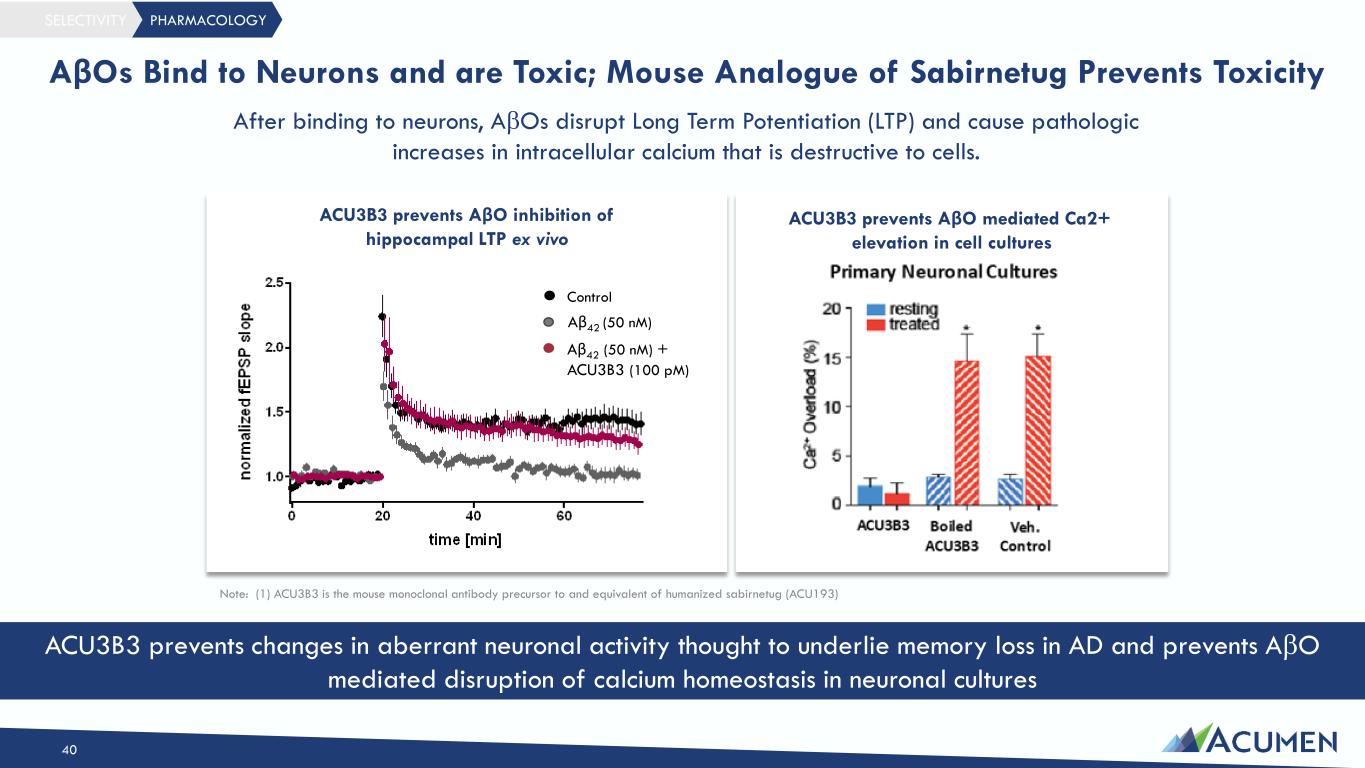
サビルネツグ(ACU193)は、Aβ単量体やアミロイド斑ではなく、Aβの中でも毒性が強く病原性の高い可溶性アミロイドβオリゴマー(AβOs)に対する選択性に着目して創製されたヒト化モノクローナル抗体(mAb)である。可溶性AβOsは、ニューロンに結合し、シナプス機能を阻害し、神経変性を引き起こす強力な神経毒であることが観察されている。sabirnetugは、毒性のある可溶性AβOを選択的に標的とすることで、可溶性AβOがアルツハイマー病(AD)における神経変性過程の早期かつ永続的な根本原因であるという仮説に取り組むことを目指している。Sabirnetugは米国食品医薬品局(FDA)より早期AD治療薬としてファスト・トラック指定を受けており、現在、早期AD患者を対象としたフェーズ2試験で評価中である。
About ALTITUDE-AD (Phase 2)
2024年に開始されるALTITUDE-ADは、多施設、無作為化、二重盲検、プラセボ対照の第2相臨床試験であり、早期アルツハイマー病患者を対象に、サビルネツグ(ACU193)を4週間に1回点滴静注し、プラセボと比較して認知機能および機能低下を遅らせる有効性と安全性を評価することを目的としています。本試験には、約540名の早期アルツハイマー病患者(ADによる軽度認知障害または軽度認知症)が登録される予定です。この国際共同試験は現在、米国とカナダの複数の治験施設で登録が行われており、欧州と英国でも追加登録が予定されている。詳細はwww.clinicaltrials.gov(NCT識別子:NCT06335173)に掲載されている。
About INTERCEPT-AD (Phase 1)
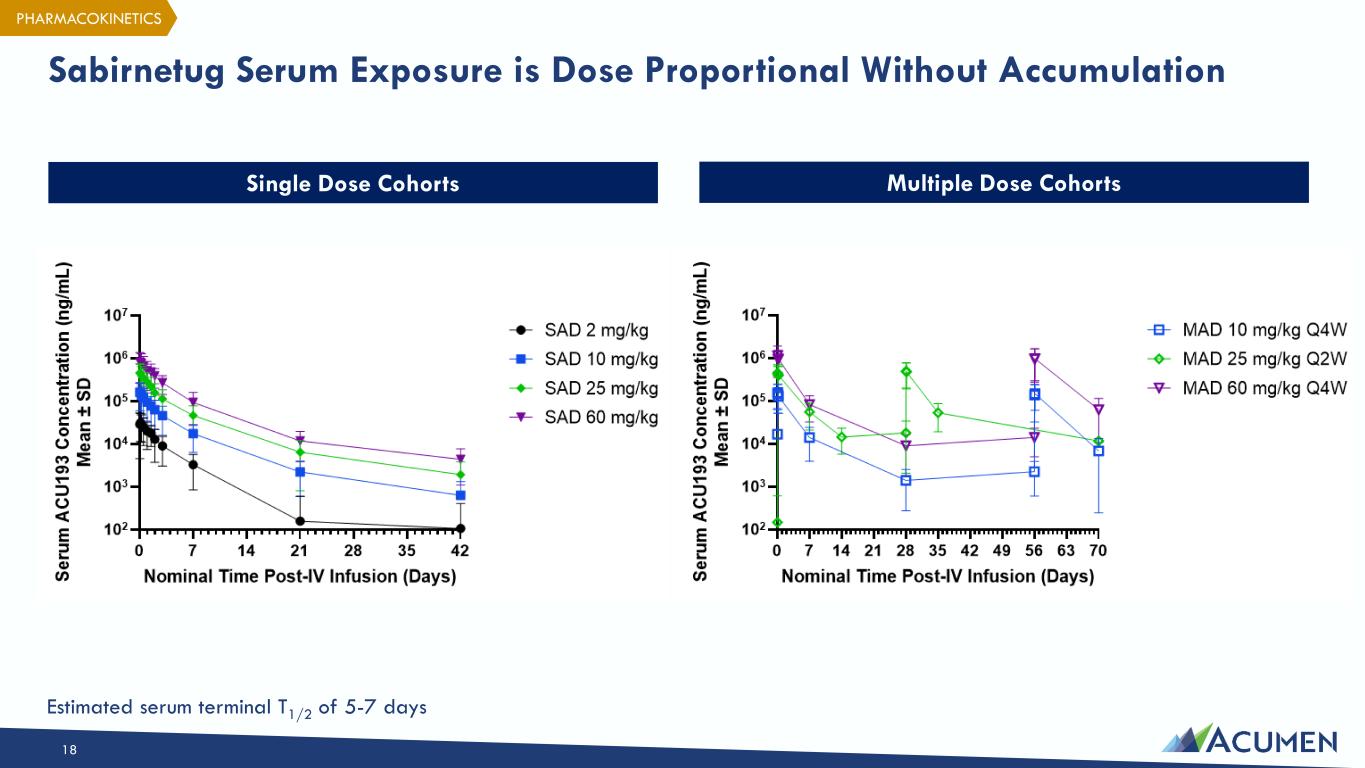
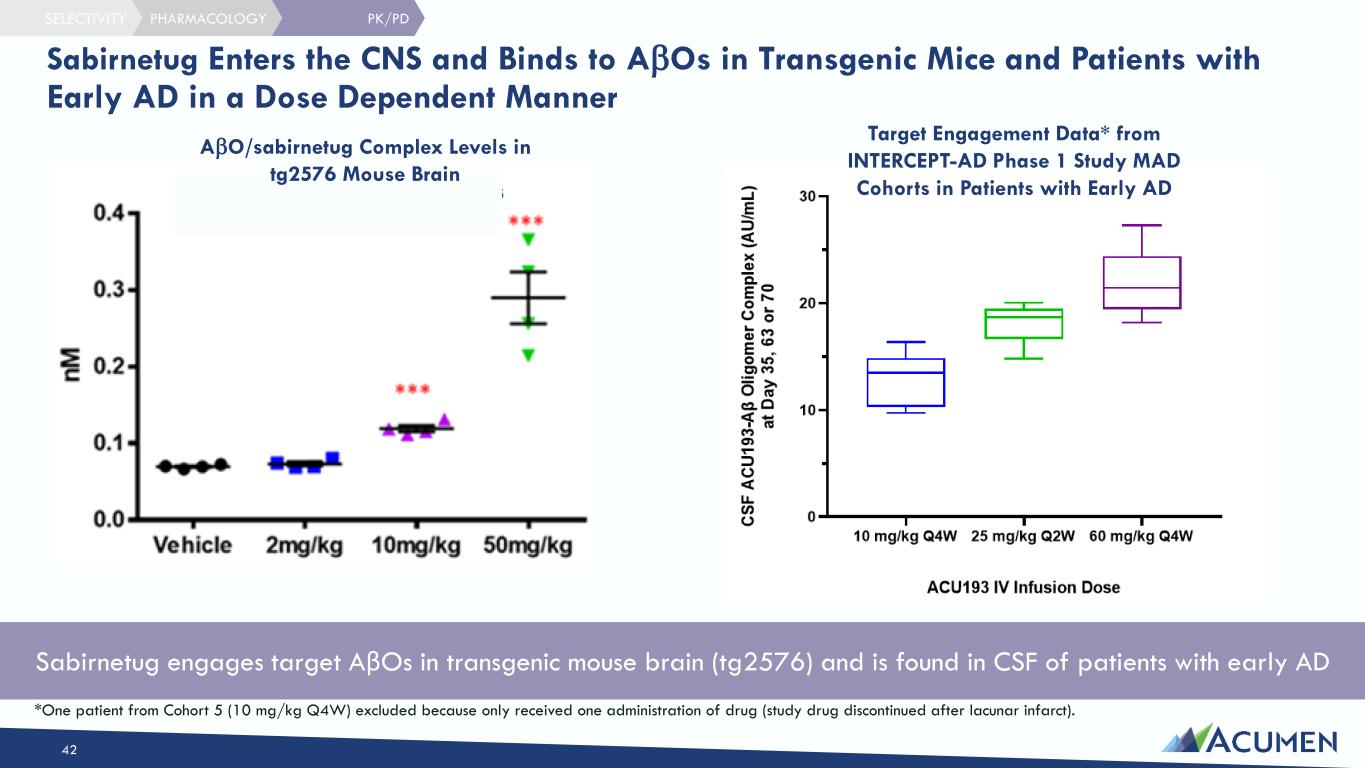
2023年に完了したINTERCEPT-ADは、米国をベースとした第1相多施設共同無作為化二重盲検プラセボ対照臨床試験であり、早期アルツハイマー病(AD)患者を対象にsabirnetugの安全性と忍容性を評価し、メカニズムの臨床的証明を確立した。早期AD(ADによる軽度認知障害または軽度認知症)の65人が、sabirnetugのこの初のヒト試験に登録した。INTERCEPT-AD試験は、単回投与(SAD)と複数回投与(MAD)のコホートから構成された。その結果、sabirnetugは良好な忍容性を示し、全体的な安全性プロファイルも良好であった。本試験では、アミロイドプラークの減少、シナプスバイオマーカーへの効果、ARIA-E発現率の低さ、そして機序の証明を検証する標的関与の証拠が示された。詳細情報はwww.clinicaltrials.gov、NCT識別子NCT04931459に掲載されている。
About Acumen Pharmaceuticals, Inc.
アキュメン・ファーマシューティカルズ社は、アルツハイマー病(AD)の治療薬として、毒性のある可溶性アミロイドβオリゴマー(AβOs)を標的とした新規治療薬を開発する臨床段階のバイオ医薬品企業である。アキュメンの創業者たちは、AβOsに関する研究のパイオニアであり、このAβOsがアルツハイマー病病態の早期かつ持続的な引き金であることを示す証拠が増えてきている。アキュメンは現在、その治験薬候補であり、毒性のある可溶性AβOsを選択的に標的とするヒト化モノクローナル抗体であるサビルネツグ(ACU193)を、その第1相臨床試験INTERCEPT-ADでの良好な結果に続き、現在進行中の早期症状のアルツハイマー病患者を対象とした第2相臨床試験ALTITUDE-AD(NCT06335173)で進めることに注力している。同社はマサチューセッツ州ニュートンに本社を置く。詳細はwww.acumenpharm.com。
Forward-Looking Statements
本プレスリリースには、1995年米国私募証券訴訟改革法(The Private Securities Litigation Reform Act of 1995)の意味における将来の見通しに関する記述が含まれています。Acumenの目標、期待、財務またはその他の予測、意図または信念を記述した声明は、将来の見通しに関する声明であり、リスクのある声明とみなされるべきものです。確信する」、「期待する」、「予想する」、「可能性がある」、「はずである」、「だろう」、「求める」、「目指す」、「計画する」、「可能性」、「予定する」、「マイルストーン」および同様の表現は、将来見通しに関する記述を識別することを意図していますが、すべての将来見通しに関する記述がこれらの識別語を含むわけではありません。将来予想に関する記述には、アキュメンの事業に関する記述、およびアキュメンがその戦略的・財務的目標を達成する能力に関する記述が含まれ、これには、現金、現金同等物、有価証券の使用予測、および2027年前半までの現金資源の充足予測が含まれる、アキュメンの製品候補であるsabirnetug(ACU193)の治療上の可能性(他の抗体に対するものも含む)、ALTITUDE-ADの登録進捗の見込み、sabirnetugの皮下投与オプションを支持するための第1相試験の結果の予定スケジュール。
これらの記述は、アキュメン社の経営陣の現在の信念と期待に基づくものであり、特定の要因、リスク、不確実性、特に安全で効果的なヒト治療薬の発見、開発、商業化の過程に固有の要因の影響を受けます。このようなリスクは、インフレや金利の上昇、供給の混乱、信用・金融市場の不確実性など、地政学的事象やマクロ経済状況の影響によって増幅される可能性があります。アキュメンのプログラムに関するこれらおよびその他のリスクについては、アキュメンの最新の年次報告書(Form 10-K)を含む、証券取引委員会(SEC)への提出書類、およびその後のSECへの提出書類にさらに詳しく記載されています。これらおよびその他の文書のコピーはアキュメンから入手可能である。追加情報は、アキュメンがSECに随時提出するその他の提出書類で入手可能である。これらの将来の見通しに関する記述は、本書の日付時点のものであり、アキュメンは、法律で義務付けられている場合を除き、新たな情報、将来の出来事、またはその他の結果にかかわらず、将来の見通しに関する記述を更新または修正する義務を明示的に否認します。
CONTACTS:
Investors:
Alex Braun
abraun@acumenpharm.com
Media: AcumenPR@westwicke.com
会社開示情報をすべてご覧になるには株探プレミアムの登録が必
会社開示情報をすべてご覧になるには株探プレミアムの
会社開示情報をすべてご覧になるには株探プレミアムの登録が必
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの
会社開示情報をすべてご覧になるには株探プレミアムの登録が必
会社開示情報をすべてご覧になるには株探プレミアムの登録が必
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」
会社開示情報をすべてご覧になるには株探プレミアムの登録が必
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初め









































 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン