米国証券取引委員会
Washington, D.C. 20549
FORM 8-K
現行レポート
第13条または第15条(d)に基づき
1934年証券取引所法
報告日(最も古いイベントの報告日):2023年8月9日
ADAPTIMMUNE THERAPEUTICS PLC
(定款に明記された登録者の正確な名称)
England and Wales |
|
1-37368 |
|
Not Applicable |
(法人設立の州またはその他の管轄区域) |
|
(Commission File Number) |
|
(IRS Employer Identification No.) |
60 ジュビリー・アヴェニュー、ミルトン・パーク
Abingdon, Oxfordshire OX14 4RX
英国
(主たる事務所の所在地(郵便番号を含む)
(44) 1235 430000
(登録者の電話番号(市外局番を含む)
Form8-Kの提出が、以下の条項のいずれかに基づく登録者の提出義務を同時に満たすことを意図している場合は、以下の該当するチェックボックスをチェックしてください:
☐証券法規則425(17 CFR 230.425)に基づく書面によるコミュニケーション
☐取引所法の規則14a-12(17 CFR 240.14a-12)に基づく資料の勧誘
☐取引所法の規則14d-2(b)(17 CFR 240.14d-2(b))に基づく開始前のコミュニケーション
☐取引所法の規則13e-4(c)(17 CFR 240.13e-4(c))に基づく開始前のコミュニケーション
法第12条(b)に従って登録された証券:
Title of each class |
|
Trading Symbol |
|
登録されている各取引所名 |
米国預託株式、1株につき普通株式6株を表章、額面0.001ポンド |
|
ADAP |
|
ナスダック・グローバル・セレクト・マーケット |
登録者が1933年証券法規則405(本章230.405節)または1934年証券取引法規則12b-2(本章240.12b-2節)で定義される新興成長企業であるかどうかをチェックマークで示す。
Emerging growth company ☐
新興成長企業の場合、登録者が取引所法第13条(a)に従い提供される新規または改訂された財務会計基準に準拠するための延長された移行期間を使用しないことを選択した場合は、チェックマークで示す。
項目2.02 営業成績および財務状況。
2023 年 8 月 9 日、Adaptimmune Therapeutics plc(以下「当社」)は、2023 年 6 月 30 日をもって終了した第 2 四半期の業績を発表し、企業最新情報を提供しました。このプレスリリースのコピーは別紙99.1として提出され、参照により本書に組み込まれる。
本Form 8-Kの項目2.02に記載された情報は、本報告書に添付された別紙99.1を含め、1934年証券取引所法(「取引所法」)第18条に照らして「提出」されたものとはみなされず、また、1933年証券取引所法(「改正法」)または取引所法に基づき当社が提出するいかなる提出書類においても、当該提出書類において当社が明示的に具体的な言及を行う場合を除き、参照により組み込まれることはないものとする。
項目9.01 財務諸表および別紙。
(d) 出展物
Exhibit No. |
|
Description of Exhibit |
|
|
|
99.1 |
|
|
|
|
|
104 |
|
カバーページ インタラクティブな日付ファイル(inline xbrlドキュメントに埋め込まれている) |
SIGNATURES
1934年証券取引所法(Securities Exchange Act of 1934)の要件に従い、登録者は本報告書に正式に権限を付与された署名者により、登録者を代表して署名させた。
|
ADAPTIMMUNE THERAPEUTICS PLC |
||
|
|
|
|
Date: August 9, 2023 |
By: |
/s/ Margaret Henry |
|
|
|
Name: |
Margaret Henry |
|
|
Title: |
Corporate Secretary |
Exhibit 99.1

アダプティミューン社、第2四半期決算および事業最新情報を発表
アファミセルのBLAに大幅な進展。FDAは確認エビデンスの計画に合意し、市販のT細胞活性測定法についても好意的なフィードバックを得た。
rete-celのGSK社からの移管、滑膜肉腫とMRCLSを対象としたピボタル試験の完了データは2023年後半に予定
卵巣がんを対象としたフェーズ2試験SURPASS-3を開始。
TCR2社との戦略的合併を完了し、パイプライン、技術、約40名の従業員、8,460万ドルの総流動性1 を有する卓越した細胞治療会社を設立。
今後18ヶ月間のパイプラインデータの読み出しを確認
2026年初頭までのキャッシュ・ランウェイ
ウェブキャストは本日2023年8月9日午前8時(日本時間午後1時)から開催される。
ペンシルベニア州フィラデルフィアおよび英国オックスフォード、2023年8月9日 - がん治療のための細胞治療のリーダーであるアダプティミューン セラピューティクス plc(Nasdaq:ADAP)は本日、2023年6月30日を期末とする第2四半期の業績を報告し、事業の最新情報を提供した。
Adaptimmune の最高経営責任者であるAdrian Rawcliffeは、次のように述べています:「afami-celのBLA申請手続きは、主要なリスク回避項目に関する当局との調整により、順調に進んでいます。現在、固形がんを適応症とする初の遺伝子組換えT細胞療法の承認申請パート3を完成させるため、残りのセクションの執筆と公表に集中しています。TCR2社との統合を完了し、パイプライン資産、技術を追加し、流動性を約8500万ドル増加させました。GSK社からのlete-celの移管も順調に進んでいます。私たちは、がん患者さんに真の変化をもたらすことができると確信できる医薬品を上市するために、データに基づいてポートフォリオを決定する体制を整えました」。
パイプラインの最新情報と、データに基づいた厳密な投資判断のための短期・中期カタリストの概要
Adaptimmune社の主要な臨床フランチャイズは、広範な固形癌に発現するMAGE-A4、NY-ESO(GSKから移行中)、メソセリンを標的とする人工T細胞療法を利用している。これらの細胞療法の使用は、当社の最初のBLA申請の基礎となる後期滑膜肉腫での結果を含む説得力のある臨床データによって裏付けられている。当社は、PRAMEとCD70プログラムを含む「次世代ツールボックス」と前臨床パイプラインを強化している。
次の図は、データ主導の投資判断に使用されるパイプライン・データ触媒の概要を示している。この図の拡大版を見るには、https://images.newsfilecorp.com/files/8845/168338_adptimage.jpg。なお、この図はAdaptimmune社のコーポレートデッキおよびTCR2社との戦略的統合の完了を発表するために6月1日に発表されたプレスリリースで以前に提供されたものである。
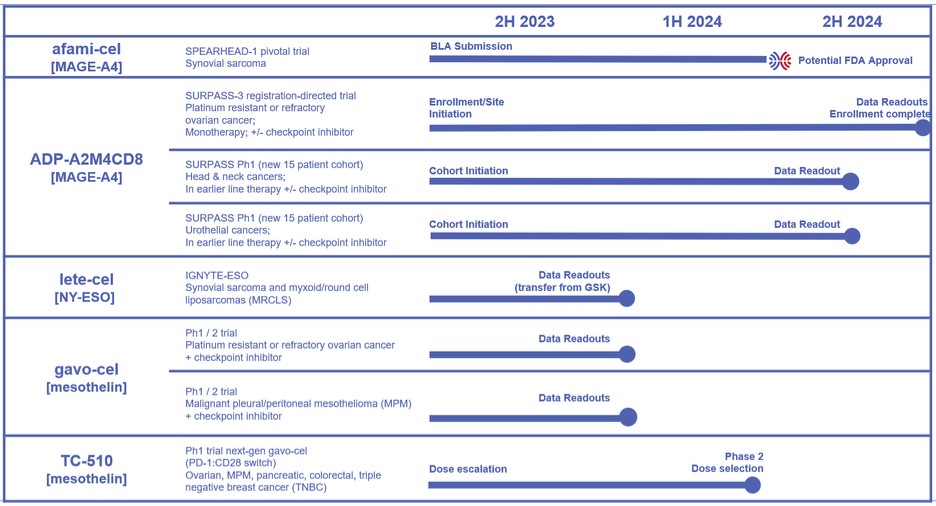

Afami-cel targeting MAGE-A4
| ● | afami-celのBLA申請パート1とパート2は完了し、最終モジュール(パート3)が進行中である。マイルストーンの達成状況は、以下のBLAアップデートのセクションに概説されている。 |
NY-ESOを標的とするLete-cel(GSKから移行中):肉腫患者に対する新たな商業的治療法の可能性がある。
| ● | 滑膜肉腫または粘液様/円形細胞脂肪肉腫(MRCLS)の治療に対するrete-cel(IGNYTE-ESO)の完了した主要臨床試験のデータは2023年後半に期待されている。rete-celのGSKからAdaptimmuneへの移行は進行中であり、2023年第2四半期中に条件が合意された。当社は、BLAの可能性を含め、rete-celの次のステップを2024年初めに決定する予定である。 |
ADP-A2M4CD8:MAGE-A4を標的とする次世代療法
| ● | プラチナ製剤抵抗性卵巣がんを対象としたニボルマブとの併用による第2相SURPASS-3試験を開始。この試験は登録の可能性がある。ADP-A2M4CD8はプラチナ製剤抵抗性卵巣癌の治療薬としてFDAのRMAT指定を受けた。 |
| ● | チェックポイント阻害剤との併用による頭頸部癌および尿路上皮癌の前治療ラインでのフェーズ1試験SURPASSの追加コホートを開始。データ発表は2024年下半期を予定。 |
| ● | 第1相SURPASS試験(ADP-A2M4CD8単独またはニボルマブ併用)の最新情報は、10月23日(月)11:08-11:18(中央ヨーロッパ標準時)に開催される欧州腫瘍学会(ESMO)2023年大会で口頭発表される。 |
Gavo-cel targeting mesothelin
| ● | 卵巣がん患者を対象にニボルマブとの併用でガボセルを評価する第2相試験が進行中である。中間データレビューの対象となる患者はすべて登録されている。登録された全患者は予定通り治療を受け、試験を継続する。データレビューが完了するまで、追加患者の登録は行わない。 |
2
| ● | なお、卵巣がん、非小細胞肺がん(NSCLC)、悪性胸膜/腹膜中皮腫(MPM)、胆管がんを対象とした臨床試験のフェーズ1部分は終了している。フェーズ1試験の初期データは2022年9月に報告された。その後、焦点が卵巣がんに絞られた。 |
| ● | ガボセルの次のステップを決定するため、より成熟した臨床およびトランスレーショナルな第1相および第2相データが今年後半に評価される予定である。 |
TC-510:メソセリンを標的とした次世代治療薬
| ● | MPM、卵巣癌、膵臓癌、大腸癌、トリプルネガティブ乳癌を対象としたTC-510の第1/2相臨床試験は、用量漸増段階で進行中である。TC-510の更なる方向性を決定するため、今年中に初期データの読み出しが予定されている。 |
PRAMEとCD70を標的とした前臨床プログラム(図には示していない)
| ● | Adaptimmune社は、PRAME標的TCR T細胞療法で2023年後半にINDレディになる予定である。PRAMEは、乳がん、腎臓がん、子宮内膜がん、卵巣がん、胃食道がん、非小細胞肺がん、頭頸部がんなどの固形がんとメラノーマを含む広範ながんで高発現している臨床的に検証された標的である。臨床試験は2024年に開始される予定である(適応症は未定)。 |
| ● | CD70のINDは2024年に予定されている。CD70は急性骨髄性白血病(AML)、リンパ腫を含む血液悪性腫瘍、腎細胞癌を含む固形癌で発現している。 |
アファミセルAdaptimmune社は2023年第4四半期にBLA申請を完了する予定
2022年後半、Adaptimmune社はBLAの前臨床モジュール(パート1)の提出を完了した。2023年第1四半期、臨床モジュール(パート2)の提出を完了。現在、最終のCMCモジュール(パート3)を完成させているところである。
最近、いくつかの重要なマイルストーンが完了した:
| ● | 臨床試験供給ベクターと商業供給ベクターで製造されたアファミセル医薬品バッチの比較可能性が実証された。 |
| ● | コンパニオン診断薬(CDx)パートナーと共同で、MAGE-A4 CDxアッセイの市販前申請(PMA)をFDAに提出。 |
| ● | FDAと確認エビデンス計画で合意:SPEARHEAD-1試験のコホート2が完全承認のための確認エビデンスとなる。 |
| ● | ロットリリースアッセイ(力価アッセイを含む)のメソッドバリデーション完了) |
| ● | ベクター・プロセス・パフォーマンス・クオリフィケーション(PPQ)完了) |
| ● | T細胞プロセス性能適格性評価(PPQ)を開始) |
| ● | 市販のT細胞力測定法についてFDAから良好なフィードバックを得た。FDAはBLA申請に先立ち、T細胞力価に関する新たな追加情報を要求していない。 |
このBLAは、主要評価項目である有効性を達成した主要臨床試験SPEARHEAD-1のコホート1のデータによって裏付けられている。当社は、滑膜肉腫を適応症とするafami-celについて、FDAから再生医療先進治療(RMAT)の指定を受けている。
ASCO2023でアファミセルのデータ発表
SPEARHEAD-1のデータは米国臨床腫瘍学会(ASCO)年次総会でポスター発表された。
3
| ● | 極めて重要なSPEARHEAD-1試験のコホート1では、アファミセル単回投与後に約39%の患者に臨床効果が認められ、奏効期間の中央値は約12カ月であった(CTOS 2022年) |
| ● | 全生存期間(mOS)中央値は約17カ月であった。 |
| ● | RECISTで奏効した患者の12ヵ月OS確率は90%、24ヵ月OS確率は70%であり、奏効例のmOSはまだ達成されていない |
| ● | 進行滑膜肉腫の過去の治療成績は悪く、2次治療以降のmOSは12カ月未満であった。 |
Corporate news
| ● | アダプティミューンは6月、TCR2社との戦略的統合の完了を発表し、卓越した細胞治療会社を設立した。統合の完了により、アダプティミューン社の総流動性1が8,460万ドル追加され、39名の従業員が加わった。パイプラインの優先順位付けや投資決定を含む統合作業は現在進行中である。 |
| ● | Adaptimmune社とGSK社は、第2四半期にPRAMEとNY-ESO(rete-cel)標的プログラムをAdaptimmune社に戻す条件で合意した。Adaptimmune社は、第4四半期に予定されている進行中のlete-cel臨床試験の移行に関連して、GSK社から3700万ドル程度を受領する予定である。 |
4
2023年3月期第1四半期および第2四半期決算について
会社開示情報をすべてご覧になるには株探
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無
会社開示情報をすべてご覧になるには株探プ
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が
会社開示情報をすべてご覧になるには株
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プ
5
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日
会社開示情報をすべてご覧になるには株探プレミアムの登録
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報を
会社開示情報をすべてご覧になるに
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日
6
会社開示情報をすべて
会社開示情報をすべてご覧になるには株探プレミア
7
会社開示情報をすべて
会社開示情報をすべてご覧になるには株探プ
8
会社開示情報をすべてご覧になるには
(unaudited, in thousands)
9
会社開示情報をすべてご覧になるには株探プ
会社開示情報をすべてご覧になるには株探
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無
会社開示情報をすべてご覧になるには株探
会社開示情報をすべてご覧になるには株探
会社開示情報をすべてご覧になるには株探プレミアムの登録が
会社開示情報をすべてご覧になるに
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初め
会社開示情報をすべてご覧になるには株探
会社開示情報をすべてご覧になるには株探プレミアムの登録
10
 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン