UNITED STATES
SECURITIES AND EXCHANGE COMMISSION
Washington, D.C. 20549
FORM 8-K
現行レポート
1934年米国証券取引所法第13条または第15条(d)に基づき
報告日(最も古いイベントの報告日):2024年3月18日
ランタン・ファーマ
(定款に明記された登録者の正確な名称)
| デラウェア | 001-39318 | 46-3973463 | ||
|
(State or Other Jurisdiction of Incorporation) |
(Commission File Number) |
(IRS Employer Identification No.) |
|
1920 マッキニー通り7階 Dallas, Texas |
75201 | |
| (主要経営陣の住所) | (Zip Code) |
(972) 277-1136
(登録者の電話番号(市外局番を含む)
フォーム8-Kの提出が、以下のいずれかの規定(以下の一般的説明A.2.を参照)に基づく登録者の提出義務を同時に満たすことを意図している場合は、以下の該当するボックスにチェックしてください:
| ☐ | 証券法に基づく規則425に従った書面によるコミュニケーション(17 cfr 230.425) |
| ☐ | 取引所法の下でのルール14a-12(17 cfr 240.14a-12)に基づく資料の勧誘。) |
| ☐ | 取引所法の規則14d-2(b)に基づく開始前のコミュニケーション(17 cfr 240.14d-2(b)) |
| ☐ | 証券取引法の規則13e-4(c)に基づく開始前のコミュニケーション(17 cfr 240.13e-4(c)) |
法第12条(b)に基づき登録された証券:普通株式
| Title of each class | Trading Symbol | 登録されている各取引所の名称 | ||
| 普通株式、額面0.0001ドル | LTRN | ナスダック株式市場 |
登録者が1933年証券法規則405(本章230.405節)または1934年証券取引法規則12b-2(本章240.12b-2節)で定義される新興成長企業であるかどうかをチェックマークで示す。
Emerging growth company ☒
新興成長企業の場合、登録者が取引所法第13条(a)に従い提供される新規または改訂された財務会計基準に準拠するための延長された移行期間を使用しないことを選択した場合は、チェックマークで示すこと。☒ 2024年3月18日、ランタン・ファーマ・インク(以下「当社」)は、2023年12月31日に終了した会計年度および第4四半期の業績を発表するプレスリリースを発表します。このプレスリリースのコピーは、本フォーム 8-K の別紙 99.1 として提出され、参照することにより本書に組み込まれます。
Item 2.02 営業成績および財務状況
本項目2.02に記載された情報は、別紙99.1を含め、改正1934年証券取引法(以下「取引所法」)第18条において「提出」されたものとはみなされず、また同条の適用を受けるものでもなく、1933年証券取引法(以下「1933年証券取引法」)または同取引所法に基づくいかなる提出書類においても、当該提出書類における一般的な組み込み文言にかかわらず、当該提出書類において明示的に特定の参照により組み込まれない限り、参照により組み込まれたものとはみなされないものとする。
Item 7.01 Regulation FD Disclosure
2024年3月18日、当社は、2023年12月31日に終了する会計年度および第4四半期の財務および営業成績について、当社主催の電話会議およびライブ・ウェビナーにおいて、当社の議論を支援するためのプレゼンテーションを活用する予定です。同プレゼンテーションのコピーは本フォーム8-Kカレント・レポートの別紙99.2として提出され、参照することにより本書に組み込まれる。
本項目7.01に記載された情報は、別紙99.2を含め、改正1934年証券取引法(以下「取引所法」)第18条において「提出」されたものとはみなされず、また同条の適用を受けるものでもなく、1933年証券取引法(以下「1933年証券取引法」)または取引所法に基づく提出書類において、当該提出書類における一般的な組み込み文言にかかわらず、当該提出書類において明示的に特定の参照により組み込まれない限り、参照により組み込まれたものとはみなされないものとします。
Item 9.01 財務諸表および添付資料
(d) 出展物
| Exhibit No. | Exhibit Description | |
| 99.1 | 2024年3月18日付プレスリリース:2023年12月期および2023年12月期四半期決算発表 | |
| 99.2 | 2024年3月18日、2023年12月31日に終了した会計年度および四半期の財務・経営成績に関する電話会議およびライブ・ウェビナーに関するプレゼンテーション。 | |
| 104 | 表紙 インタラクティブ・データ・ファイル(インライン xbrl 形式、別紙 101 に記載)。 |
|
|
SIGNATURES
1934年証券取引法の要件に従い、登録者は本報告書に正式に権限を付与された署名者により、登録者を代表して署名させた。
| Lantern Pharma Inc., | ||
| A Delaware Corporation | ||
| Dated: March 18, 2024 | By: | /s/ David R. Margrave |
| デビッド・r・マーグレイブ 最高財務責任者(cfo | ||
|
|
Exhibit 99.1

ランタンファーマの2023年3月期第4四半期決算と業績ハイライトについて
| ● | LP-184は2024年後半に最初のデータと結果が出る見込みで、3つのAI誘導薬候補について複数の臨床試験が進行中であり、さらに次世代医薬品開発プログラムがIND試験に近づいている。 | |
| ● | 合成致死性薬剤候補であるLP-184とLP-284の両第1相臨床試験において初期患者を投与。 | |
| ● | LP-300 Harmonic™の第2相臨床試験を米国で12施設に拡大し、日本、台湾、韓国での試験開始に向けた最初の規制当局の承認に向けて前進。 | |
| ● | スターライト・セラピューティクス社は最高医学責任者(CMO)を採用し、2024年後半に開始する成人中枢神経系腫瘍を対象としたフェーズ1B/2臨床試験の準備を進める。 | |
| ● | 複数の固形がんモデルにおいて、クリプトフィシンに焦点を当てた抗体薬物複合体プログラム(cpADC)が大きく前進していることを示し、IND試験に先立ち2024年中にさらなる前臨床データを取得する予定。 | |
| ● | がん領域の医薬品開発AIプラットフォーム「RADR®」の2023年目標600億データポイントを超過達成し、2024年目標1000億データポイントを発表、プラットフォーム機能へのジェネレーティブAI機能の統合をさらに進める。 | |
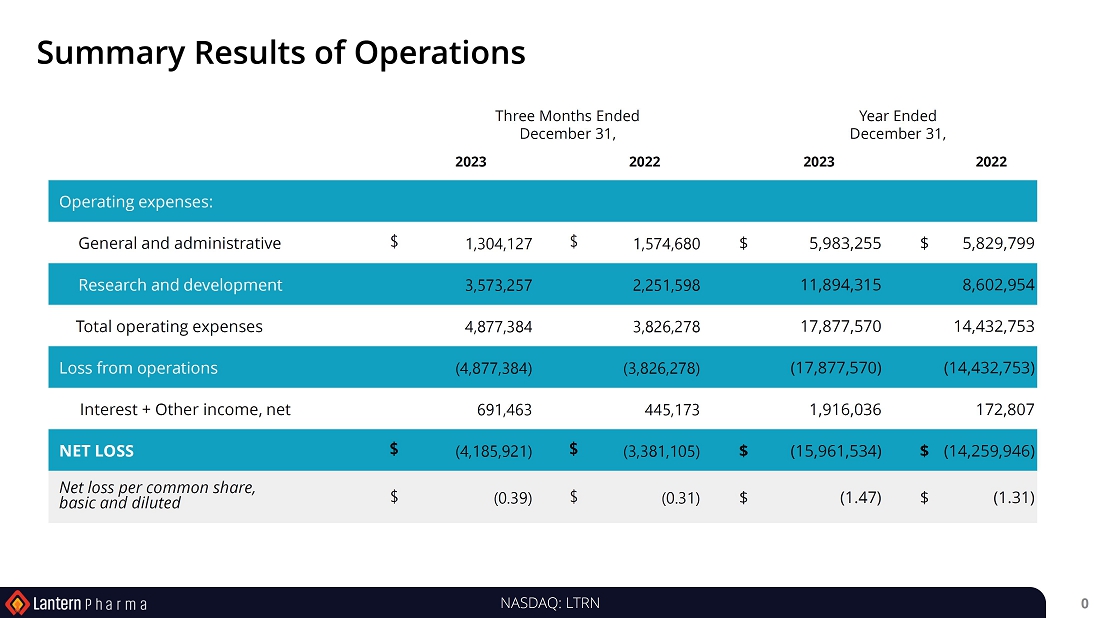
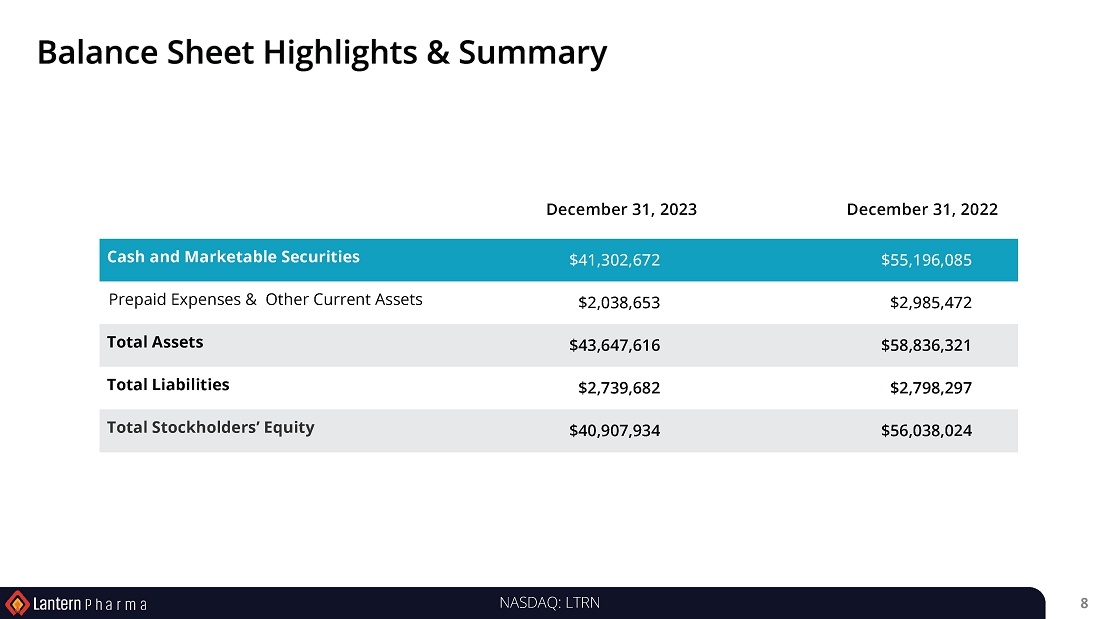
| ● | 2023年12月31日現在の現金、現金同等物および有価証券は約4130万ドル。 | |
| ● | 電話会議とウェブキャストは本日2024年3月18日(月)午後4時30分(東部標準時)/午後1時30分(東部標準時)に予定されている。 |
Monday, March 18, 2024
ダラス-(ビジネスワイヤ)-独自のRADR®AIと機械学習(「ML」)プラットフォームを活用し、複数の臨床段階の新薬プログラムを持ち、標的を絞った画期的ながん治療を開発する人工知能(「AI」)企業であるランタン・ファーマ・インク(NASDAQ: LTRN)は本日、2023年12月31日を期末とする第4四半期および会計年度の業務ハイライトと業績を発表しました。
|
|

「この四半期と2023年全体は、ランタン・ファーマのプログラムとAIプラットフォームにとって有意義で目覚ましい進展の期間でした。私たちのチームは、新たなAI技術、がん生物学モデルと実験、化学、分子、マルチオミクスバイオマーカーデータ、そして大規模な患者データを組み合わせることで、がん領域の医薬品開発におけるタイムラインとコストを変革できることを実証しました。ランタン・ファーマの社長兼最高経営責任者(CEO)であるパナ・シャルマは、次のように述べています。「私たちは2024年に向けて非常に意気込んでおり、LP-184フェーズ1A試験の初期データの可能性、AIから生まれた新会社スターライト・セラピューティクスの前進、中枢神経系癌に特化したADC癌プログラムの進展など、目の前にあるマイルストーンを達成し、場合によってはそれを超えることに積極的に注力していきます。
シャルマは、次のように続けた。「計算とAIを駆使したアプローチは、がん領域の医薬品開発において価値を高める効果を高めており、当社のチームは、当社のプラットフォームの機能と有用性を継続的に高めると同時に、既存の臨床新薬候補のリスク軽減と焦点の絞り込みを支援しています。AIと機械学習を革新的に活用し、高精度がん治療薬の開発コストと開発期間を変革する当社のリーダーシップは、現在進行中の臨床試験において3つの新薬開発プログラムを導いています。業界が成熟し、データとAIを中心とした医薬品開発のアプローチを採用し、受け入れていく中で、当社の集中したチームとリソースによるこの開発ペースは、投資家と患者さんにとって将来的に大きな利益をもたらすはずだと考えています。"
Highlights of AI-Powered Pipeline:
| Ø | LP-284 - 再発性非ホジキンリンパ腫(NHL)およびその他の癌を対象とした初のヒト第 1 相臨床試験を開始。ランタンはまた、LP-284の臨床試験において初回患者が投与されたことを最近発表した。 |
LP-284は、マントル細胞リンパ腫(MCL)、ダブルヒットリンパ腫(DHL)、およびDNA損傷応答欠損を有する他の進行性非ホジキンリンパ腫のサブタイプ(特に、変異または欠失により失調症-脊髄拡張症変異(ATM)遺伝子の機能が低下したもの)を含む、複数の公表されたin vitroおよびin vivo試験においてナノモルの効力を示した。
MCL、DHL、高悪性度B細胞リンパ腫(HGBL)患者のほぼ全員が現在の標準治療薬で再発し、これらの患者に対する新規の改善された治療選択肢に対する緊急かつ満たされていないニーズがある。欧米では、MCL、DHL、HGBLは毎年16,000~20,000人の患者が診断されており、年間市場規模は30億米ドル以上と推定されている。
|
|

| Ø | LP-184 - 現在進行中の第 1 相臨床試験において、複数のコホートの患者への投与が完了した。この試験は、 既存の標準治療薬に抵抗性の進行固形がんを対象とした、ヒト初の第 1 相バスケット試験である。本試験では、膵臓がん、膠芽腫(GBM)、脳転移、肺がん、トリプルネガティブ乳がんなどの再発・難治性の進行固形がんや、DNA損傷応答欠損を有する他の複数の固形がん種の患者を登録している。ランタンは、フォックス・チェイスがんセンター、ジョンズ・ホプキンス・メディシン、その他の主要施設など、増えつつある米国の臨床試験施設において、2024年前半を通じて第1相試験の登録を継続し、夏の終わりから秋の初めにかけて第1相試験の最初の読み出しが行われる可能性があると見込んでいる。 |
フェーズ1A試験で得られた投与量と安全性のデータは、ランタン社の完全子会社であるスターライト・セラピューティクス社がスポンサーとなる将来のフェーズ1b/2試験で中枢神経系(CNS)の適応を進めるために使用されることが期待される。さらに、がん治療で広く使用されているFDA承認薬との併用により、LP-184の奏効持続性および/または全奏効率を改善することを裏付ける薬剤併用試験をさらに改良するため、AIおよび前臨床試験が進行中です。世界的に、LP-184 の標的適応症の年間潜在市場規模は約 120 億ドル以上と推定され、その内訳は、中枢神経系 がんで 45 億ドル以上、固形がんで 75 億ドル以上です。
| Ø | LP-300 - Harmonic™の臨床第2相試験のための12施設が米国で稼動し、アジア3カ国は臨床試験開始のための様々な規制上の許容段階にある。この戦略により、2024年中にHarmonic™の第2相臨床試験で追加患者を投与できる可能性が高まり、Harmonic™が米国で直面している患者登録の課題を解決できるはずです。これらのアジア諸国、日本、韓国、台湾では、NSCLC(非小細胞肺がん)の未喫煙者の罹患率は米国の患者の2倍以上である。ハーモニック試験は、再発NSCLCの非喫煙患者を対象に、LP-300と標準化学療法との併用効果を評価するものである。 |
世界的に、NSCLCの一度も喫煙したことがない患者は増加傾向にあり、PD-1/PD-L1ベースの治療薬にあまり反応しないため、治療の選択肢が減少している。米国では、年間約20,000~40,000人の非喫煙者がNSCLCと診断されており、米国では年間15億ドル、世界では年間26億ドル以上の市場ポテンシャルがあると推定されています。Harmonic™試験に関する追加情報は、Harmonic™ウェブサイトおよびclinicaltrials.govをご覧ください。
|
|

radr®プラットフォームの成長・発展:
| Ø | RADR®は、その規模、範囲、機能において進化を続けており、また、がん領域におけるAI主導の医薬品開発(早期開発、後期段階の患者バイオマーカーおよび併用療法の同定)の標準となることを目指して進んでいます。RADR®は現在、がん領域に特化したデータポイントが600億件を超え、2024年末には1,000億件を超えると予測されています。RADR®のデータ範囲は、新たなクラスの化合物、化学的・生化学的特徴に関する詳細なデータ、薬物相互作用データに戦略的に焦点を当て、拡大しています。さらに、リキッドバイオプシーから得られるような臨床試験からのデータや、薬物相互作用や最適な投与量を定義することを目的とした前臨床併用試験からのデータも、RADR®のデータポイントやデータセットに組み込まれています。 |
ランタンは、RADR®プラットフォームのさらなるデータ増加の取り組みとして、希少がんにおける薬剤感受性データ、併用治療結果データ、バイオマーカーデータ、およびランタンとそのパートナーのための新しい治療法の開発を加速させることを目的とした新たな合成致死性ターゲットに焦点を当てる可能性があります。さらに、RADR®プラットフォームのジェネレーティブAI機能は、分子力学、安全性、薬物-薬物相互作用の理解と予測を向上させるための分子最適化と自動特徴抽出に焦点を当てており、今後数四半期で機能と範囲を拡大する予定です。
Starlight Therapeutics:
| Ø | 2023年第1四半期、ランタンは、薬剤候補lp-184の中枢神経系(cns)および脳腫瘍(gbm、脳転移、いくつかの希少な小児cns癌を含む)の臨床開発のために、完全子会社であるスターライト・セラピューティクス社(以下、「スターライト社」)を設立した。スターライト社は、cnsを適応症として開発されるlp-184分子を「star-001」と呼ぶ。 |
ランタンは最近、スターライトの最高医学責任者を採用し、スターライトの臨床試験、計画された臨床戦略を実行するための人材育成、企業開発活動全般のサポートに専念する。スターライトとランタンは、2024年後半に第1B/2相臨床試験を開始する予定である。スターライト社の合成致死性癌細胞DNA損傷剤-STAR-001の現在計画されている適応症の潜在的市場規模は、成人および小児の原発性および二次性中枢神経系癌全体で45億ドルから50億ドル以上と推定されている。
|
|

ADC Program:
| Ø | ランタンは、学術研究パートナーと共同で、新規で高活性のクリプトフィシンベースのADC(cpADC)の開発、合成、前臨床試験を進めてきた。cpADCは、前臨床開発で試験された広範な固形癌においてピコモル単位の効力を示し、さらに6つの固形癌適応症における臨床的可能性を評価中である。前臨床試験において、cpADCは80%のがん細胞死滅率を示したが、これは他のADC薬剤ペイロードを上回るものであり、これにはアンメットで重要な患者ニーズである中程度のHER-2発現がんも含まれる。 |
ランタンは、がん治療薬開発のための独自のAIプラットフォームであるRADR®を活用し、ADCにおける標的選択と分子ペイロードの特性評価を行い、非特異的なコンジュゲーションを抑制しながら薬剤対抗体の比率を最大化するための独自の制御されたコンジュゲーションアプローチを開発した。ランタンは、2024年中にADCプログラムのIND開発に移行し、現在の治療法に反応しないか難治性の固形がんを選択することを期待している。
Additional Operational Highlights:
| Ø | 2023年第4四半期、ランタンは新たに3件の特許出願を行い、2023年暦年で11件の特許出願となった。 |

会社開示情報をすべてご覧になるには株探プレミアムの
会社開示情報をすべてご覧になるには株
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧にな

会社開示情報をすべてご覧になるには株探プレミ
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施
会社開示情報をすべ
Investor Relations
ir@lanternpharma.com
会社開示情報をすべてご覧になるに

会社開示情報をすべてご覧になるには株探プレミアムの登録が
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会
会社開示情報をすべてご覧になるには株探
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料
会社開示情報をすべてご覧に

















 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン