UNITED STATES
SECURITIES AND EXCHANGE COMMISSION
Washington, D.C. 20549
FORM 8-K
現行レポート
1934年米国証券取引所法第13条または第15条(d)に基づき
報告日(最も古いイベントの報告日):2023年8月9日
ランタン・ファーマ
(定款に明記された登録者の正確な名称)
| デラウェア | 001-39318 | 46-3973463 | ||
|
(State or Other Jurisdiction of Incorporation) |
(Commission File Number) |
(IRS Employer Identification No.) |
|
1920 マッキニー通り7階 Dallas, Texas |
75201 | |
| (主要経営陣の住所) | (Zip Code) |
(972) 277-1136
(登録者の電話番号(市外局番を含む)
フォーム8-Kの提出が、以下のいずれかの規定(以下の一般的説明A.2.を参照)に基づく登録者の提出義務を同時に満たすことを意図している場合は、以下の該当するボックスにチェックしてください:
| ☐ | 証券法に基づく規則425に従った書面によるコミュニケーション(17 cfr 230.425) |
| ☐ | 取引所法の下でのルール14a-12(17 cfr 240.14a-12)に基づく資料の勧誘。) |
| ☐ | 取引所法の規則14d-2(b)に基づく開始前のコミュニケーション(17 cfr 240.14d-2(b)) |
| ☐ | 証券取引法の規則13e-4(c)に基づく開始前のコミュニケーション(17 cfr 240.13e-4(c)) |
法第12条(b)に基づき登録された証券:普通株式
| Title of each class | Trading Symbol | 登録されている各取引所の名称 | ||
| 普通株式、額面0.0001ドル | LTRN | ナスダック株式市場 |
登録者が1933年証券法規則405(本章230.405節)または1934年証券取引法規則12b-2(本章240.12b-2節)で定義される新興成長企業であるかどうかをチェックマークで示す。
Emerging growth company ☒
新興成長企業の場合、登録者が、取引所法第13条(a)に従って提供される新規または改訂された財務会計基準に準拠するための延長された移行期間を使用しないことを選択した場合は、チェックマークで示すこと。2023年8月9日、ランタン・ファーマ・インク(以下「当社」)は、2023年6月30日に終了する第2四半期の決算を発表するプレスリリースを発表します。プレスリリースのコピーは、本フォーム 8-K の別紙 99.1 として提出され、参照することにより本書に組み込まれます。
Item 2.02 営業成績および財務状況
本項目2.02に記載された情報は、別紙99.1を含め、改正1934年証券取引法(以下「取引所法」)第18条において「提出」されたものとはみなされず、また同条の適用を受けるものでもなく、1933年証券取引法(以下「1933年証券取引法」)または同取引所法に基づくいかなる提出書類においても、当該提出書類における一般的な組み込み文言にかかわらず、当該提出書類において明示的に特定の参照により組み込まれない限り、参照により組み込まれたものとはみなされないものとする。
Item 7.01 Regulation FD Disclosure
2023年8月9日、当社は、2023年6月30日に終了した第2四半期の財務および営業成績について、当社主催の電話会議およびライブ・ウェビナーにおいて、当社の議論を支援するためのプレゼンテーションを利用する予定です。同プレゼンテーションのコピーは本フォーム8-Kカレント・レポートの別紙99.2として提出され、参照することにより本書に組み込まれる。
本項目7.01に記載された情報は、別紙99.2を含め、改正1934年証券取引法(以下「取引所法」)第18条において「提出」されたものとはみなされず、また同条の適用を受けるものでもなく、1933年証券取引法(以下「1933年証券取引法」)または取引所法に基づく提出書類において、当該提出書類における一般的な組み込み文言にかかわらず、当該提出書類において明示的に特定の参照により組み込まれない限り、参照により組み込まれたものとはみなされないものとします。
Item 9.01 財務諸表および添付資料
(d) 出展物
| Exhibit No. | Exhibit Description | |
| 99.1 | 2023年8月9日付プレスリリース(2023年6月30日終了四半期決算発表)。 | |
| 99.2 | 2023年8月9日、2023年6月30日に終了した四半期の財務および営業成績に関する電話会議およびライブ・ウェビナーに関するプレゼンテーション。 | |
| 104 | 表紙 インタラクティブ・データ・ファイル(インライン xbrl 形式、別紙 101 に記載)。 |
|
|
SIGNATURES
1934年証券取引法の要件に従い、登録者は本報告書に正式に権限を付与された署名者により、登録者を代表して署名させた。
| Lantern Pharma Inc., | ||
| A Delaware Corporation | ||
| Dated: August 9, 2023 | By: | /s/ David R. Margrave |
| デビッド・r・マーグレイブ 最高財務責任者(cfo | ||
|
|
Exhibit 99.1

ランタン・ファーマ、2023年第2四半期決算と経営ハイライトを発表
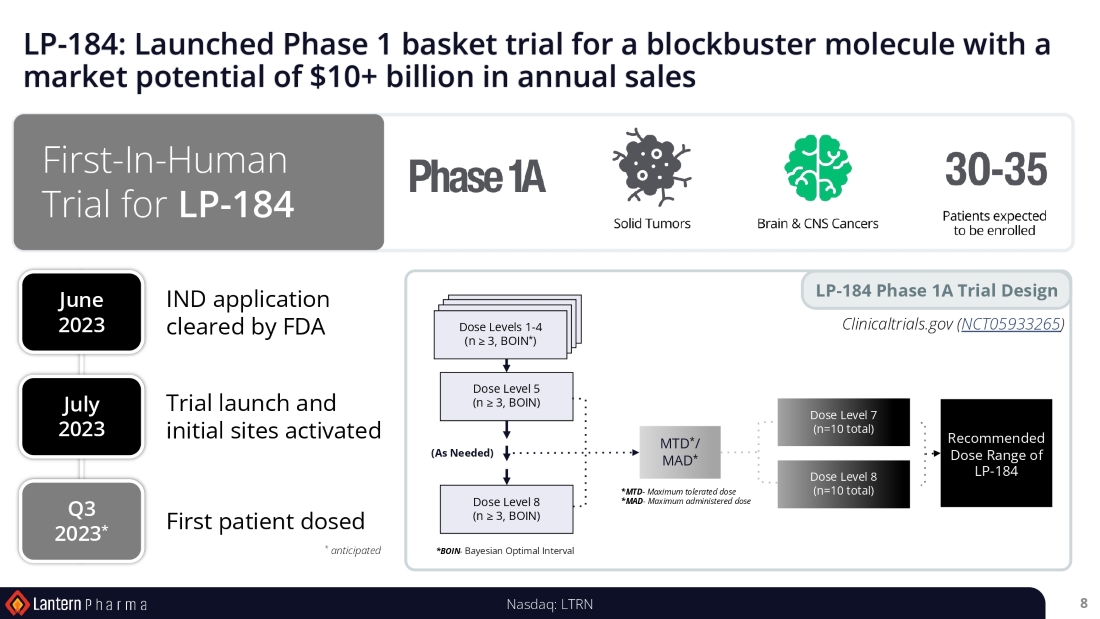
| ● | LP-184のIND申請がFDAより許可され、アンメット・クリニカル・ニーズのある患者集団である再発/難治性の進行性固形がんおよび脳腫瘍を対象とした第1相バスケット試験の初期臨床施設が稼働。 | |
| ● | 進行性非ホジキンリンパ腫を対象とした初のヒト第1相臨床試験を第4四半期に実施予定。 | |
| ● | 肺がん症例全体の15~20%を占める喫煙経験のないNSCLC患者を対象とした臨床第2相試験Harmonic™の初回患者を投与、米国における臨床試験施設の追加拡大を継続し、患者募集活動を強化。 | |
| ● | ビーレフェルト大学とのRADR®共同研究を開始し、より高い精度と有効性を持つ画期的な抗体薬物複合体(ADC)の設計・開発を目指す。 | |
| ● | 米国特許商標庁よりLP-284の物質特許の許可通知を受領。 | |
| ● | 2023年6月30日現在、4,800万ドルの現金、現金同等物および有価証券があり、2025年まで資金を供給できる。 | |
| ● | 電話会議とウェブキャストは本日午後4時30分(東部標準時)/午後1時30分(東部標準時)に予定されている。 |
ダラス-(ビジネスワイヤ)-独自のRADR®AIと機械学習(「ML」)プラットフォームを活用し、複数の臨床段階の新薬プログラムで標的を絞った画期的ながん治療を開発する人工知能(「AI」)企業ランタン・ファーマ・インク(NASDAQ: LTRN)は本日、2023年6月30日に終了した第2四半期の業務ハイライトと財務業績を発表しました。
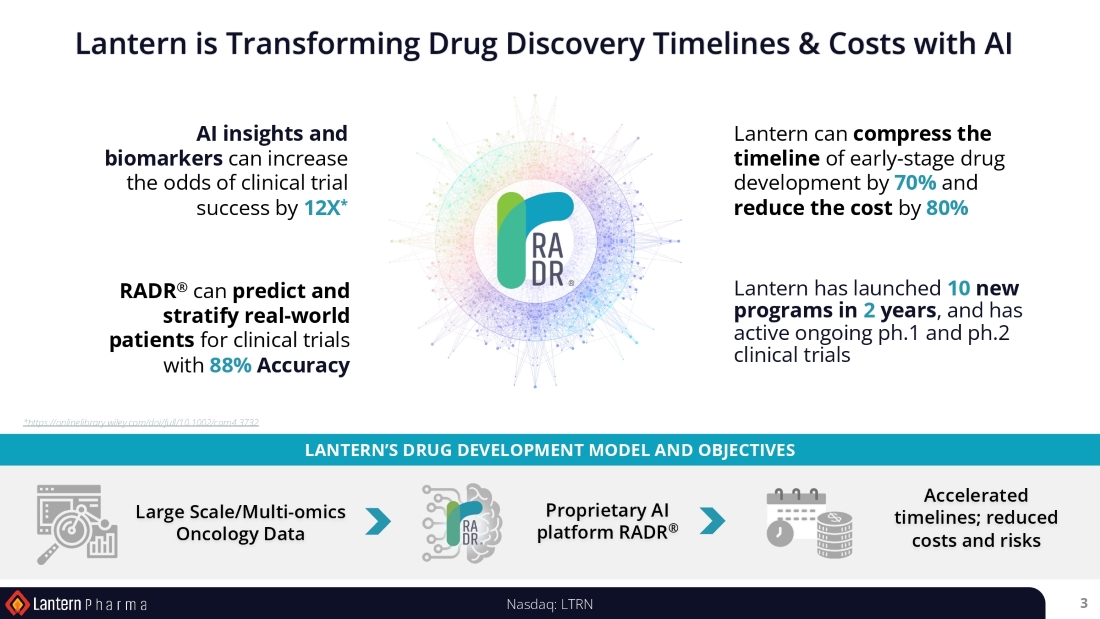
「特に、LP~184 と LP~284 のプログラムを臨床段階に進め、次世代 ADC の開発に重点を置くようになりました。当社の RADR® AI プラットフォームは、薬物と癌の相互作用を理解し予測する方法に革命をもたらし、新たに開発した薬剤プログラ ムを AI による最初の洞察からヒトでの臨床試験まで平均 2 年、1 プログラムあたり約 1~2 百万ドルのコストで進めることを可能にしています。
シャルマは次のように続けた。「コンピューターとAIを駆使したアプローチは、大手製薬会社でも新興製薬会社でも、創薬と開発のあらゆる場面で存在感を増し、利用されるようになっています。AIと機械学習を革新的に活用し、高精度がん治療薬の開発コストと開発期間を変革する当社のリーダーシップは、業界が成熟し、医薬品開発にAI中心のアプローチを採用するにつれて、投資家と患者に大きなリターンをもたらすはずです。当社のトップクラスのAIアルゴリズムは、あらゆる化合物の血液脳関門透過性を89~92%の精度で予測することができます。これは、脳腫瘍や中枢神経系がん、その他の神経疾患に対する治療法の開発スケジュールを加速させる大きなブレークスルーです。また、今期はAACRとASCOの年次総会で画期的なRADR®の進歩を発表し、ユニークな新薬候補を持つバイオファーマとの共同研究において、患者反応を88%の精度で予測できることを実証しました。"
「創薬にAIの力を活用するという当社の揺るぎないコミットメントは、AIを使用して設計・開発された次世代のADCを開発するためのビーレフェルト大学との共同研究の形成にもつながりました。この共同研究は、急成長する新たな治療法において、より高い有効性、より迅速な開発、大幅なコスト削減への道を開く可能性を秘めている。これらの具体的な価値創造の事例と、中枢神経系および脳腫瘍に特化した全く新しい会社であるスターライト・セラピューティクスの開発は、ランタンががん領域の創薬において変革的なアプローチの最前線に立ち続けていることを示しています。
Highlights of AI-Powered Pipeline:
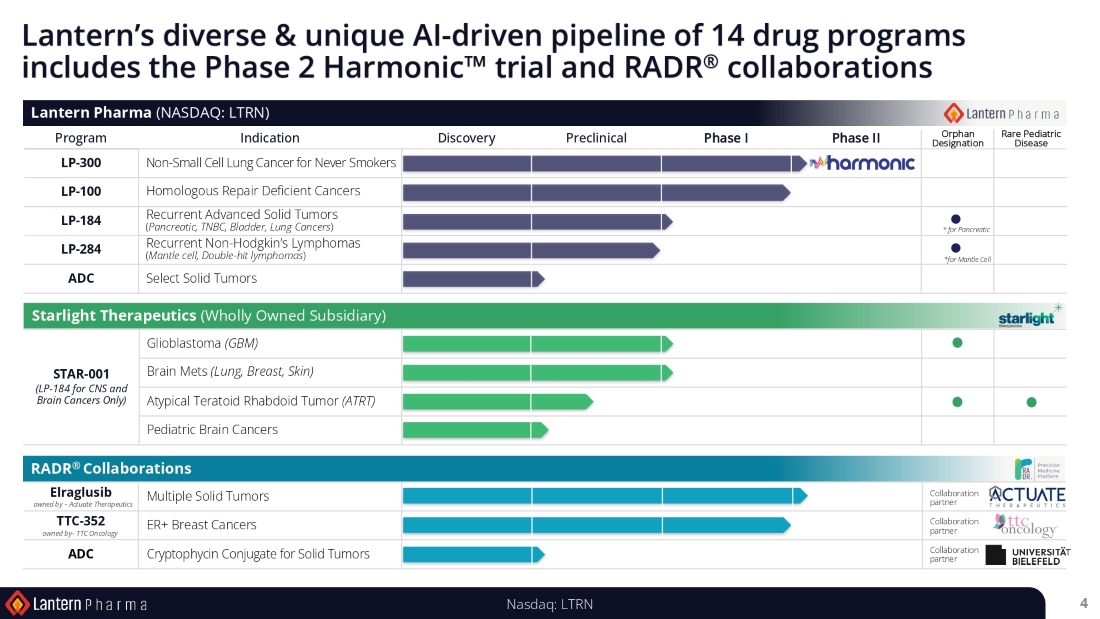
| ● | LP-184-2023年第2四半期中にFDA(米国食品医薬品局)から治験許可申請を受領。LP-184は、ランタンのAIおよびMLプラットフォームであるRADR®の支援により、ランタン社内で完全に開発された最初の医薬品候補であり、ファースト・イン・ヒト第1相バスケット試験に進む。ランタンはLP-184の臨床開発を急速に加速させ、最初の第1相臨床試験2施設を稼動させ、患者のスクリーニングを開始した。本試験の適応症には、再発・難治性の進行膵臓がん、膠芽腫(GBM)、脳転移(脳転移)、DNA損傷応答欠損を有する他の複数の固形がん種が含まれると予想されます。 | |
| 第 1 相試験で得られた投与量と安全性のデータは、ランタン社の完全子会社であるスターライト・セラピュー ティブティクス社がスポンサーとなる将来の第 2 相試験で、中枢神経系(CNS)の適応を進めるために使用されます。世界的には、LP-184 の標的適応症の年間潜在市場規模は、中枢神経系癌で 50 億ドル以上、固形癌で 60 億ドル以上、合計で約 100 億ドル以上と推定されます。 | ||
| ● | LP-284 - LP-284 の治験許可申請は完了し、8 月に FDA に申請する予定です。LP-284は、マントル細胞リンパ腫(MCL)、ダブルヒットリンパ腫(DHL)、その他の進行性非ホジキンリンパ腫(NHL)を含む、複数のin vitroおよびin vivo試験でナノモルの効力を示しています、また、マントル細胞リンパ腫(MCL)、ダブルヒッ トリンパ腫(DHL)、DNA 損傷応答欠損を有する他の進行性非ホジキンリンパ腫(NHL)のサブタイプ、特に、 変異や欠失により失調性-血管拡張症変異(ATM)遺伝子の発現が低下しているものなど、複数の 試験管内および生体内の試験でナノモルの効力を示しています。 | |
| MCL患者のほぼ全員が、現在のMCL標準治療薬で再発するため、これらの患者に対する新規の改善された治療選択肢に対する緊急かつ満たされていないニーズがある。米国と欧州では、MCLとDHLは毎年約9,000人の患者が診断されており、年間12億ドルの潜在市場があると推定されている。 | ||
| ● | LP-300 - 非喫煙者の再発非小細胞肺がん(NSCLC)患者を対象に、LP-300と標準化学療法との併用効果を評価する第 2相ハーモニック™試験の初期患者を投与。投与された患者に加え、20数名の潜在的な患者が事前にスクリーニングされ、米国内の複数の試験施設において登録の可能性を監視されている。当社は、米国内の複数の戦略的施設をさらに活性化させること、NSCLCの未喫煙者の有病率が著しく高いことが知られているアジアの国々へ臨床試験を拡大する可能性があること、臨床開発・運営チームに経験豊富な主要人材を加えることなど、募集を強化するための努力を加速している。 |
Fox Chase Cancer CenterのJoseph Treat医学博士は、Harmonic™試験の主任研究者に任命された。トリート博士は、喫煙歴のない人のNSCLCを含む肺悪性腫瘍の第一人者であり、1991年以来、肺癌患者のためにそのキャリアを捧げてきた。
世界的に、NSCLCの一度も喫煙したことがない患者は増加傾向にあり、PD-1/PD-L1ベースの治療薬にあまり反応しないため、治療の選択肢が減少している。米国では、年間約20,000~40,000人の非喫煙者がNSCLCと診断されており、米国では年間15億ドル、世界では年間25億ドル以上の市場ポテンシャルがあると推定されています。Harmonic™試験に関する追加情報は、Harmonic™ウェブサイトおよびclinicaltrials.govをご覧ください。
radr®プラットフォームの成長・発展:
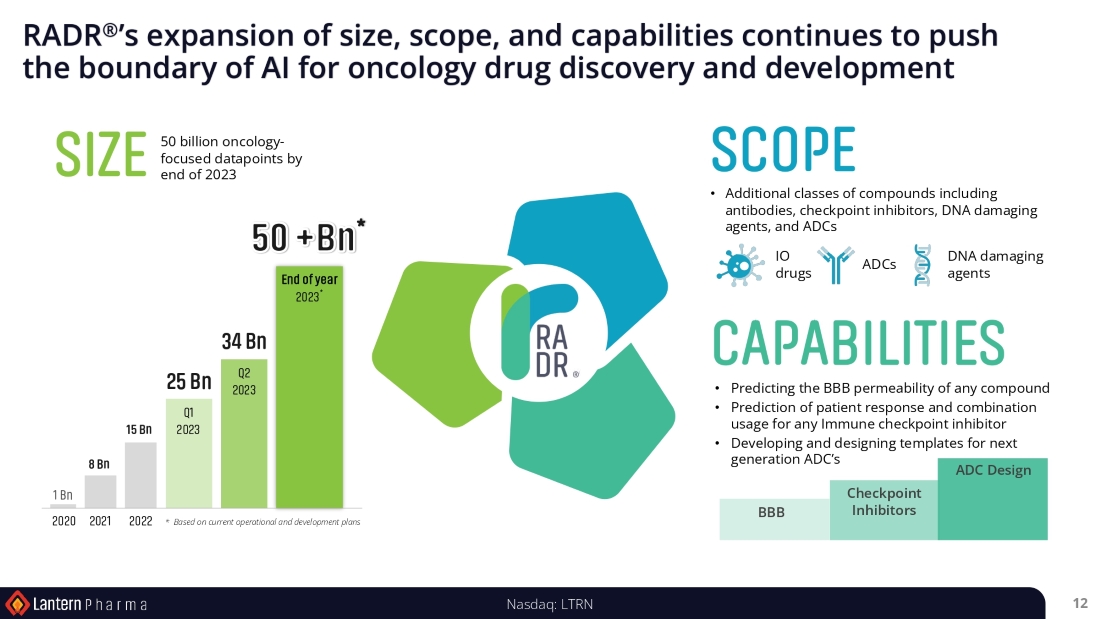
| ● | RADR®は、当社の高精度治療薬のパイプラインを加速させるとともに、がん領域におけるAI主導の医薬品開発の標準となるべく、その規模、範囲、機能を拡大し続けています。RADR®は現在、がん領域に特化したデータポイントが340億件を突破し、2023年末には500億件に達すると予測されています。RADR®のデータ範囲は、抗体、チェックポイント阻害剤、DNA損傷剤を含む化合物の追加クラスに戦略的に焦点を当て、がん診断・治療のためのリキッドバイオプシーとして臨床的に実施されている試験や、薬物相互作用や最適用量を定義することを目的とした前臨床併用試験のデータなど、追加的な試験から得られたデータにより広がっています。 | |
| これらのデータポイントとそれに伴う自動化の進歩により、RADR® の医薬品開発能力は、1) 免疫チェックポイント阻害剤などの免疫腫瘍学(IO)薬の患者反応の予測と最適な併用レジメンの特定、2) BBB透過性の予測、などを含む高度なものとなりました、3)安全性と有効性を向上させる可能性のある次世代抗体薬物複合体(ADC)のための薬物複合体テンプレートの設計と開発の加速。これら3つのモジュールは、RADR®プラットフォームが今後数四半期にわたり、がん治療薬の創製に関連するスピードの向上、コストとリスクの削減を目指し、迅速かつ地に足のついた進歩を遂げることを例証するものです。 | ||
| ● | ランタンは、画期的なADCを開発するため、ビーレフェルト大学との新たな共同研究を開始した。この分野の主要研究者であり、Magicbullet::reloadedコンソーシアムの責任者であるビーレフェルト大学のノルベルト・セワルド教授(Ph.D.)との共同研究は、強力な抗腫瘍分子の有望なグループであるクリプトフィシンに連結した新規ADCの合成と評価に焦点を当てている。現在40億ドル以上と評価されている世界のADC市場は、2027年までに140億ドルに達すると予測されており、ランタンはこの急成長分野の最前線に位置する。 |
Starlight Therapeutics:
| ● | 2023年第1四半期、ランタンは、薬剤候補LP-184の中枢神経系(CNS)および脳腫瘍(GBM、脳転移、いくつかの希少な小児CNS癌を含む)の臨床開発のために、完全子会社であるスターライト・セラピューティクス社(以下、「スターライト社」)を設立した。スターライト社は、CNSを適応症として開発されるLP-184分子を「STAR-001」と呼ぶ。 | |
| ● | 同社は、成人および小児の中枢神経系がんを対象とした今後の臨床試験の実施施設として、中枢神経系に特化したがんセンターの主要な臨床医および主要なオピニオンリーダーと協議を開始した。さらに、スターライト社の科学的/臨床的諮問委員会の設立が進んでおり、第3四半期に発表される予定である。諮問委員会のメンバーは、今後のスターライト社の臨床試験の目的を明確にし、認知度を高めるのに役立つと期待されている。 |
Additional Operational Highlights:
| ● | Oncotarget 誌に掲載された新たな知見により、本薬候補の LP-284 が、MCL および DHL を含む 15 以上の非ホジキンリンパ腫モデルにおいて、in vitro および in vivo で抗腫瘍効果を示すことが実証されました。LP-284 Targets Non-Hodgkin's Lymphoma and DNA Damage Repair Deficiency(LP-284は非ホジキンリンパ腫とDNA損傷修復欠損をターゲットとする)」と題された論文には、LP-284の基本的な知見として、1)MCL異種移植片を移植したマウスにおいて、LP-284は現在のMCL標準治療薬(SOC)であるイブルチニブおよびボルテゾミブを上回るレベルで腫瘍増殖を抑制したこと、2)これらのSOC薬に耐性を示したMCL異種移植片において、その後のLP-284投与により腫瘍がほぼ完全に退縮したこと、が示されています。 | |
| ● | ランタン・ファーマは、米国特許商標庁(USPTO)より、LP-284分子を対象とする物質特許(特許番号17/192,838)について、新規分子体を対象とするクレームを含む特許査定通知を受領しました。ランタン・ファーマは、LP-284の特許がオレンジブックに登録され、2039年初頭に満了すると予想しています。 | |
| さらに、当四半期中にLP-184およびLP-284について5件の特許が新たに出願され、特定の腫瘍サブタイプに対する併用レジメンでのこれらの薬剤候補の使用をカバーするクレームが記載されました。 | ||
| ● | 今後開催される複数の科学会議で新データと研究結果が発表される予定: |
| ● | 2023年8月10日午後5時30分~7時30分(太平洋標準時)、カリフォルニア州サンフランシスコで開催される神経腫瘍学会/米国臨床腫瘍学会中枢神経系癌会議(Society of Neuro-Oncology/American Society of Clinical Oncology CNS Cancer Conference)。学会登録へのリンクはこちら。 | |
| 発表タイトル新規アシルフルベン由来腫瘍部位活性化低分子LP-184は成人および小児の中枢神経系腫瘍細胞の増殖を阻害する | ||
| ● | 2023年8月24日(木)9:45-10:15(中央ヨーロッパ標準時)、ドイツのダルムシュタットで開催される「Drug Conjugates for Directed Therapy」に関する国際会議。会議参加登録へのリンクはこちら。 | |
| 発表タイトル腫瘍選択性を改善したADC標的同定のためのインシリコアプローチ | ||
| ● | 血液腫瘍学会年次総会(テキサス州ヒューストン)2023年9月6日(水)18:00p.m. CT.学会登録へのリンクはこちら。 | |
| 発表タイトル新規抗腫瘍低分子LP-284によるB細胞非ホジキンリンパ腫の相同組換え欠損の標的化 |
2023年第2四半期 財務概要:
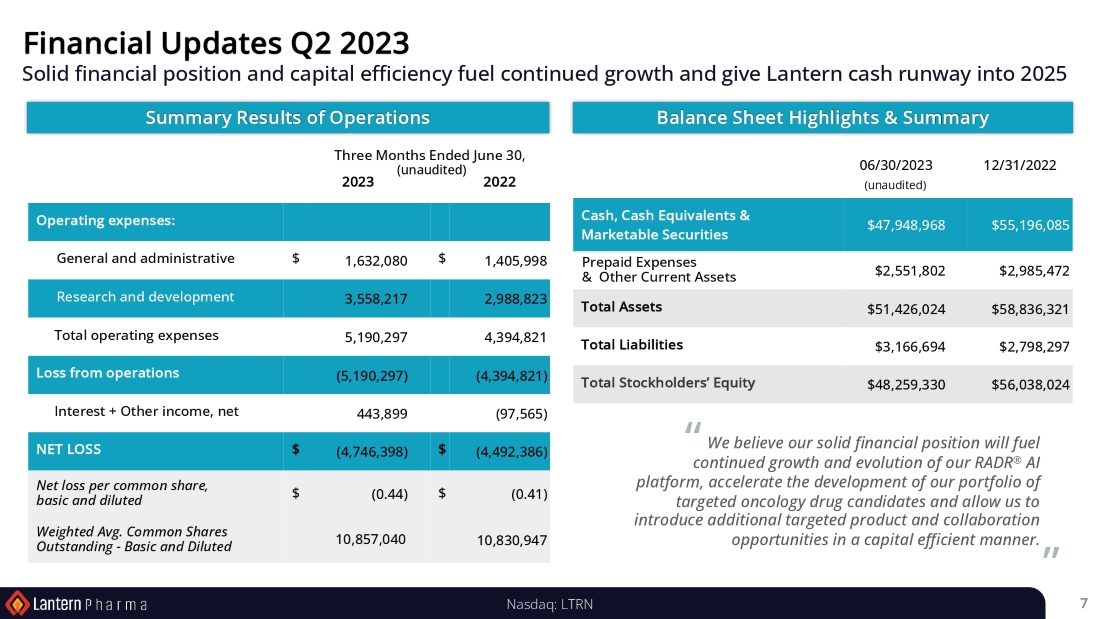
| ● | 貸借対照表:現金、現金同等物および有価証券は、2022年12月31日時点の約5,520万ドルに対し、2023年6月30日時点では約4,800万ドルとなっている。四半期ごとの現金消費率は、引き続き資本効率の高い、共同研究者中心のビジネスモデルを反映している。 | |
| ● | 研究開発費:研究開発費は、2022年6月30日に終了した四半期が約300万ドルであったのに対し、2023年6月30日に終了した四半期は約360万ドルであった。 | |
| ● | 一般管理費:一般管理費は、2022年6月30日に終了した四半期が約140万ドルであったのに対し、2023年6月30日に終了した四半期は約160万ドルであった。 | |
| ● | 純損失:2023年6月30日に終了した四半期の純損失は約470万ドル(1株当たり0.44ドル)であったのに対し、2022年6月30日に終了した四半期の純損失は約450万ドル(1株当たり0.41ドル)であった。 |
決算説明会およびウェビナーの詳細:
ランタンは本日8月9日(水)午後4時30分(米国東部時間)より、2023年第2四半期決算説明会およびウェビナーを開催する。
| ● | https://us06web.zoom.us/webinar/register/1016902973506/WN_h4QZ0ZyxR3mZZbNQxa2eMw | |
| ● | 関連するプレゼンテーション資料は、https://ir.lanternpharma.com からアクセスできます。 | |
| ● | 第2四半期決算説明会およびウェビナーのリプレイはhttps://ir.lanternpharma.com。 |
About Lantern Pharma:
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミ
会社開示情報をすべ
Nicole Leber
Investor Relations Associate
ir@lanternpharma.com
会社開示情報をすべてご覧になるに
Website: www.lanternpharma.com
LinkedIn: https://www.linkedin.com/company/lanternpharma/
X/Twitter: @lanternpharma
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中
会社開示情報をすべてご覧になるには株探プレミアムの登録が
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」
会社開示情報をすべてご覧になるには株探
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料
会社開示情報をすべてご覧に










 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン