UNITED STATES
SECURITIES AND EXCHANGE COMMISSION
Washington, D.C. 20549
FORM 8-K
現行レポート
第13条または第15条(d)に基づき
1934年証券取引所法
報告日(最も早く報告された事象の日付):2023年5月10日
マティナス・バイオファーマ・ホールディングス(株)
(チャーターで指定された登録者の正確な名前)
| デラウェア | 001-38022 | 46-3011414 | ||
|
(State or other jurisdiction of incorporation) |
(Commission File Number) |
(IRS Employer ID Number) |
|
1545 ルート206サウス、スイート302 Bedminster, New Jersey |
07921 | |
| (主要経営陣の住所) | (Zip Code) |
登録者の電話番号(市外局番を含む):(908) 484-8805
Not Applicable
(旧姓または旧住所(前回の報告書から変更された場合)。)
Form 8-Kの提出が、以下のいずれかの規定に基づく登録者の提出義務を同時に満たすことを意図している場合は、以下の該当するボックスにチェックします(以下の一般教示A.2.を参照してください):
| ☐ | 証券法に基づく規則425に従った書面によるコミュニケーション(17 cfr 230.425) |
| ☐ | 取引所法の下でのルール14a-12(17 cfr 240.14a-12)に基づく資料の勧誘。) |
| ☐ | 取引所法の規則14d-2(b)に基づく開始前のコミュニケーション(17 cfr 240.14d-2(b)) |
| ☐ | 証券取引法の規則13e-4(c)に基づく開始前のコミュニケーション(17 cfr 240.13e-4(c)) |
法第12条(b)に基づき登録された証券:
| Title of Each Class | Trading Symbol | 登録されている各取引所の名称 | ||
| 普通株式 | MTNB | NYSE American |
登録者が1933年証券法の規則405(17 CFR §230.405)または1934年証券取引法の規則12b-2(17 CFR §240.12b-2)に定義される新興成長企業であるかどうかをチェックマークで示す。
Emerging growth company ☐
新興成長企業の場合、登録者が取引所法第13条(a)に従って提供される新規または改訂された財務会計基準への準拠のための延長移行期間を使用しないことを選択した場合、チェックマークで示すこと。☐
Item 2.02. 営業成績および財務状況
2023年5月10日、Matinas BioPharma Holdings, Inc.(以下「当社」)は、2023年3月31日に終了した四半期の決算を発表するプレスリリースを発表しました。プレスリリースの全文は、本書の別紙99.1として提出され、参照することにより本書に組み込まれています。
本Current Report on Form 8-Kの項目2.02および添付の別紙99.1の情報は、1934年証券取引法改正(以下「取引所法」)第18条にいう「提出」、または同条の義務の対象とはみなされず、1933年証券法改正(以下「証券法」)または取引所に基づくいかなる提出においても、当該提出において特定の参照により明確に規定されるものを除き、参照により組み込まれるとみなされることはないものとします。
Item 7.01 Regulation FD Disclosure
2023年5月10日、当社は、特に当社の戦略的イニシアティブ及びプログラムの一部に関する最新情報を発表するプレスリリースを発表しました。このプレスリリースの全文は別紙99.1として提供され、参照することにより本書に組み込まれます。
当社は、様々な会議や投資家向け会合で使用する予定のコーポレート・プレゼンテーション(以下「コーポレート・ プレゼンテーション」)を更新しました。コーポレート・プレゼンテーションは別紙99.2として添付され、参照することにより本書に組み込まれます。
本項目7.01および添付の別紙99.1および99.2の情報は、1934年証券取引法改正法(以下「取引所法」)第18条にいう「提出」、または同条の義務の対象となるものとはみなされず、1933年証券法改正法または取引所に基づく提出書類に参照により組み込まれるものとは、当該提出書類に特定の参照により明確に記載されているものを除き、みなされないものとします。
Item 8.01. Other Events
2023年5月10日、当社は、以下のような一部のプログラム及びイニシアティブに関する最新情報を発表しました:
| ● | 当社は、2023年第2四半期中にBiomedical Advanced Research and Development AuthorityおよびNational Institutes of Healthに対するAdvanced Research Project Agency for Healthを通じた資金調達提案の提出を完了する予定である。; |
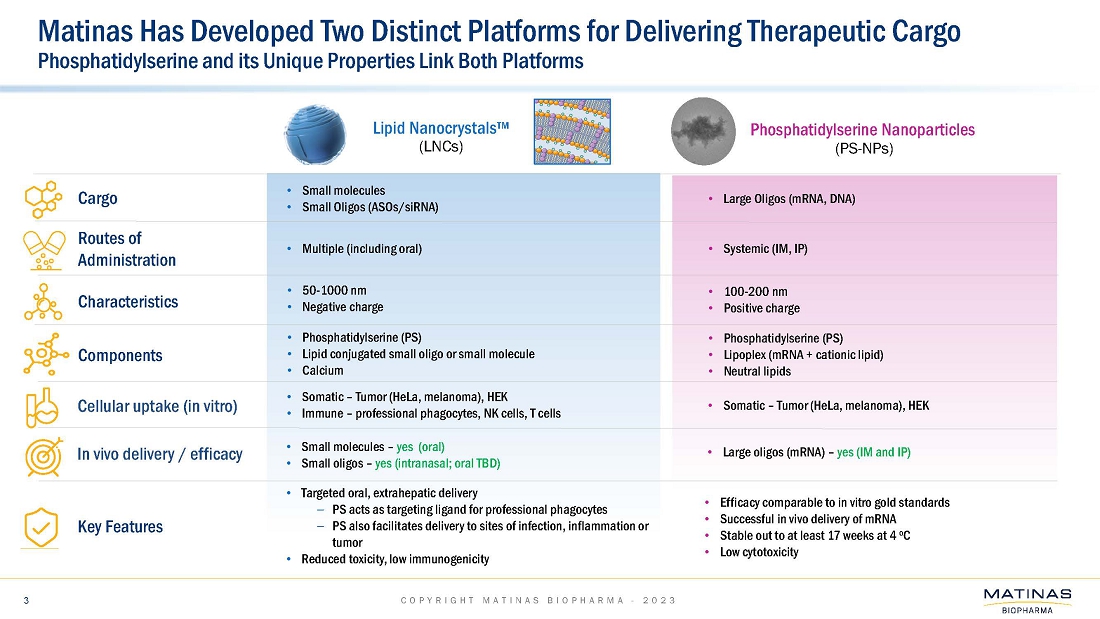
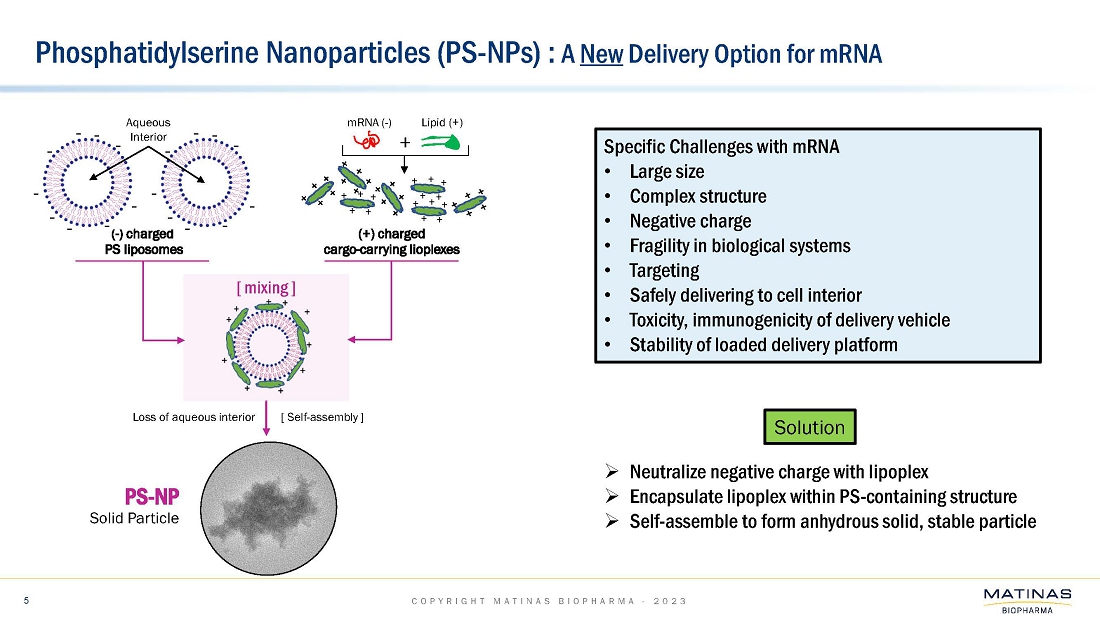
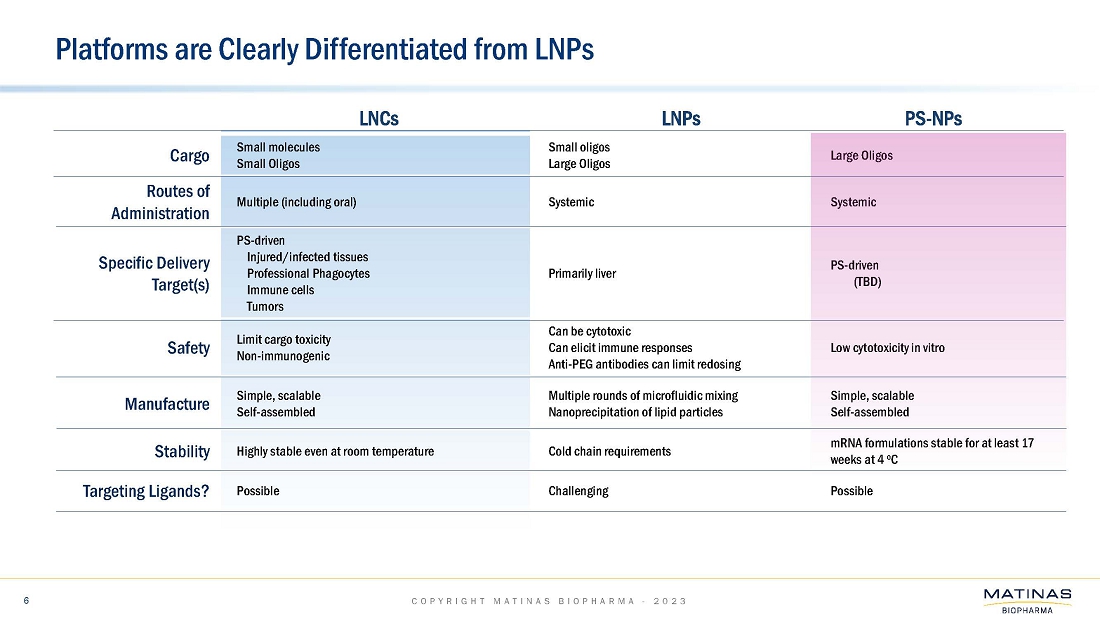
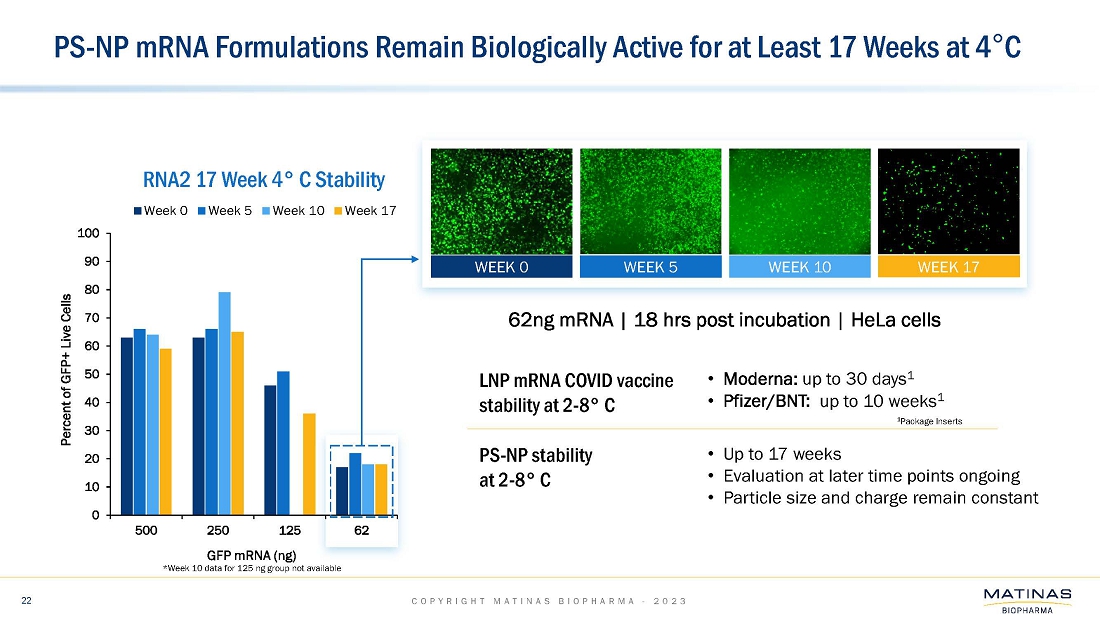
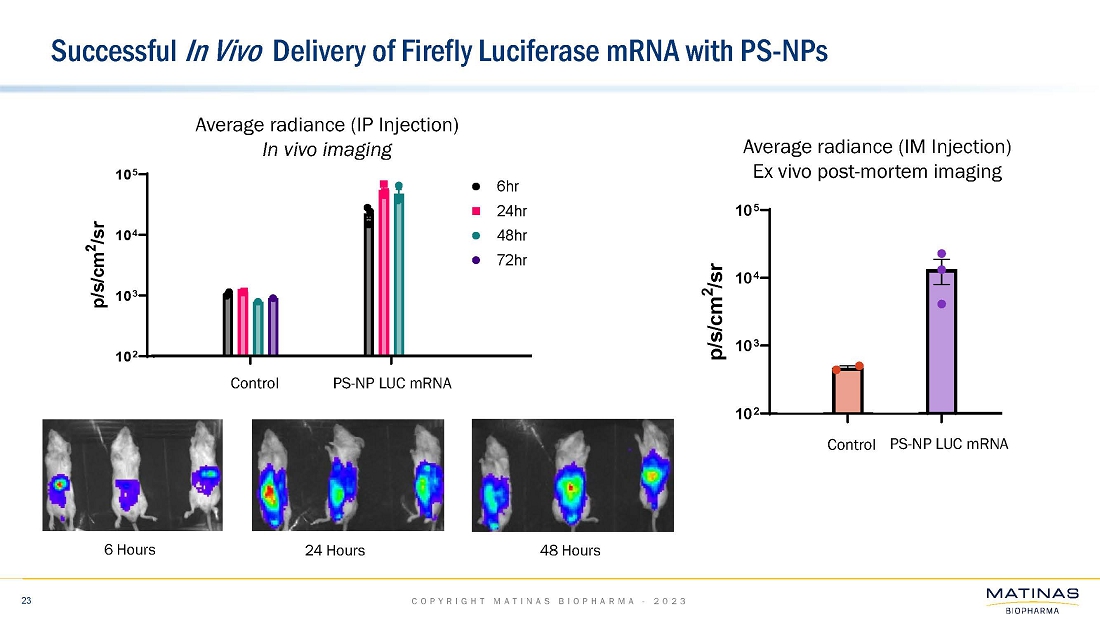
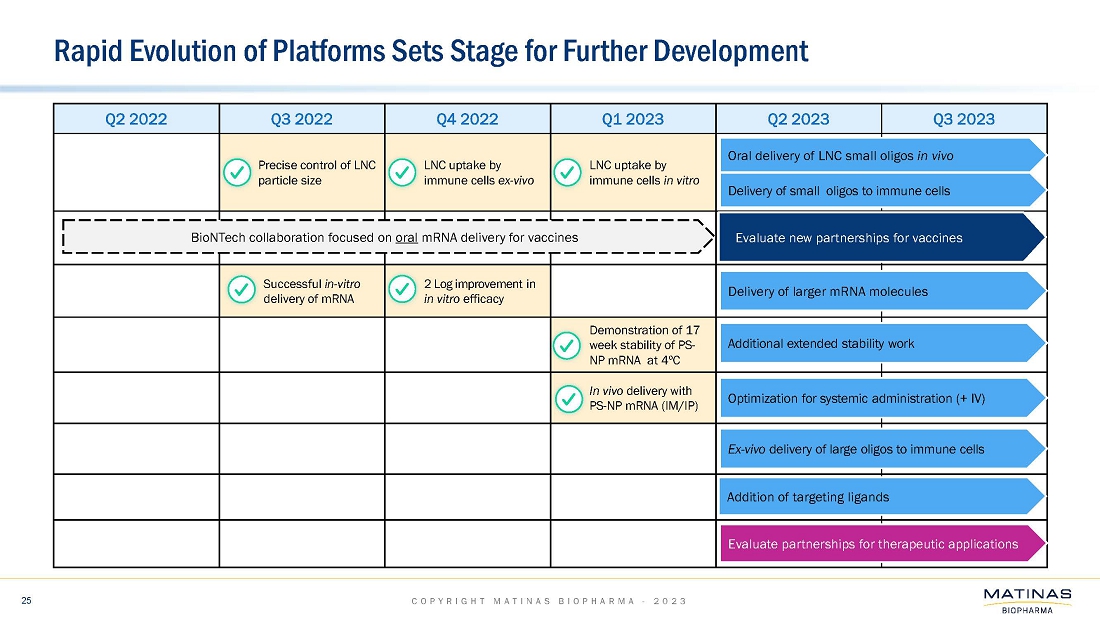
| ● | BioNTech SE社と共同で実施した経口mRNAデリバリーの最初のin vivo試験では、経口前臨床活性を示すことはできませんでした。この製剤は、健康なマウスを用いたin vivo試験に進む前に、複数の細胞株においてin vitroでmRNAを送達することに成功していました。同様の非脂質ナノ結晶(「LNC」)mRNA製剤の追加の社内in vivo試験では、全身投与(筋肉内および腹腔内)により活性が示されました。また、これらの製剤は、脂質ナノ粒子(LNP)と比較して、4℃で少なくとも17週間という高い安定性を示しています。MatinasとBioNTech SAとの共同研究は終了しました。; |
| - |
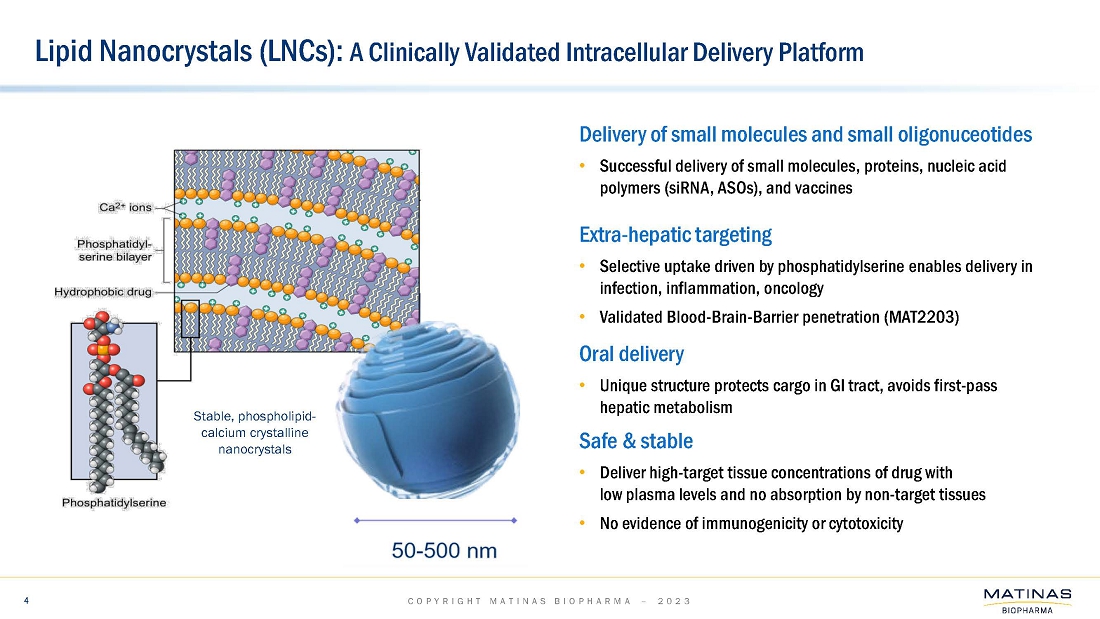
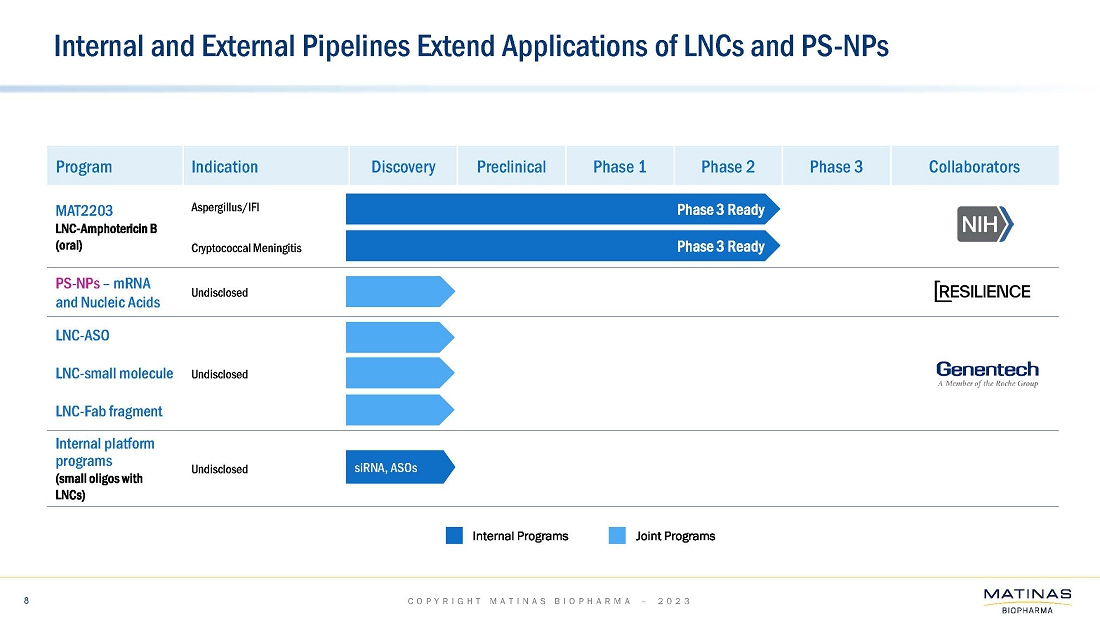
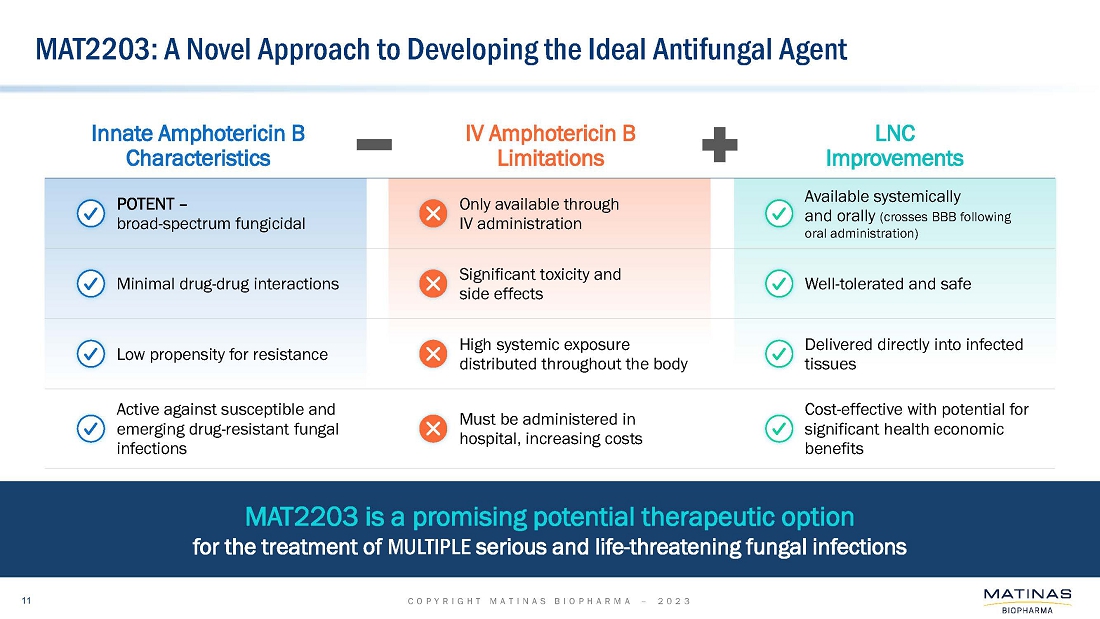
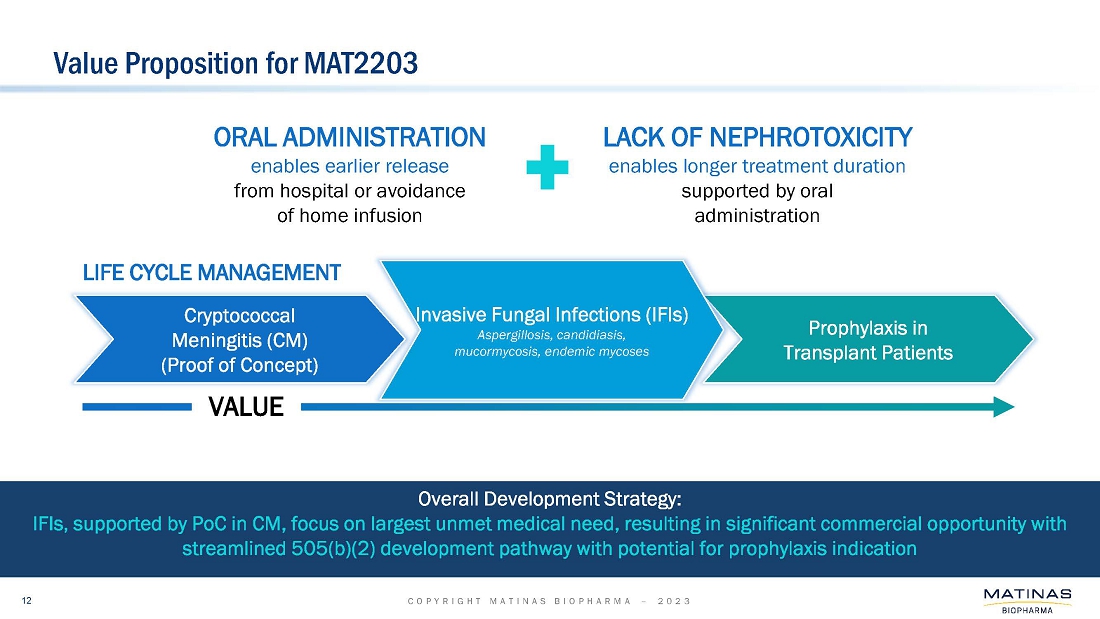
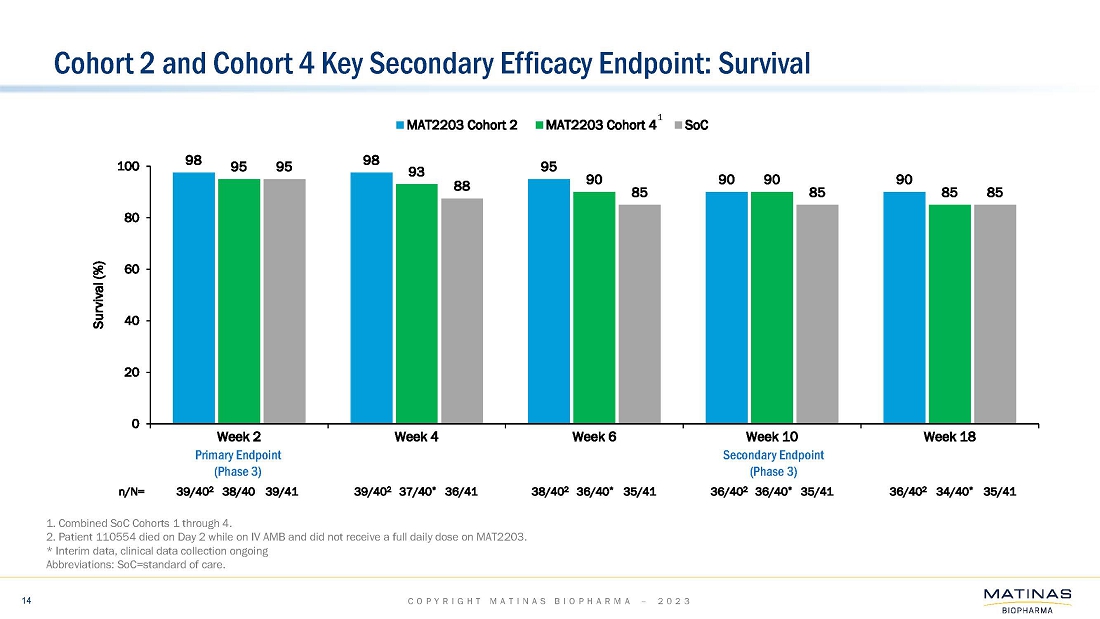
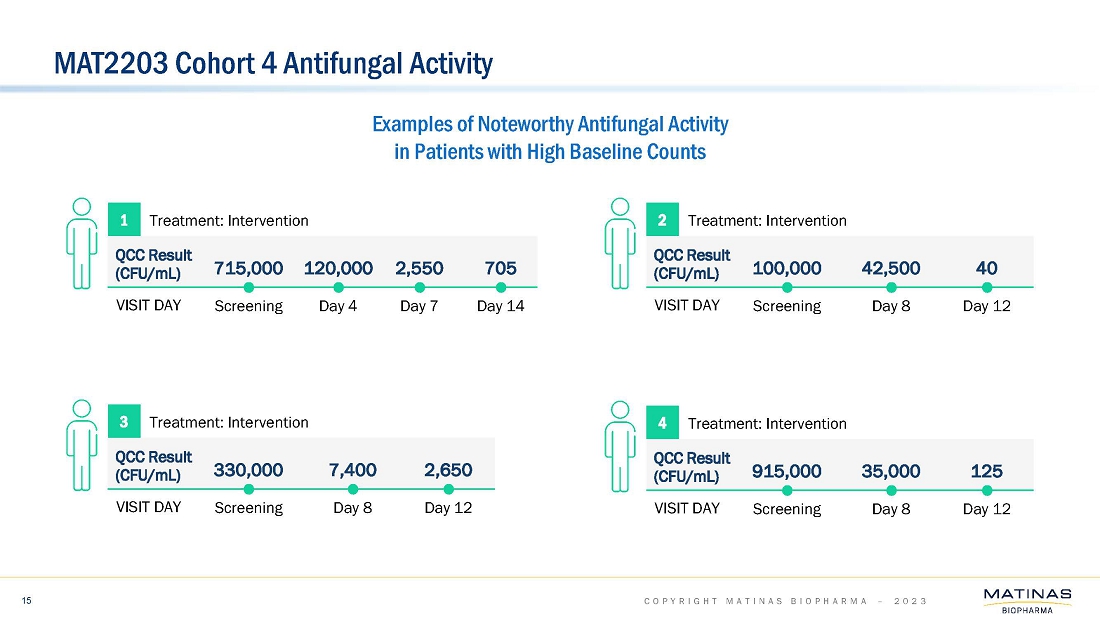
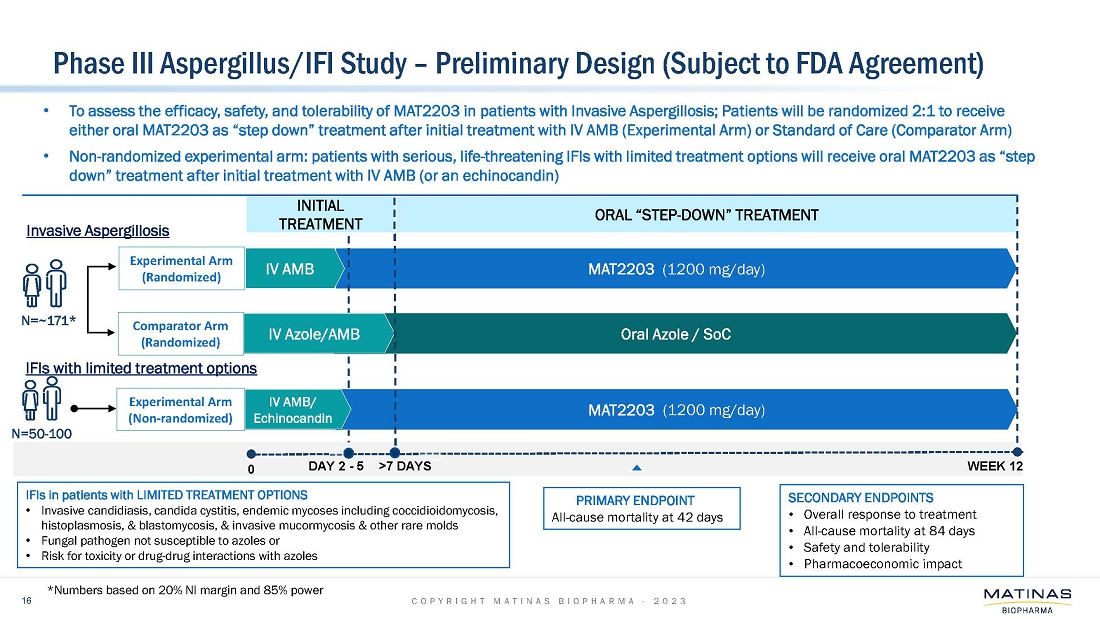
| ● | 当社は、治療選択肢が限られている患者さんを含む、生命を脅かす重篤な侵襲性真菌感染症(以下、IFI)患者さんを対象に、MAT2203製品候補の安全性、有効性、忍容性を評価するための改訂フェーズ3試験のデザインを2023年の第2四半期に提出する予定です。本試験の主要コホートは、アスペルギルス症患者を対象とし、標準治療のアゾール系抗真菌薬静注療法患者との非劣性比較としてデザインされる予定です。このメインコホートには、ファーストラインとセカンドラインの両方が含まれると予想され、そのデザインには、MAT2203の単剤投与による経口治療への早期ステップダウンが含まれると思われます。また、本試験では、アゾール系薬剤の経口投与に移行できない、治療選択肢が限られている様々なIFIの患者さんを対象とした非盲検コホートも追加される可能性があります。この非盲検コホート試験は、505(b)(2)の規制パスウェイに基づき、アスペルギルス症以外にも、侵襲性粘菌症、その他のまれなカビ感染症、侵襲性カンジダ症、カンジダ膀胱炎、コクシジオイドミカ症、ヒストプラズマ症、ブラストミカ症などの固有菌症を含む患者を対象にラベル拡大する予定であると予想される。; |
| ● | 米国食品医薬品局からの最新のフィードバックに基づき、当社は、クリプトコッカス髄膜炎(以下、「CM」)を対象としたMAT2203の以前に計画されていたフェーズ3試験を再検討しています。当社は、CMを対象としたより小規模で集中的な試験により、CMの治療に関する追加適応の規制要件を満たすことができると考えています。; |
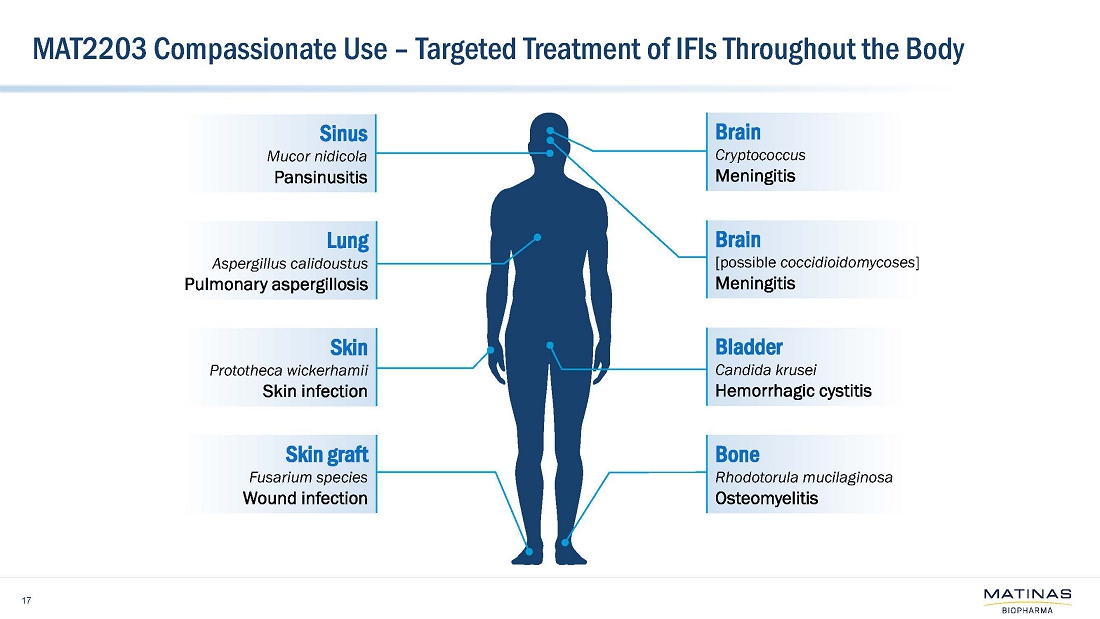
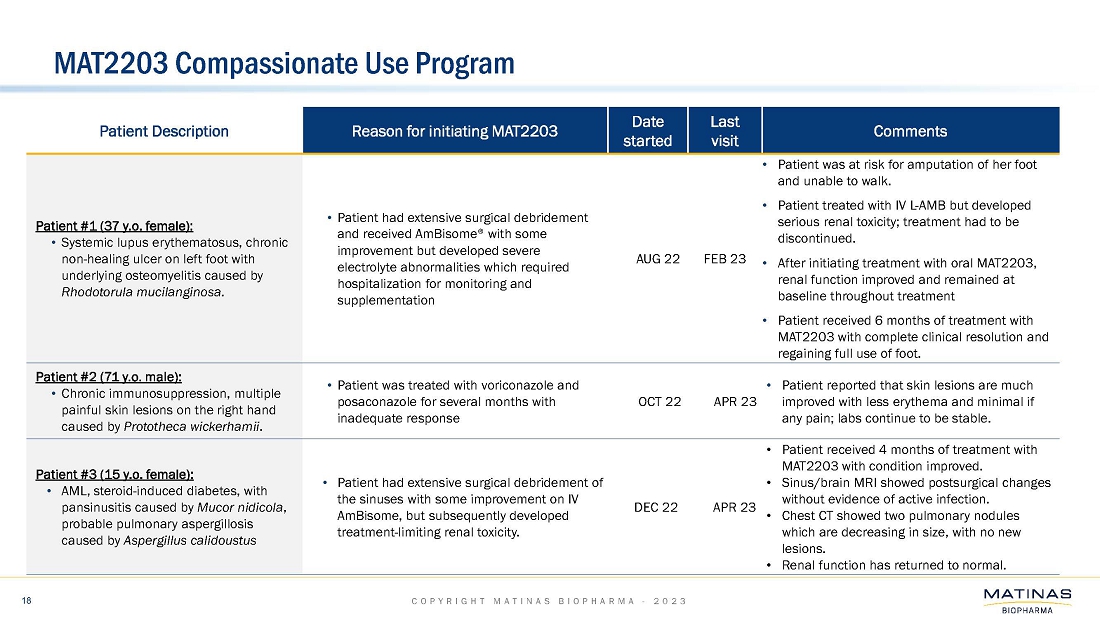
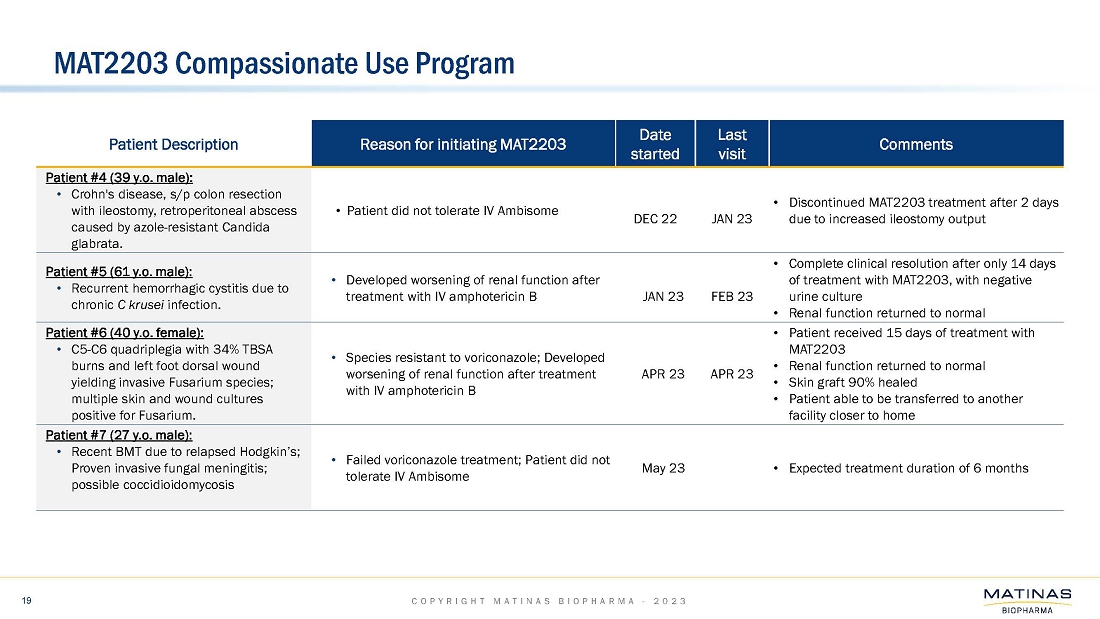
| ● | これまでに、当社のコンパッショネートユースプログラムのもと、さまざまなIFIの患者さん7名にMAT2203が投与されました。これらの限られた症例における臨床データは、経口投与されたMAT2203が標的であり、安全で、最も困難な症例のIFIを効果的に根絶することを示しました。コンパッショネートユースプログラムでは、MAT2203は、骨、中枢神経系、肺、副鼻腔、膀胱、皮膚など、全身の深刻な感染症の治療に成功しました。; |
| ● | LNCプラットフォーム技術を活用したサイレンシングRNA(siRNA)療法のデリバリーに関する社内プログラムによるin vitroデータの生成に向けて取り組んでいます。初期製剤データは、2023年第3四半期に期待されています。このプログラムは、2023年下半期に複数のin vivo生体内分布および動物有効性試験を継続する予定です;および |
| ● | National Resilience, Inc.(以下「National Resilience」)との共同研究プログラムは、mRNAを用いたin vitroおよびin vivo試験に焦点を当て、当社とNational Resilienceはレポーターおよび治療用オリゴヌクレオチドの送達;参照LNPに対するin vitroおよびin vivo送達両方に焦点を当て、初期データは2023年の第3四半期に期待されています。 |
| ● | 現在の予測によれば、当社のキャッシュポジションは、2024年後半までの計画的な事業運営に必要な資金を確保するのに十分であると判断しています。 |
Forward- Looking Statements
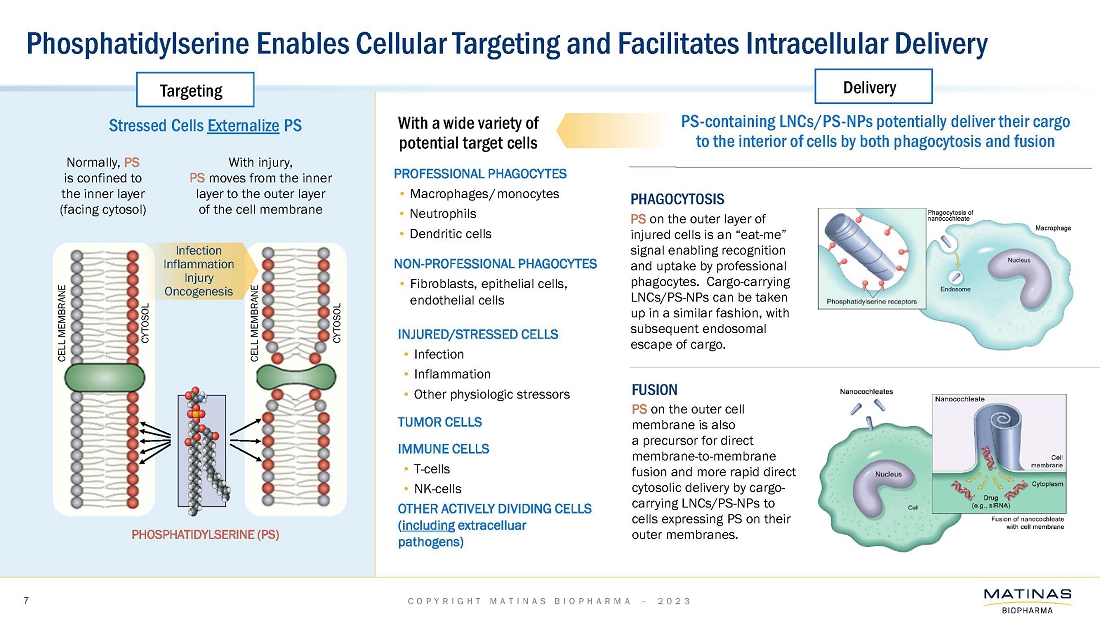
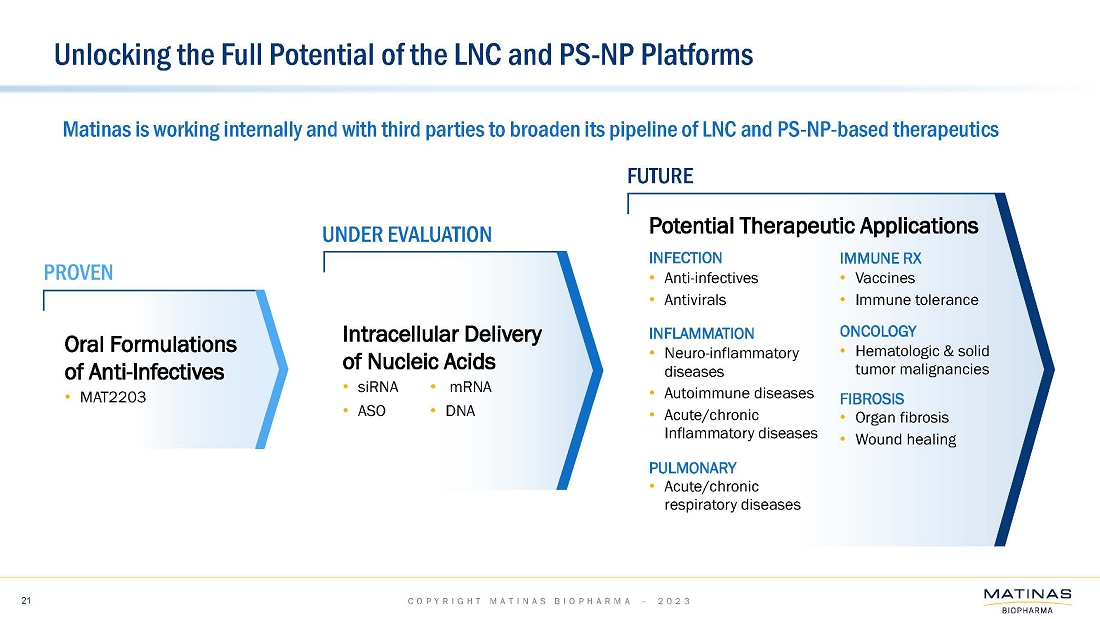
このForm 8-Kによる最新報告書には、National Resilience社との協業、同社のLNCおよびPS-NPプラットフォーム配信技術の可能性に関するものを含め、1933年証券法27A条、1934年証券取引法21E条および改正私募証券訴訟改革法の意味における一定の将来予想に関する記述が含まれています、および製品候補の将来の開発、当社の製品またはプラットフォーム・デリバリー技術に関する開発、ライセンスおよびパートナーシップの機会を特定し、有利な条件で追求する能力、必要な規制当局の承認を得る能力、ならびに将来の事象または条件に依存または言及する、本質的に予測的なその他の記述です。歴史的事実に関する記述以外のすべての記述は、将来予測に関する記述となりうるものです。
| - |
これらの記述は、「期待する」、「予想する」、「意図する」、「計画する」、「可能性がある」、「信じる」、「推定する」および同様の表現を含むが、これらに限定されない、将来予想に関する表現の使用によって識別されることがあります。これらの記述は、既知及び未知のリスク、不確実性及びその他の要因を含んでおり、実際の結果は、将来予想に関する記述によって明示的又は黙示的に示される将来の結果とは大きく異なる可能性があります。将来予想に関する記述は、以下のような多くのリスクおよび不確実性を伴いますが、これらに限定されるものではありません:当社が流動性ニーズを満たすための追加資本を許容できる条件で、または全く入手する能力(当社の製品候補の臨床試験を完了するために必要な追加資本を含む);当社の製品候補の研究および開発ならびに商業化を成功させる能力;臨床試験特有の不確実性、規制当局の承認取得の時期、費用および不確実性、当社の知的財産を保護する能力、執行役員、主要な人員またはコンサルタントの損失、競争、規制環境の変化または当社製品に影響を与える規制の賦課、ならびにフォーム10K、10Qおよび8KなどのSECへの提出書類の「リスク要因」に記載されている他の要因。投資家の皆様におかれましては、本書の日付現在においてのみ語られているこれらの将来予想に関する記述に過度の信頼を置かないようご 注意ください。法律で義務づけられている場合を除き、当社は、本書の日付後の事象や状況、または予期せぬ事象の発生を反映するために、かかる将来予想に関する記述の修正を公に発表する義務を負うものではありません。当社の製品候補はすべて開発段階にあり、販売または使用可能ではありません。
Item 9.01 財務諸表および添付資料
| Exhibit No. | Description | |
| 99.1 | 2023年5月10日付プレスリリース | |
| 99.2 | 2023年5月10日付の会社説明会 | |
| 104 | カバーページ インタラクティブデータファイル(inline xbrlドキュメントに埋め込まれています。) |
| - |
SIGNATURES
1934年証券取引法の要求事項に従い、登録者は本報告書を、正式に権限を与えられた以下の署名者によって、登録者を代表して署名させました。
| MATINAS BIOPHARMA HOLDINGS, INC. | ||
| Dated: May 10, 2023 | By: | /s/ Jerome D. Jabbour |
| Name: | Jerome D. Jabbour | |
| Title: | Chief Executive Officer | |
| - |
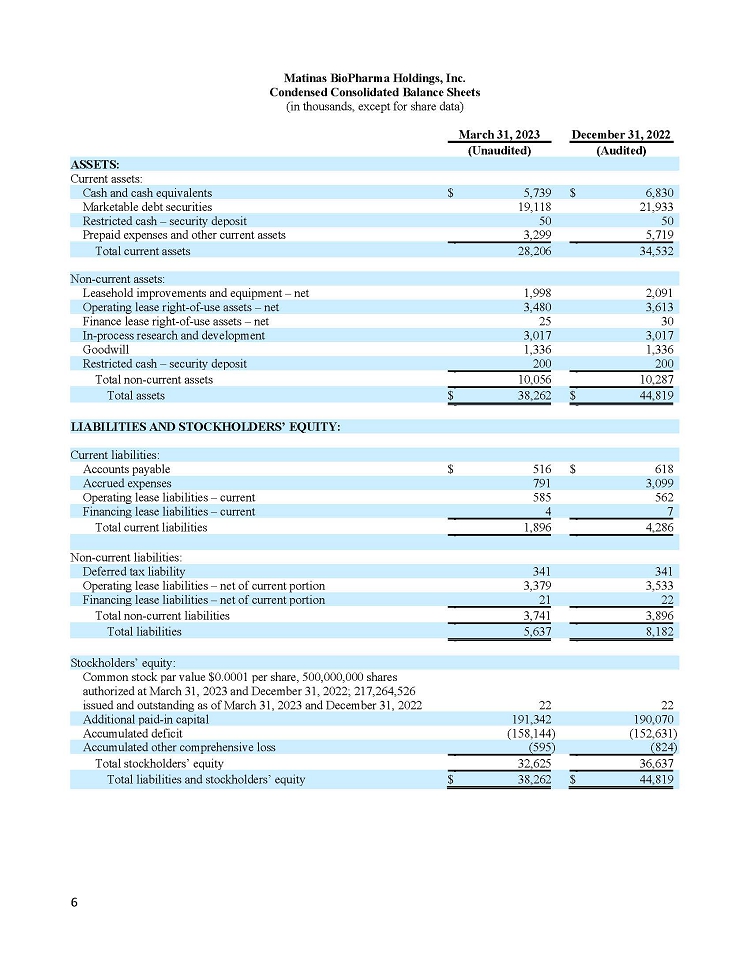
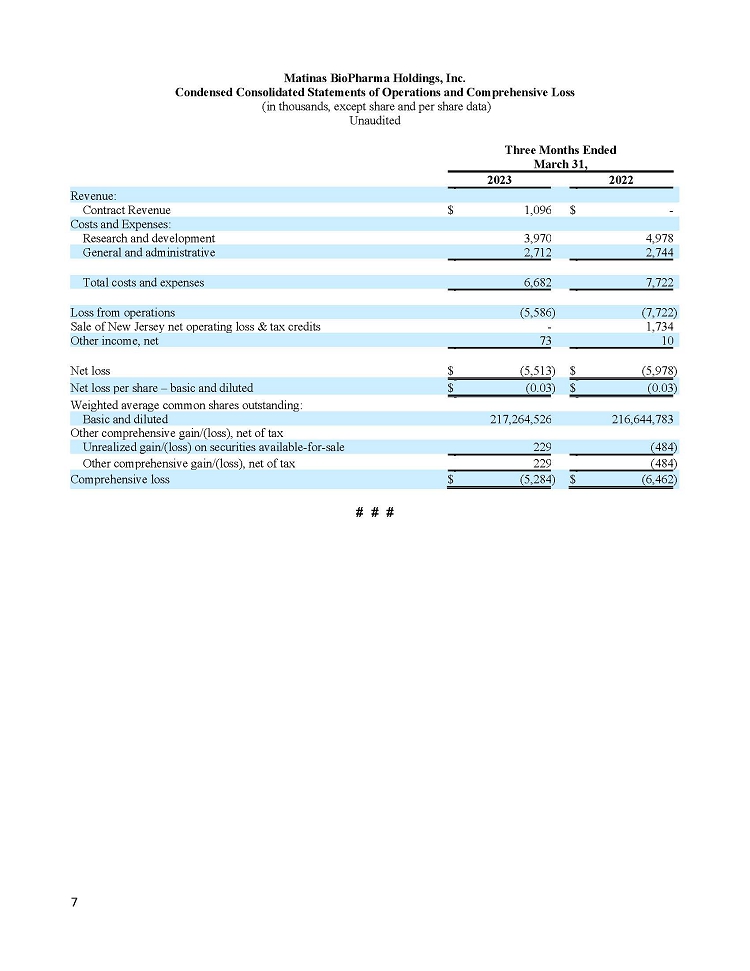
Exhibit 99.1





会社開示情報をすべてご覧に