Document
Exhibit 99.1
アーデリックス、2025年第4四半期および通期決算を発表、事業進捗状況を報告
IBSRELAの収益は2025年に73%増加し2億7420万ドルに達し、総収益は4億730万ドルとなった
患者第一のXPHOZAH戦略はアクセスを維持し、総処方数を増加させた
新規IBSRELA適応症および次世代NHE3阻害剤の開発プログラムを開始
会社は現在の事業目標を達成するために十分な資本を有している
カンファレンスコール(米国東部時間午後4時30分予定
マサチューセッツ州ウォルサム、2026年2月19日 - 重要な未充足医療ニーズを満たす革新的医薬品の開発と商業化に注力する商業段階のバイオ医薬品企業、アーデリックス社(Nasdaq: ARDX)は本日、2025年12月31日終了の第4四半期および通期の財務実績を発表し、事業進捗状況について報告した。
「2025年に達成した成果は、当社の医薬品をより多くの患者様に届けるためのチームの努力と規律ある実行力を反映したものであり、IBSRELAの著しい成長、XPHOZAHの採用拡大、臨床開発プログラムの迅速な進展がそれを裏付けています」と、Ardelyxの社長兼最高経営責任者であるマイク・ラーブは述べた。 「この強固な勢いをさらに拡大するため、2026年は当社の事業を、幅広い優れた医薬品ポートフォリオを基盤とした意義ある企業へと進化させる重要な機会と捉えています。当社の長期戦略は明確かつ揺るぎないものです。それは、未充足の医療ニーズが深刻な患者様に革新的な治療法を提供し、株主の皆様に持続的な価値を創出することです」
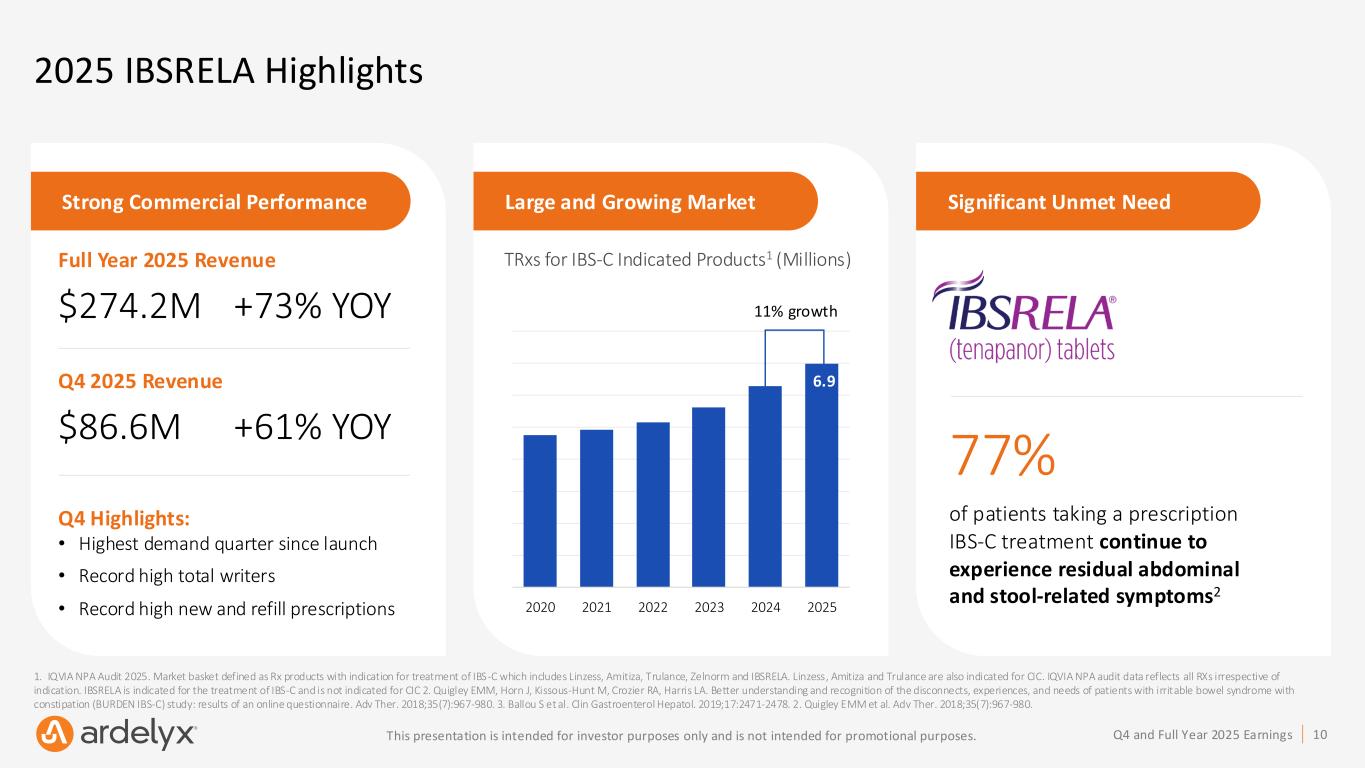
IBSRELA®(テナパノール)は2025年に2億7420万ドルの売上高を達成した
2025年のIBSRELAの収益は2億7420万ドルで、2024年通年の1億5830万ドルから73%の成長を示した。 同社は2025年第4四半期にIBSRELA収益8,660万ドルを記録し、2024年同期比61%増、2025年第3四半期比11%増となった。
アーデリックスは、対象医療提供者における処方箋の深さと幅の拡大、便秘型過敏性腸症候群(IBS-C)患者との関与強化、および処方箋の引き受け率のさらなる向上により、2026年以降も継続的な成長を見込んでいる。
アーデリックス社は、IBSRELAの2026年通期売上高が4億1000万ドルから4億3000万ドルの間になると予想しており、これは2025年比で少なくとも50%の成長を示す。IBSRELAが生み出した大きな勢いを受け、同社は2029年に年間売上高10億ドルを達成し、その後もさらなる成長を遂げると見込んでいる。
XPHOZAH®(テナパノール)は2025年、1億360万ドルの収益で終了した
2025年のXPHOZAHの売上高は1億360万ドルで、XPHOZAHの総処方量の前年比増加を反映しており、治療を受けるメディケア対象外の患者数の増加も含まれています。同社はまた、2025年第4四半期に2780万ドルの売上高を記録しました。
アーデリックス社は、2026年の成長が、対象となる医療処方者における臨床的確信の高まりと処方増加によって牽引されると見込んでいる。同社は2026年通期のXPHOZAH売上高が1億1000万ドルから1億2000万ドルの間になると予測している。
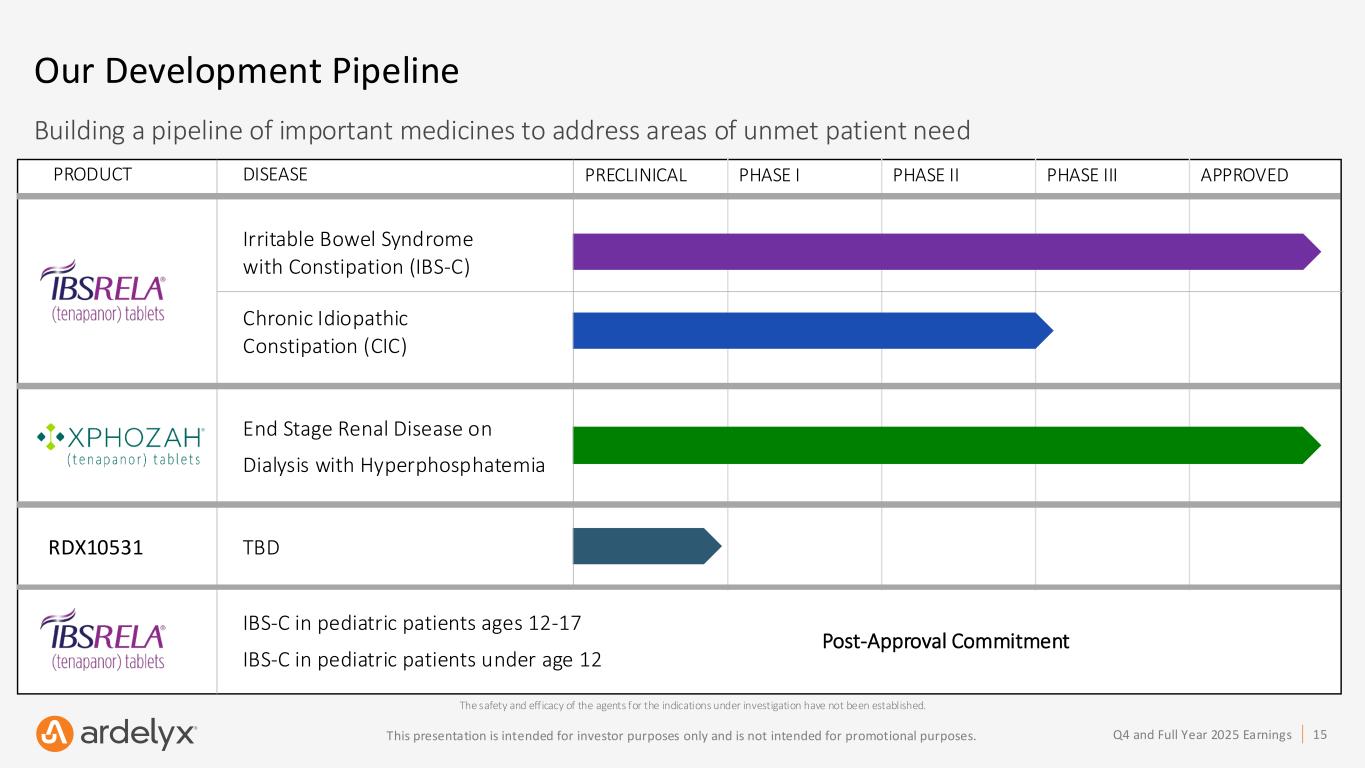
重要な医薬品パイプラインの構築
同社はIBSRELAの適応患者集団を慢性特発性便秘(CIC)患者に拡大する取り組みを推進し、CIC患者におけるテナパノールを評価する第3相試験「ACCEL」を開始した。初回投与は2026年第1四半期に実施予定である。 第3相試験の結果を待って、Ardelyx社はCIC適応症について米国食品医薬品局(FDA)に追加新薬申請(sNDA)を提出する意向である。ACCEL試験の患者登録は2026年末までに完了し、トップライン結果は2027年後半に得られる見込みである。
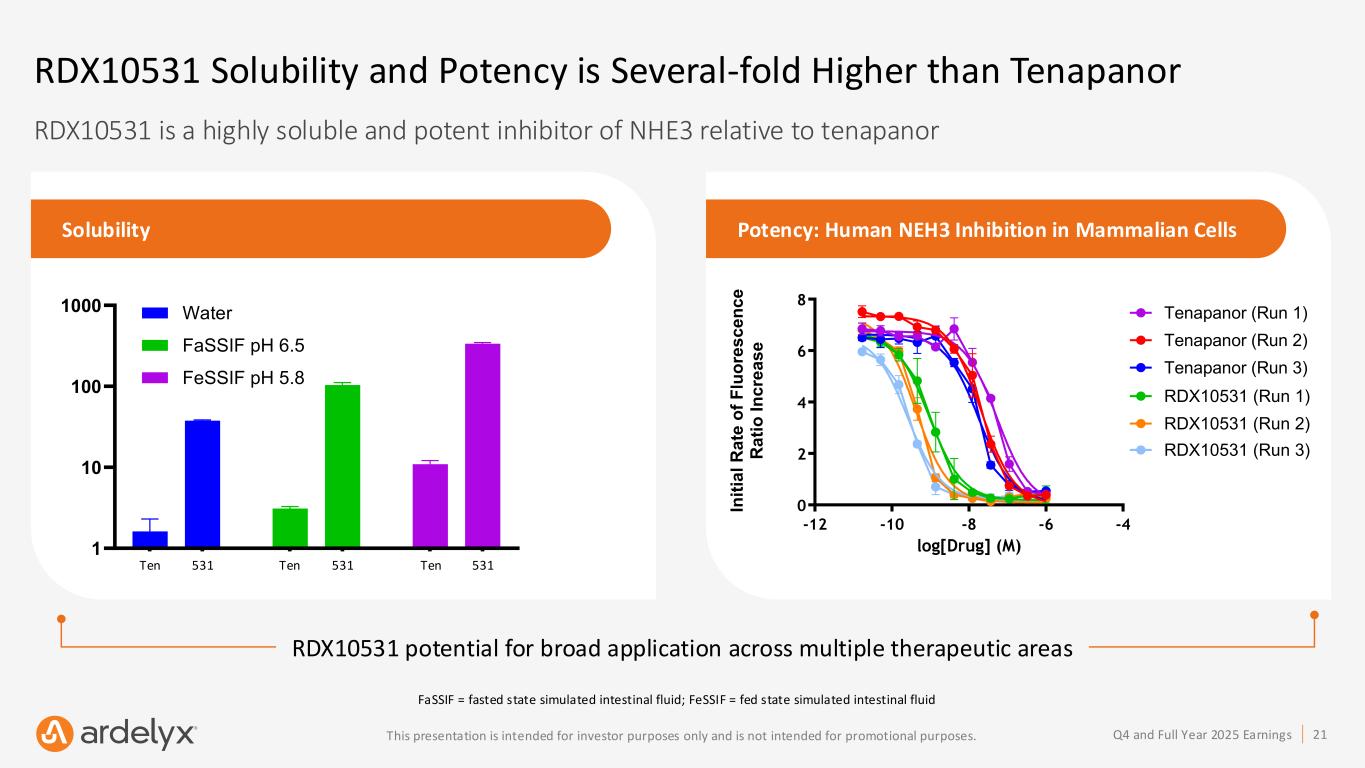
アーデリックス社は2025年、次世代型ナトリウム/水素交換体3(NHE3)阻害剤であるRDX10531の開発プログラムを開始した。同社は現在、2026年後半のFDAへの治験薬申請(IND)提出およびその後の第1相臨床試験開始に先立ち、前臨床開発活動を完了させている。
Other Corporate Developments
•米国特許商標庁は「テナパノールの経口製剤」と題する米国特許第12,539,299号を発行した。 本特許はIBSRELAおよびXPHOZAHの市販製剤をカバーし、有効期限は2042年11月26日である。両製品とも、FDAの「治療的同等性評価付き承認医薬品リスト」(通称オレンジブック)に本特許が記載されている。
•米国腎臓学会の年次総会「キッドニー・ウィーク」において、XPHOZAHによる患者満足度と血清リン値の低減を示す実世界エビデンス研究のデータを含む4件のポスター発表が行われた。
•IBSRELAの有効性を裏付ける3つのポスターが、米国消化器病学会(ACG)2025年次総会で発表された。
2025年通期決算
• 現金ポジション:2025年12月31日現在、当社の現金、現金同等物および短期投資の合計は2億6470万ドルであり、2024年12月31日現在の合計2億5010万ドルから増加した。
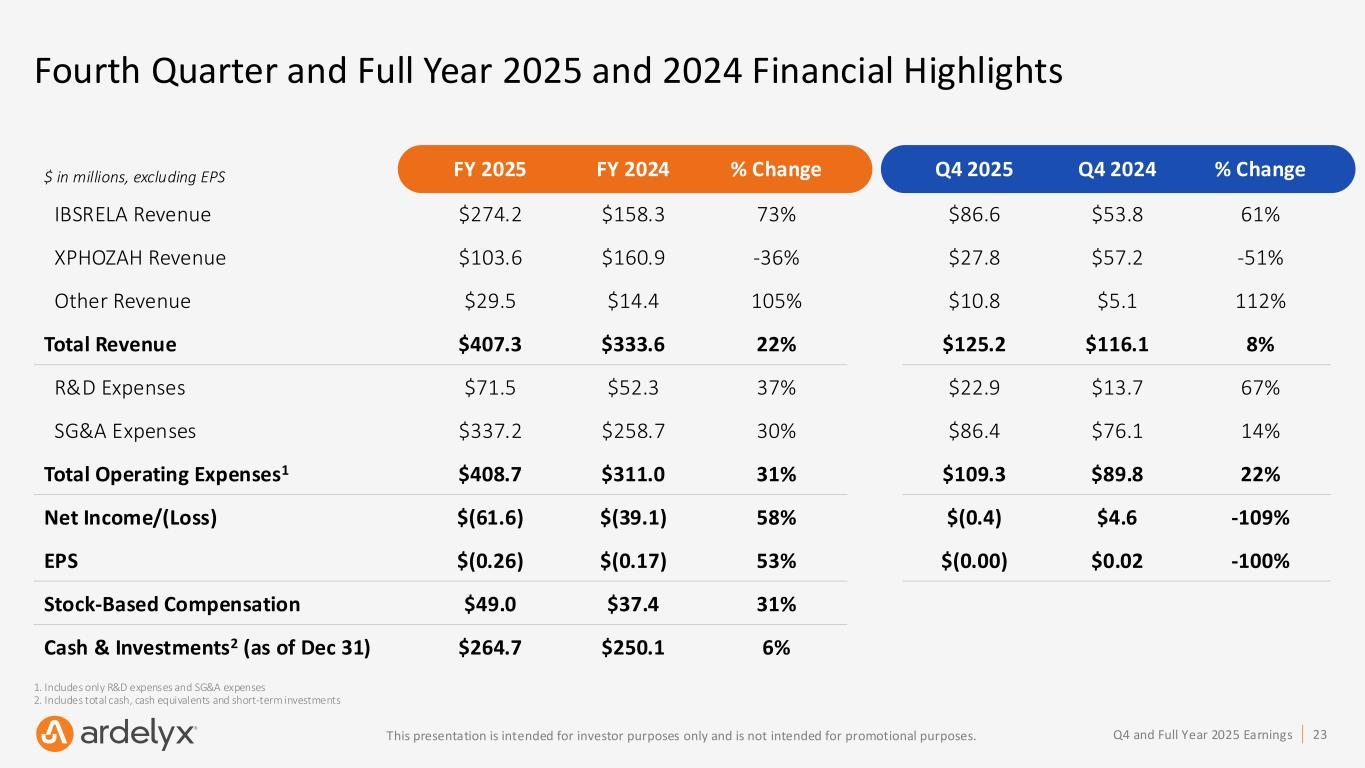
• 収益:2025年12月31日終了年度の総収益は4億730万ドルであり、2024年度の総収益3億3360万ドルから増加した。これはIBSRELA収益の増加によるものである。
◦IBSRELAの収益は2億7420万ドルで、2024年の1億5830万ドルと比較した。
◦XPHOZAHの収益は1億360万ドルで、2024年の1億6090万ドルと比較した。
◦その他の収益(製品供給、ライセンス料、将来のロイヤルティ売却に関連する非現金ロイヤルティ収益を含む)は、2024年度の1,440万ドルに対し、2,950万ドルとなった。
• 研究開発費:2025年12月31日終了年度における研究開発費は7,150万ドルであり、2024年12月31日終了年度の5,230万ドルから増加した。この増加は、最近発表されたパイプラインプログラムへの投資および科学コミュニティとの医療連携強化に関連するものだった。
• 販売費及び一般管理費:2025年12月31日終了年度の販売費及び一般管理費は3億3,720万ドルであり、2024年12月31日終了年度の2億5,870万ドルから増加した。この増加は主に、IBSRELAおよびXPHOZAHの継続的な商業化に伴うコスト増に関連している。
• 当期純損失:2025年12月31日終了年度の当期純損失は6,160万ドル(1株当たり損失0.26ドル)であり、2024年12月31日終了年度の当期純損失3,910万ドル(1株当たり損失0.17ドル)と比較した。 2025年度通期の純損失には、株式報酬費用4,900万ドルが含まれています。
Conference Call Details
当社は本日2026年2月19日午後4時30分(米国東部時間)に、本日の発表内容に関する電話会議を開催します。電話会議への参加をご希望の方は、国内からは(877) 346-6112、国際からは(848) 280-6350におかけいただき、「Ardelyxの電話会議に参加したい」とお伝えください。 ライブ音声ウェブキャストおよび関連プレゼンテーション資料は、当社ウェブサイト(www.ardelyx.com)の投資家向けページからもアクセス可能です。電話会議終了後30日間、同サイトで閲覧いただけます。
IMPORTANT SAFETY INFORMATION (IBSRELA)
|
|
|
|
|
|
| 警告:小児患者における重篤な脱水の危険性 |
|
| ibsrelaは6歳未満の患者には禁忌である。幼若ラットの非臨床試験において、テナパノールの投与により脱水が原因と推定される死亡が発生した。6 歳から 12 歳未満の患者には ibsrela の使用を避けてください。18歳未満の患者におけるibsrelaの安全性と有効性は確立していない。 |
CONTRAINDICATIONS
•IBSRELAは、重篤な脱水症状のリスクがあるため、6歳未満の患者には禁忌である。
•IBSRELAは、既知または疑われる機械的消化管閉塞を有する患者には禁忌である。
WARNINGS AND PRECAUTIONS
小児患者における重篤な脱水のリスクについて
•IBSRELAは6歳未満の患者には禁忌である。18歳未満の患者におけるIBSRELAの安全性および有効性は確立されていない。幼若ラット(生後1週間未満;ヒト年齢換算で2歳未満相当)において、テナパノール経口投与後に体重減少および死亡が認められ、脱水によるものと推定された。 より年長の若齢ラット(ヒト年齢換算2歳以上12歳未満)におけるデータは存在しません。
•6歳以上12歳未満の患者へのIBSRELAの使用は避けること。より年長の若齢ラットにおけるデータはないものの、より若いラットにおける死亡例および小児患者における臨床的安全性・有効性データの欠如を考慮し、6歳以上12歳未満の患者へのIBSRELAの使用は避けること。
Diarrhea
IBS-Cを対象とした2件の無作為化二重盲検プラセボ対照試験において、下痢が最も頻度の高い有害事象であった。IBSRELA投与患者の2.5%に重度の下痢が報告された。重度の下痢が生じた場合は、投与を中止し、患者に水分補給を行うこと。
MOST COMMON ADVERSE REACTIONS
IBSRELA投与患者における最も頻度の高い有害事象(発生率≥2%かつプラセボより高い)は、下痢(16%対プラセボ4%)、腹部膨満感(3%対<1%)、鼓腸(3%対1%)、めまい(2%対<1%)であった。
INDICATION
IBSRELA(テナパノール)は、成人の便秘型過敏性腸症候群(IBS-C)の治療に用いられます。
追加のリスク情報については、箱枠警告を含む添付文書全文をご参照ください。
IMPORTANT SAFETY INFORMATION (XPHOZAH)
CONTRAINDICATIONS
XPHOZAH is contraindicated in:
•6歳未満の小児患者
•既知または疑われる機械的消化管閉塞を有する患者
会社開示情報をすべてご覧になるには株探プレミアムの
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初め
会社開示情報をすべてご覧になるには株探プレミアムの登録
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるに
会社開示情報をすべてご覧になるには株探プレミアムの登録が
Caitlin Lowie
clowie@ardelyx.com
会社開示情報をすべてご覧になるには株探プレミアムの
(in thousands)
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初
(Unaudited)
会社開示情報をすべてご覧になるには株探プレミアムの登録が
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30






























 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン