米国証券取引委員会
Washington, D.C. 20549
FORM 8-K
1934年証券取引所法第13条または第15条(d)に基づく最新報告書
報告日(最も古いイベントの報告日):2024年8月8日
IMMUNIC社
(チャーターで指定された登録者の正確な名前)
| デラウェア | 001-36201 | 56-2358443 |
| (法人設立の州またはその他の管轄区域) | (Commission File Number) | (IRS Employer Identification No.) |
1200アベニュー・オブ・ジ・アメリカズ、スイート200
New York, NY 10036
USA
(主要経営陣の住所)
登録者の電話番号(市外局番を含む(332) 255-9818
Form8-Kの提出が、以下の条項のいずれかに基づく登録者の提出義務を同時に満たすことを意図している場合は、以下の該当するチェックボックスをチェックしてください:
| ☐ | 証券法に基づく規則425に従った書面によるコミュニケーション(17 cfr 230.425) |
| ☐ | 取引所法の下でのルール14a-12(17 cfr 240.14a-12)に基づく資料の勧誘。) |
| ☐ | 取引所法の規則14d-2(b)に基づく開始前のコミュニケーション(17 cfr 240.14d-2(b)) |
| ☐ | 証券取引法の規則13e-4(c)に基づく開始前のコミュニケーション(17 cfr 240.13e-4(c)) |
法第12条(b)に従って登録された証券:
| Title of each class | Trading Symbol(s) | 登録されている取引所の名称 |
| 普通株式、額面0.0001ドル | IMUX | the nasdaq stock market llc |
登録者が1933年証券法規則405(本章§230.405)または1934年証券取引法規則12b-2(本章§240.12b2)で定義される新興成長企業であるかどうかをチェックマークで示す。
Emerging growth company ☐
新興成長企業の場合、登録者が、取引所法第13条(a)に従って提供される新規または改訂された財務会計基準に準拠するための移行期間の延長を利用しないことを選択した場合は、チェックマークで示す。はい ☐ いいえ
Item 2.02. 営業成績および財務状況
2024年8月8日、Immunic, Inc.(以下「当社」)は、2024年6月30日に終了した四半期決算を発表し、企業最新情報を提供するプレスリリース(以下「本プレスリリース」)を発表した。
プレス・リリースを含め、本フォーム 8-K の項目 2.02 に記載された情報は、1934 年証券取引所法(改正後)第 18 条における「提出された」ものとはみなされず、同法または 1933 年証券取引所法(改正後)第 11 条および第 12 条(a)(2)の責任を問われるものではありません。また、本情報は、米国証券取引委員会に提出する当社のいかなる提出書類にも、当該提出書類に明示的に言及されている場合を除き、参照により組み込まれるものとはみなされません。
Item 8.01. Other Events
2024年8月8日、当社は最新のプレゼンテーション(以下「本プレゼンテーション」)をウェブサイトに掲載した。同プレゼンテーションの写しは別紙99.2としてここに提出され、参照することによりここに組み込まれる。
将来の見通しに関する記述についての注意事項
本Form 8-K、プレスリリース、およびプレゼンテーションに記載されている一部の記述は、1995年米国私募証券訴訟改革法が定めるセーフハーバーの趣旨に照らし、重大なリスクと不確実性を伴う「将来の見通しに関する記述」です。本Current Report on Form 8-K、プレスリリース、および本プレゼンテーションに含まれる、新しい経営陣の採用および昇進、戦略、将来の事業、将来の財務状況、将来の収益、予測経費、現金およびキャッシュ・ランウェイの充足、予想される時期、臨床試験の開発および結果、経営陣の見通し、計画、目標に関する記述は、過去の事実に関する記述を除き、すべて将来の見通しに関する記述です。このような記述の例としては、イミュニックの開発プログラムおよび対象疾患に関する記述、イミュニックの開発プログラムが対象疾患を安全かつ効果的に治療できる可能性に関する記述、イミュニックの開発プログラムに関する前臨床および臨床データ、現在および将来の臨床試験の実施時期、予想される臨床マイルストーンなどがありますが、これらに限定されるものではありません;当社の性質、戦略および重点事項ならびにこれらに関する今後の更新情報、当社の製品候補の開発および商業的可能性、当社の資本、資源および所有構造に関する予想、当社の経営陣および取締役会の構成、ならびに当社の予想されるキャッシュ・ランウェイ。Immunicは、将来予想に関する記述で開示された計画を実際に達成したり、意図を実行したり、期待や予測を達成したりしない可能性があり、これらの将来予想に関する記述を過度に信頼すべきではありません。このような記述は経営陣の現在の予想に基づくものであり、重大なリスクと不確実性を伴います。実際の結果および業績は、COVID-19の流行、インフレの進行、ウクライナ・ロシア紛争および中東紛争が計画中および進行中の臨床試験に及ぼす影響、偶発的な将来の負債および事業運営に必要な将来の現金利用および準備金を予測する能力に関連するリスクおよび不確実性、事業目標および事業要件を満たすのに十分な財務およびその他の資源の利用可能性など(ただし必ずしもこれらに限定されない)、多くの要因の結果として、将来見通しに関する記述で予測されたものとは大きく異なる可能性があります、2024年1月の第三者割当増資のトランシェ2およびトランシェ3において資金調達を受けるために必要な最低平均価格および取引量の条件を満たす能力を含む、事業目的および事業要件を満たすのに十分な財務および経営資源の利用可能性、前臨床試験および臨床試験の結果が将来の臨床試験結果を予測できない可能性があること、Immunicの知的財産による保護および市場独占性、医薬品開発および薬事承認プロセスに関するリスク、競合製品および技術変化の影響。これらのリスク、不確実性およびその他の要因の詳細なリストおよび説明は、2024年2月22日にSECに提出された当社の2023年12月31日終了会計年度の年次報告書(フォーム10-K)およびその後のSECへの提出書類の「リスク要因」の項に記載されています。これらの提出書類のコピーは、www.sec.gov または ir.imux.com/sec-filings からオンラインで入手できます。
本Current Report on Form 8-K、プレスリリース、およびプレゼンテーションに記載された記述は、本書に記載された日付現在のものであり、その後の事象や展開により、当社の期待や確信が変更される可能性があります。当社は、将来のある時点で、これらの将来の見通しに関する記述を更新することを選択する可能性がありますが、当社は、法律で義務付けられている場合を除き、新たな情報、将来の出来事またはその他の結果にかかわらず、その義務を明確に否認します。これらの将来見通しに関する記述は、ここに記載された日付以降の当社の見解を表すものとして依拠すべきではありません。
Item 9.01. 財務諸表および添付資料
| Exhibit | Description |
| 99.1 | 2024年8月8日付プレスリリース。 |
| 99.2 | 2024年8月8日付プレゼンテーション。 |
| 104 | inline xbrlでのこのcurrent report on form 8-kのカバーページ |
SIGNATURES
1934年証券取引所法(改正後)の要件に従い、登録者は本報告書に正式に権限を付与された署名者により、登録者を代表して署名させた。
| Dated: August 8, 2024 | Immunic, Inc. | |
| By: | /s/ Daniel Vitt | |
| Daniel Vitt | ||
| Chief Executive Officer | ||
 |
イミュニック・インク2024年第2四半期決算報告と最新情報のお知らせ
– ノバルティス社およびバイオジェン社で多発性硬化症治療薬商業化の経験を積んだジェイソン・タルディオ氏が最高執行責任者兼社長に就任 - ニュースリリース
– ブレインヘルス分野のオピニオンリーダーであるシモーナ・スケリャネック氏を取締役に迎え、取締役会を強化。
– 再発性多発性硬化症を対象としたENSURE臨床第3相試験および進行性多発性硬化症を対象としたCALLIPER臨床第2相試験は順調に進行中
– 本日8月8日午前8時(米国東部時間)よりウェブキャストを実施。
ニューヨーク発、2024年8月8日 - 慢性炎症性疾患および自己免疫疾患に対する経口低分子治療薬の臨床パイプラインを開発中のバイオテクノロジー企業、イムニック・インク(Nasdaq: IMUX)は本日、2024年6月30日を期末とする第2四半期および6カ月間の決算を発表し、企業最新情報を提供しました。
「第2四半期およびその後の期間において、当社は引き続き臨床面および事業面で進歩を遂げることができました。ジェイソンのノバルティス社やバイオジェン社を含む大手バイオテクノロジー企業や製薬企業における多発性硬化症(MS)治療薬の上市と商業化における実績ある経験や豊富な提携経験は、特に当社の後期臨床資産である経口核内受容体関連1(Nurr1)活性化剤ビドフルジムス・カルシウム(IMU-838)の商業化の可能性に近づく中で、非常に貴重なものとなるでしょう。シモーナ・スケリャネック氏は、直近ではロシュ社で神経科学・希少疾患グローバルヘッドの上級副社長を務め、MS治療薬として最も成功した医薬品のひとつであるオクレバス®(一般名:オクレリズマブ)を含め、2桁の売上成長を達成した実績を有しています。「9月にニューヨークで開催されるMS研究開発デーでは、当社のMS開発プログラムについて詳しく説明する予定です。このイベントでは、イミュニックの経営陣とともに、業界の著名な専門家2名をお招きし、ビドフルジムスカルシウムのユニークなプロファイルと、再発性MS(RMS)と進行性MS(PMS)の両患者に選択される画期的な治療薬となる可能性について議論する予定です。ビドフルジムス・カルシウムは、神経保護作用、抗炎症作用、抗ウイルス作用により、くすぶり続けるMSのすべての要素を選択的に管理するように設計されていることから、MS患者のあらゆる範囲に総合的な解決策を提供することで、今日の標準治療を向上させることができると考えています。"
「PMS患者を対象としたビドフルジムス・カルシウムの第2相CALLIPER試験のトップラインデータを来年4月に報告できることを楽しみにしています。先に報告された中間解析では、アンメット・メディカル・ニーズが最も高いサブタイプである非再発性二次性進行性MS(SPMS)を含むPMS患者集団全体において、ニューロフィラメント軽鎖(NfL)レベルがプラセボから明確に分離したことが示されました。トップラインデータが引き続き神経保護効果を示し、試験の主要評価項目および主要な副次評価項目を満たせば、本薬を非再発性SPMSに対する初めての経口治療薬として位置づけることができる可能性もあります。また、RMSを対象とした第3相ENSUREプログラムも順調に進んでおり、2026年第2四半期に第1次ENSURE試験を、2026年後半に第2次ENSURE試験を完了する予定です。"
 |
第2四半期には、当社の2番目の臨床プログラムであるIMU-856の第2相臨床試験の準備も進めました。IMU-856は、腸管バリア機能と腸管上皮の生理的再生の転写制御因子として機能するタンパク質であるサーチュイン6(SIRT6)を標的とした経口投与可能な全身作用型低分子モジュレーターです。当社は、本プログラムの次の臨床開発ステップのための資金調達、ライセンス供与、提携の可能性を模索しています。IMU-856は、腸壁の再生を通じて健康な腸を回復させることにより、胃腸障害を治療する画期的な治療法となる可能性があると考えています。セリアック病患者を対象とした当社の第1b相臨床試験のデータでは、IMU-856がセリアック病の病態生理の4つの重要な側面(腸管構造の保護、患者の症状の改善、バイオマーカー反応、栄養吸収の促進)において、プラセボを上回る効果を示したことが示されています。このデータに基づいて、他の消化器疾患への臨床応用の可能性も検討しています。"
2024年第2四半期以降のハイライト
| · | 2024年7月2024年7月22日付で、医薬品開発と商業化において数十年の経験を持つ脳の健康分野のオピニオンリーダーであるシモーナ・スケリャネック氏(M.Pharm, MBA)を取締役に任命することを発表。 |
| · | 2024年7月ヴィドフルディムス・カルシウムの上市に向けた社内体制を整えるとともに、パトリック・ウォルシュ最高経営責任者(CEO)と緊密に連携し、ヴィドフルディムス・カルシウムおよびイミュニックの他の新薬候補に関するさまざまな提携の可能性に備える。また、プログラム管理・臨床開発業務担当副社長であったワーナー・グラディネスが最高開発責任者に昇格したことも報告された。 |
| · | 2024年4月再発寛解型MS患者を対象としたビドフルジムス・カルシウムの第2相EMPhASIS試験のデータが、米国神経学会の機関誌Neurology® Neuroimmunology & Neuroinflammationに掲載されることを発表。 |
| · | 2024年4月:サンフランシスコでMS研究開発デーを開催し、ビドフルジムスカルシウムの神経保護効果を裏付ける前臨床および臨床データとともに、MSの最新動向について経営陣が議論した。 |
Anticipated Clinical Milestones
| · | MSにおけるビドフルジムスカルシウム:PMSを対象としたビドフルジムスカルシウムの第2相CALLIPER試験のトップラインデータは2025年4月に期待される。ENSUREプログラムの無益性中間解析は2024年第4四半期に予定されている。最初のENSURE試験の完了は2026年第2四半期、2番目のENSURE試験の完了は2026年下半期と現在のところ予想されている。 |
| · | セリアック病におけるIMU-856:第1b相臨床試験の良好なデータに基づき、資金調達、ライセンス供与または提携を条件として、IMU-856の第2相臨床試験の準備を進めている。 |
財務および営業成績
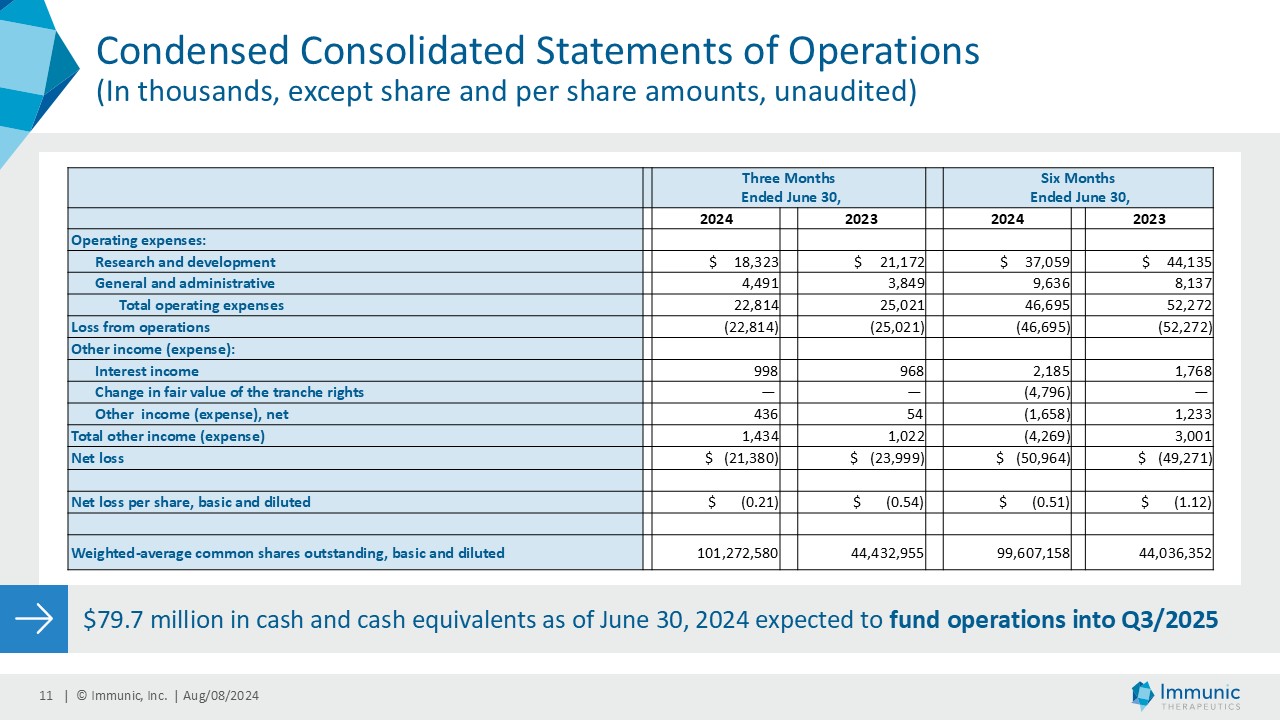
| · | 2024 年 6 月 30 日に終了した 3 ヶ月間の研究開発費は、2023 年 6 月 30 日に終了した 3 ヶ月間の 2,120 万ドルに対し、1,830 万ドルであった。この280万ドルの減少は、(i)セリアック病を対象とした第1相試験の完了によるIMU-856に関連する外部開発費の180万ドルの減少、(ii)乾癬および去勢抵抗性前立腺がんを対象としたイズメロガントプログラムの優先順位を下げたことによる100万ドルの減少、(iii)多くのカテゴリーにわたる関連費用の0.5百万ドルの減少を反映しています。この減少は、ビドフルジムス・カルシウム・プログラムに関連する外部開発費の0.5百万ドルの増加により相殺された。 |
 |
2024年6月30日に終了した6ヵ月間の研究開発費は3,700万ドルで、2023年6月30日に終了した6ヵ月間は4,410万ドルであった。この710万ドルの減少は、(i)乾癬および去勢抵抗性前立腺がんを対象としたイズメロガント・プログラムの優先順位を下げたことによる340万ドルの減少、(ii)セリアック病を対象とした第1相試験の完了によるIMU-856に関連する外部開発費の290万ドルの減少、(iii)ビドフルジムス・カルシウム・プログラムに関連する外部開発費の9百万ドルの減少、(iv)多くのカテゴリーにわたる関連費用の8百万ドルの減少を反映している。この減少は、人件費の0.9百万ドルの増加により相殺された。このうち0.2百万ドルは現金支出を伴わない株式報酬に関連するもので、残りは人員増によるものである。
| · | 2024年6月30日に終了した3ヶ月間の一般管理費(G&A)は450万ドルで、2023年6月30日に終了した同期間は380万ドルであった。これは主に、(i)G&A部門の人件費が0.3百万ドル増加したこと(うち0.1百万ドルは現金支出を伴わない株式報酬費用に関連し、残りは人員増に関連)、(ii)法務およびコンサルタント費用が0.1百万ドル増加したこと、(iii)多数のカテゴリーにわたる費用に関連して0.2百万ドル増加したことによるものである。 |
2024年6月30日に終了した6ヶ月間のG&A費は960万ドル(2023年6月30日に終了した同期間は810万ドル)であった。この150万ドルの増加は主に(i)G&A部門の人件費が110万ドル増加したことによるもので、そのうちの0.6百万ドルは現金支出を伴わない株式報酬費用に関連するもので、残りは人員の増加に関連するものである。
| · | 2024 年 6 月 30 日に終了した 3 ヶ月間の受取利息は、2023 年 6 月 30 日に終了した 3 ヶ月間と比べ横ばいの 100 万ドルとなった。 |
2024年6月30日に終了した6ヵ月間の受取利息は220万ドルであった(2023年6月30日に終了した同期間は180万ドル)。0.4百万ドルの増加は金利上昇によるものである。
| · | 2024年6月30日に終了した6ヶ月間におけるトランシェ権の公正価値の変動480万ドルは、2024年1月の第三者割当増資の将来のトランシェ2および3に関連するトランシェ権の価値の変動に関連する現金支出を伴わない費用であった。 |
| · | 2024年6月30日に終了した3ヶ月間のその他の収益(費用)は、前年同期の0.1百万ドルに対し、0.4百万ドルであった。0.4百万ドルの増加は、主に為替差益が0.7百万ドル増加したことに起因する。この増加は、(i)2023年に受領したその他の助成金が0.2百万ドル減少したこと、および(ii)オーストラリアにおける臨床試験への支出が減少した結果、オーストラリアにおける臨床試験に対する研究開発税制優遇措置が0.1百万ドル減少したことにより相殺された。 |
 |
2024年6月30日に終了した6ヶ月間において、その他の収益(費用)は(170万ドル)であった(2023年6月30日に終了した同期間は120万ドル)。この290万ドルの減少は主に、(i)2024年1月のPIPEファイナンスによる取引費用のうち、取引完了時に設定されたトランシェ権に関連する部分に関する費用170万ドル、(ii)ドイツ連邦財務省の助成金110万ドルが第4四半期に計上されたことによる。100万ドルを2023年第1四半期に認識した前年度より1四半期早い2023年第4四半期に認識したこと、(iii)オーストラリアでの臨床試験への支出が減少した結果、オーストラリアでの臨床試験に対する研究開発税制優遇措置が0.5百万ドル減少したこと、(iv)2023年に受領したその他の助成金が0.4百万ドル減少したこと。この減少は、為替差益の0.8百万ドルの増加により相殺された。
| · | 2024年6月30日に終了した3ヶ月間の純損失は約2,140万ドル、基本的および希薄化後1株当たり0.21ドルで、これに対し2023年6月30日に終了した同期の純損失は約2,400万ドル、基本的および希薄化後1株当たり0.54ドル、加重平均発行済み普通株式数は101,272,580株であった。 |
2024年6月30日に終了した6ヶ月間の純損失は約5,100万ドル、基本的および希薄化後1株当たり0.51ドルで、これに対し2023年6月30日に終了した同期の純損失は約4,930万ドル、基本的および希薄化後1株当たり1.12ドル、加重平均発行済み普通株式数は99,607,158株であった。
| · | 2024年6月30日現在の現金および現金同等物は7,970万ドル。これらの資金により、イムニック社は2025年第3四半期までの運営資金を確保できる見込みである。 |
Webcast Information
イミュニックは本日午前8時(米国東部時間)よりウェブキャストを行います。ウェブキャストへの参加をご希望の方は、https://imux.zoom.us/webinar/register/WN_ae1TwcxTQ9GTkRUmQSOgTA、またはイミュニックのウェブサイトir.imux.com/events-and-presentationsの「イベントとプレゼンテーション」セクションから事前にご登録ください。登録者には、オンライン参加用のリンクまたはダイアルイン用の電話番号が記載された確認メールが送信されます。
ウェブキャストのアーカイブ再生は、終了後約1時間後にイミュニックのウェブサイト(ir.imux.com/events-and-presentations)にてご覧いただけます。
About Immunic, Inc.
イミュニック・インク(Nasdaq: IMUX)は、慢性炎症性疾患および自己免疫疾患に対する経口低分子治療薬の臨床パイプラインを開発しているバイオテクノロジー企業である。同社の主要開発プログラムであるビドフルジムス・カルシウム(IMU-838)は、現在、再発性多発性硬化症および進行性多発性硬化症の治療薬としてそれぞれ第3相および第2相臨床試験段階にあり、再発性多発性硬化症、進行性多発性硬化症および中等度から重度の潰瘍性大腸炎を患う患者を対象とした第2相臨床試験で治療活性を示した。ビドフルジムス・カルシウムは、ジヒドロオロチン酸デヒドロゲナーゼ(DHODH)を選択的に阻害することにより、ファースト・イン・クラスの核内受容体関連1(Nurr1)活性化因子としてのメカニズムによる神経保護作用と、さらなる抗炎症作用および抗ウイルス作用を併せ持つ。サーチュイン6(SIRT6)を標的とするIMU-856は、腸のバリア機能を回復させ、腸上皮を再生させることを目的としており、セリアック病など多くの消化器疾患に応用できる可能性があり、現在第2相臨床試験の準備中である。現在前臨床試験中のIMU-381は、消化器疾患のニーズに特化して開発中の次世代分子である。詳細については、www.imux.com。
 |
将来の見通しに関する記述についての注意事項
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示
会社開示情報をすべてご覧になるには株探プ
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミ
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要で
 |
会社開示情報をすべてご
会社開示情報をすべてご覧にな
会社開示情報をすべてご覧に
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要
(Unaudited)
 |
会社開示情報をすべてご覧にな
会社開示情報をすべて
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要
(Unaudited)
















 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン