米国証券取引委員会
Washington, D.C. 20549
FORM 8-K
1934年証券取引所法第13条または第15条(d)に基づく最新報告書
報告日(最も古いイベントの報告日):2023年8月3日
IMMUNIC社
(チャーターで指定された登録者の正確な名前)
| デラウェア | 001-36201 | 56-2358443 |
| (法人設立の州またはその他の管轄区域) | (Commission File Number) | (IRS Employer Identification No.) |
1200アベニュー・オブ・ジ・アメリカズ、スイート200
New York, NY 10036
USA
(主要経営陣の住所)
登録者の電話番号(市外局番を含む(332) 255-9818
Form8-Kの提出が、以下の条項のいずれかに基づく登録者の提出義務を同時に満たすことを意図している場合は、以下の該当するチェックボックスをチェックしてください:
| ☐ | 証券法に基づく規則425に従った書面によるコミュニケーション(17 cfr 230.425) |
| ☐ | 取引所法の下でのルール14a-12(17 cfr 240.14a-12)に基づく資料の勧誘。) |
| ☐ | 取引所法の規則14d-2(b)に基づく開始前のコミュニケーション(17 cfr 240.14d-2(b)) |
| ☐ | 証券取引法の規則13e-4(c)に基づく開始前のコミュニケーション(17 cfr 240.13e-4(c)) |
法第12条(b)に従って登録された証券:
| Title of each class | Trading Symbol(s) | 登録されている取引所の名称 |
| 普通株式、額面0.0001ドル | IMUX | the nasdaq stock market llc |
登録者が1933年証券法規則405(本章§230.405)または1934年証券取引法規則12b-2(本章§240.12b2)で定義される新興成長企業であるかどうかをチェックマークで示す。
Emerging growth company ☐
新興成長企業の場合、登録者が、取引所法第13条(a)に従って提供される新規または改訂された財務会計基準に準拠するための移行期間の延長を利用しないことを選択した場合は、チェックマークで示す。はい ☐ いいえ
Item 2.02. 営業成績および財務状況
2023年8月3日、Immunic, Inc.(以下「当社」)は、2023年6月30日に終了した四半期決算を発表し、企業最新情報を提供するプレスリリース(以下「本プレスリリース」)を発表した。
プレス・リリースを含め、本フォーム 8-K の項目 2.02 に記載された情報は、1934 年証券取引所法(改正後)第 18 条における「提出された」ものとはみなされず、同法または 1933 年証券取引所法(改正後)第 11 条および第 12 条(a)(2)の責任を問われるものではありません。また、本情報は、米国証券取引委員会に提出する当社のいかなる提出書類にも、当該提出書類に明示的に言及されている場合を除き、参照により組み込まれるものとはみなされません。
Item 8.01. Other Events
2023年8月3日、当社は最新のプレゼンテーション(以下「本プレゼンテーション」)をウェブサイトに掲載した。同プレゼンテーションの写しは別紙99.2としてここに提出され、参照することによりここに組み込まれる。
Item 9.01. 財務諸表および添付資料
| Exhibit | Description |
| 99.1 | 2023年8月3日付プレスリリース。 |
| 99.2 | 2023年8月3日付プレゼンテーション。 |
| 104 | inline xbrlでのこのcurrent report on form 8-kのカバーページ |
SIGNATURES
1934年証券取引所法(改正後)の要件に従い、登録者は本報告書に正式に権限を付与された署名者により、登録者を代表して署名させた。
| Dated: August 3, 2023 | Immunic, Inc. | |
| By: | /s/ Daniel Vitt | |
| Daniel Vitt | ||
| Chief Executive Officer | ||

イミュニック・インク2023年第2四半期決算報告と最新情報のお知らせ
– ビドフルジムス・カルシウムが強力なNurr1活性化剤として多発性硬化症の神経保護ポテンシャルを強化する前臨床試験データがJournal of Medicinal Chemistry誌に掲載される-。
– imu-856のセリアック病を対象とした臨床第1b相試験の良好な結果は、腸管構造の再生を促進することにより消化器疾患を治療する新しい治療アプローチの概念実証となる - (英語)。
– 進行性多発性硬化症を対象としたビドフルジムス・カルシウムの第2相臨床試験CALLIPERの中間結果は2023年秋に期待される-。
- 7,730万ドルの現金、現金同等物および投資により、2024年第4四半期までイミュニック社の資金を賄う見込み-。
– 本日8月3日午前8時(米国東部時間)よりウェブキャストを実施。
ニューヨーク発、2023年8月3日 - 慢性炎症性疾患および自己免疫疾患に対する経口低分子治療薬の臨床パイプラインを開発中のバイオテクノロジー企業、イムニック・インク(Nasdaq: IMUX)は本日、2023年6月30日に終了した第2四半期の業績を発表し、企業最新情報を提供しました。
「イミュニックの最高経営責任者兼社長であるダニエル・ヴィット博士は、次のように述べています。「第2四半期には、最先端医薬品候補であるビドフルジムス・カルシウム(IMU-838)およびIMU-856を含む、当社の2つの主要パイプライン・プログラムから、重要な臨床データおよび前臨床データが報告されました。「重要なことは、ビドフルジムス・カルシウムが強力な核内受容体関連1(Nurr1)活性化因子として作用することを示す前臨床エビデンスが査読付きジャーナル・オブ・メディシナル・ケミストリーに掲載されたことです。本年秋には、進行性MSを対象とした第2相CALLIPER試験の中間バイオマーカー解析を報告する予定であり、これはビドフルジムス・カルシウムの神経保護作用を裏付けるもので、MS市場における差別化要因となる可能性があります。これまでのところ認められている実質的な臨床活性に加え、すでに知られている良好な安全性と忍容性のプロファイルに基づき、ビドフルジムス・カルシウムがMSの多面的な病態生理を管理するためのユニークな治療アプローチとなる可能性があることを確信しています。
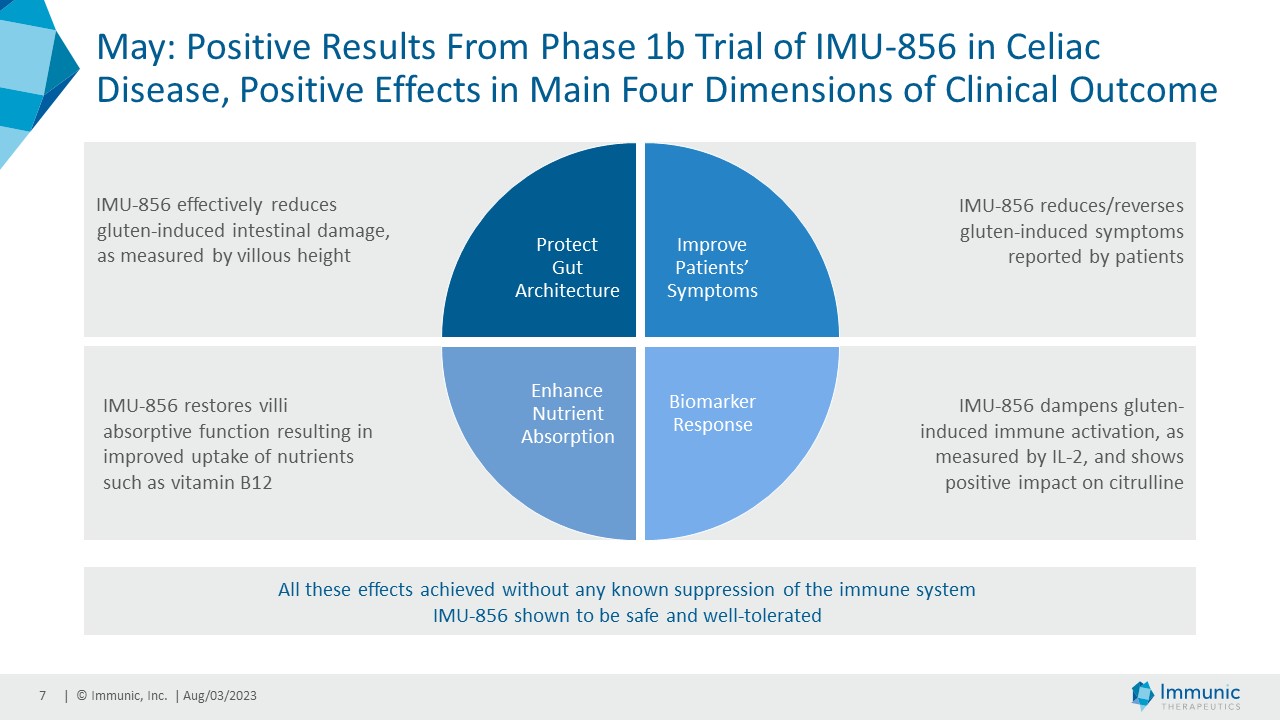
5月には、セリアック病患者を対象としたIMU-856の第1相臨床試験のパートCから、予想を上回る良好な結果が報告され、前臨床で観察されたように、腸壁を再生するIMU-856の能力が初めて臨床的に証明されました。特に第1b相試験では、IMU-856がプラセボと比較して、セリアック病の組織像、症状、バイオマーカー、栄養吸収という4つの重要な側面の改善に有効であることが示されました。続いて、Digestive Disease Weekにおいて、IMU-856の分子作用機序が、腸壁の構造の回復と再生に働くサーチュイン6(SIRT6)の強力なモジュレーターであることが発表されました。その結果、現在、IMU-856の活性を示唆する臨床エビデンスが得られており、様々な消化管疾患を新たな治療アプローチで治療できる可能性があります。これらの知見に基づき、進行中の活動性セリアック病(OACD)を対象とした第2相臨床試験の準備が現在進行中です。"

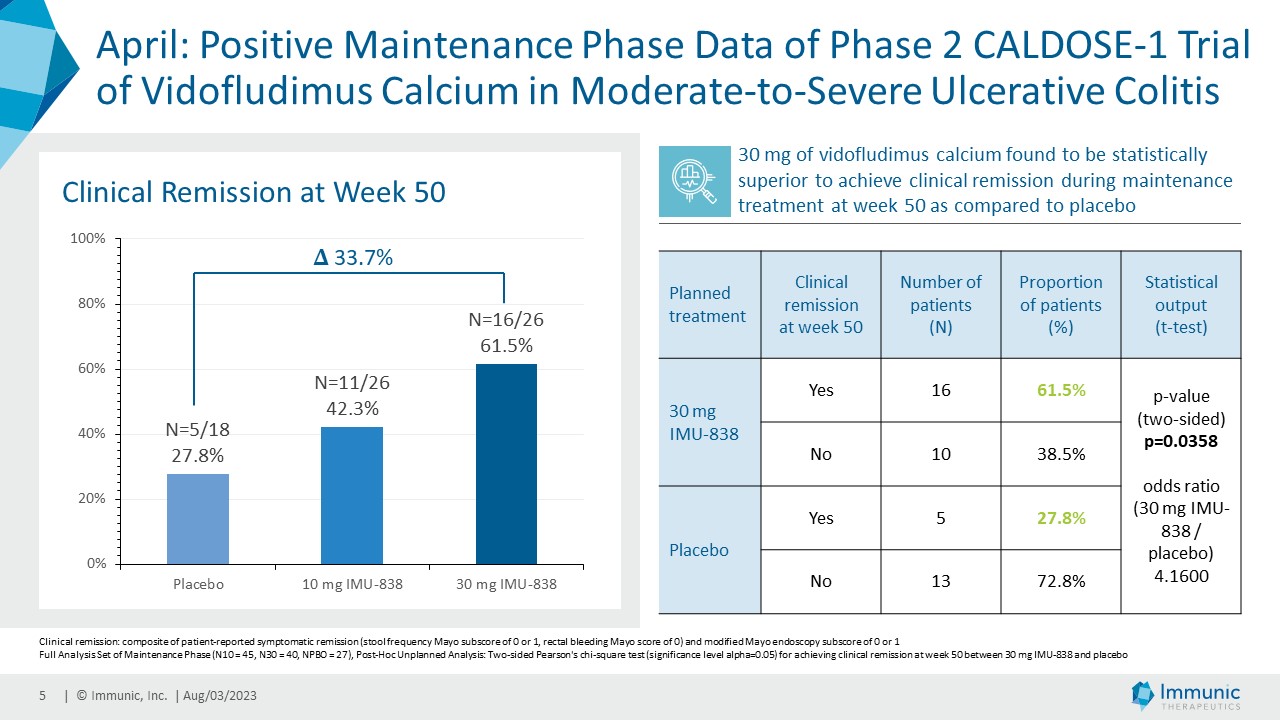
「当四半期に発表された中等症から重症の潰瘍性大腸炎(UC)患者を対象としたビドフルジムス・カルシウムのCALDOSE-1試験の維持相試験では、プラセボと比較して統計学的に有意な活性が示され、非常に有望な結果が得られました。さらに、このデータにより、ビドフルジムス・カルシウムの先行試験で認められた優れた安全性と忍容性プロファイルが再確認されました」とヴィット博士は結論づけた。
2023年第2四半期以降のハイライト
| · | 2023年7月セリアック病専門家によるバーチャルドル卓会議を開催し、新たな治療法に対するアンメット・メディカル・ニーズの高さについて議論した。また、最近発表されたセリアック病患者を対象とした第1b相臨床試験の良好な結果を含め、IMU-856プログラムの概要を説明した。 |
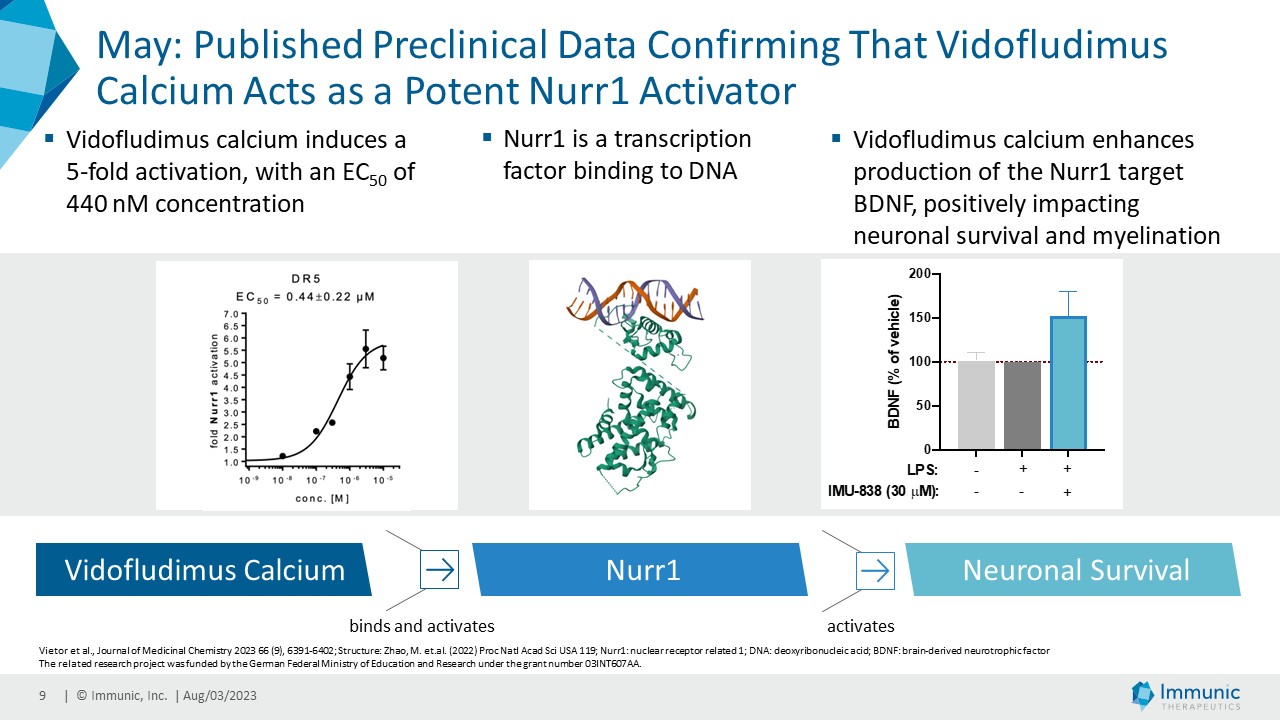
| · | 2023年5月ビドフルジムスカルシウムが、ジヒドロオロテートデヒドロゲナーゼ(DHODH)阻害剤としての既知の作用機序に加えて、強力なNurr1活性化剤として作用することを確認した前臨床データを、査読付きで高い影響力を持つJournal of Medicinal Chemistry誌に「Development of a potent Nurr1 agonist tool for in vivo applications」と題する論文で発表した。データは、Nurr1の活性化が、この薬剤の神経保護作用の原因である可能性を示し、以前に報告されたMS患者における確認された障害悪化事象の減少に寄与している可能性を示した。 |
| · | 2023年5月2023年Digestive Disease Week(DDW)において、IMU-856の臨床データおよび前臨床データを発表。その中には、腸管バリア機能と腸管上皮の再生の転写制御因子として機能するタンパク質SIRT6の高選択的かつ強力な低分子モジュレーターとしての分子作用機序が初めて含まれる。 |
| · | 2023年5月セリアック病患者を対象としたIMU-856の第1相臨床試験パートCの良好な結果を発表。データは、セリアック病の病態生理の4つの主要な側面、すなわち腸管構造の保護、患者の症状の改善、バイオマーカー反応、栄養吸収の促進において、IMU-856がプラセボを上回る効果を示した。また、本試験においてIMU-856の安全性と忍容性が確認されました。このデータは、腸管構造の再生を促進することにより、消化管疾患に対する全く新しい治療法の最初の臨床的概念実証になるとイムニックは考えています。また、このデータは、前臨床試験で観察されたIMU-856の腸管細胞の適切な再生を再確立する能力が、セリアック病患者の臨床的利益につながるという最初の臨床的証拠を提供するものです。最も重要なことは、セリアック病に特異的に関与する免疫機構を標的とすることなく、グルテンによる破壊から腸絨毛を保護することが観察されたことである。 |
| · | 2023年4月2023年4月26日付で、多発性硬化症のオピニオンリーダーであり、臨床、学界、産業界で数十年の経験を持つリチャード・ルーディック医学博士を取締役に迎え、取締役会を強化。また、ヴィンセント・オシポウ博士が2023年6月28日付で取締役を退任することも発表。 |
| · | 2023年4月中等症から重症の潰瘍性大腸炎患者を対象としたビドフルジムス・カルシウムの第Ⅱb相CALDOSE-1試験の維持期の良好なデータを報告。データは、50週目においてプラセボと比較して臨床的寛解が用量直線的に増加したことを示した。探索的統計解析の結果、ビドフルジムスカルシウム30mg用量は、プラセボと比較して50週目の臨床的寛解達成において33.7%の絶対的改善率を示し、統計学的に優れていることが確認された(p=0.0358)。さらに、内視鏡的治癒の用量直線的な増加が観察され、ビドフルジムス・カルシウム30mg用量は、プラセボと比較して37.8%の絶対的改善と関連し、探索的統計解析においても統計学的有意性を示した(p=0.0259)。ビドフルジムスカルシウムの投与は安全で忍容性が高いことが確認された。 |

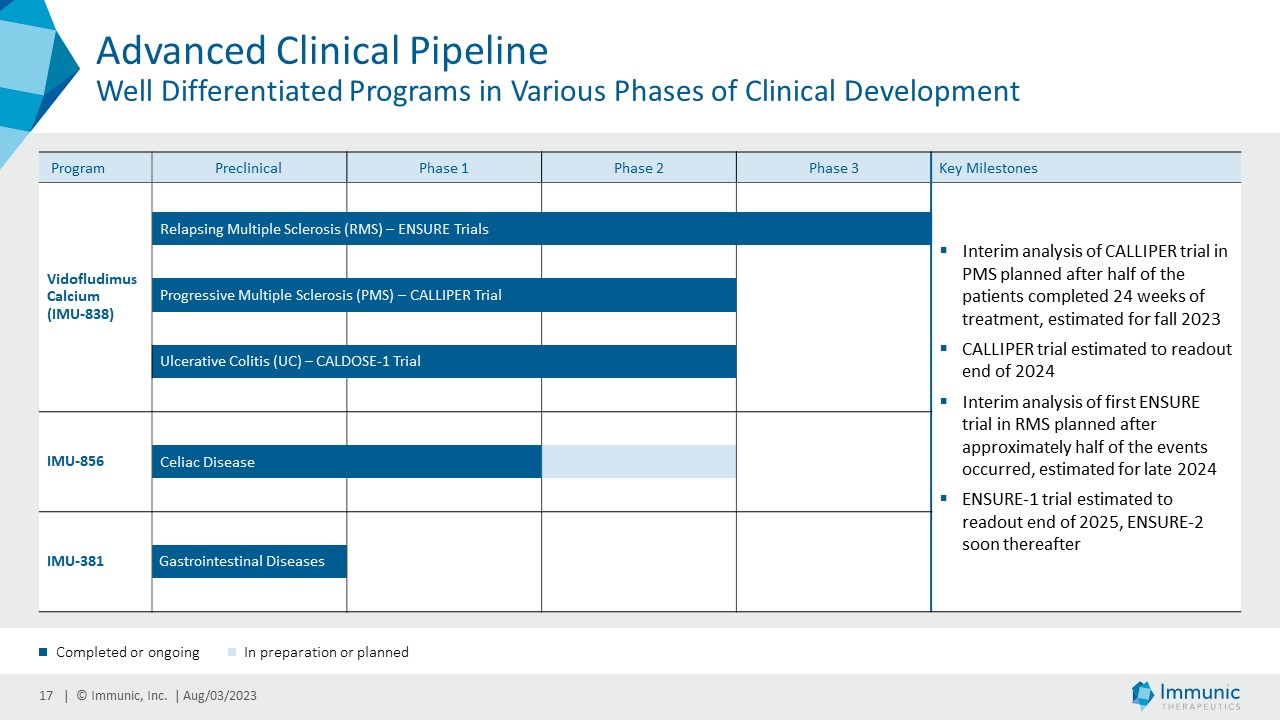
Anticipated Clinical Milestones
| · | MSにおけるビドフルジムスカルシウム:進行性MSを対象としたビドフルジムスカルシウムの第2相CALLIPER試験の中間解析データは、これまで2023年後半と案内されていたが、2023年秋に入手可能となる見込み。同試験のトップラインデータの読み出しは2024年末となる見込みである。ENSUREプログラムの中間解析データは2024年後半に、ENSURE試験の最初の読み出しは2025年末になると予想される。 |
| · | セリアック病におけるIMU-856セリアック病患者を対象としたグルテン除去食およびグルテンチャレンジ期間中のIMU-856の臨床第1b相試験の良好なデータに基づき、同社はOACD患者を対象としたIMU-856の臨床第2相試験の準備を積極的に進めている。 |
財務および営業成績
| · | 研究開発(R&D)費は、2022年6月30日に終了した3カ月間の1,650万ドルに対し、2023年6月30日に終了した3カ月間は2,120万ドルでした。この470万ドルの増加は、(i)ビドフルジムス・カルシウムの再発性および進行性MSを対象とした進行中の臨床プログラムおよびIMU-856プログラムに関連した外部開発費の610万ドルの増加、(ii)人員増加に関連した研究開発における人件費の0.6百万ドルの増加(うち0.1百万ドルは現金支出を伴わない株式ベースの報酬によるもの)、(iii)多数のカテゴリーにわたる関連費用の0.7百万ドルの増加を反映している。この増加は、(i)潰瘍性大腸炎を対象としたビドフルジムス・カルシウムの第2相臨床試験に関連した外部開発費の140万ドルの減少、(ii)IMU-935乾癬プログラムに関連した130万ドルの減少により一部相殺された。 |
2023年6月30日に終了した6カ月間の研究開発費は4,410万ドル(前年同期は3,400万ドル)であった。この1,010万ドルの増加は、(i)再発性および進行性MSを対象としたビドフルジムス・カルシウムの進行中の臨床プログラムおよびIMU-856プログラムに関連した外部開発費の1,210万ドルの増加、(ii)人員増加に関連した研究開発における人件費の110万ドルの増加(うち0.2百万ドルは現金支出を伴わない株式ベースの報酬によるもの)、および(iii)多数のカテゴリーにわたる関連費用の0.5百万ドルの増加を反映している。この増加は、(i)潰瘍性大腸炎を対象としたビドフルジムス・カルシウムの第2相臨床試験に関連する外部開発費の200万ドルの減少、(ii)IMU-935乾癬プログラムに関連する160万ドルの減少により一部相殺された。
| · | 2023年6月30日に終了した3ヶ月間の一般管理費(G&A)は380万ドルで、2022年6月30日に終了した同期間は410万ドルであった。0.3百万ドルの減少は主に現金支出を伴わない株式報酬が0.4百万ドル減少したことによるもので、多くのカテゴリーにわたる費用の増加により相殺された。 |
2023年6月30日に終了した6ヵ月間の一般管理費は810万ドルであった(前年同期は80万ドル)。この110万ドルの増加は、主に(i)多くのカテゴリーにわたって0.6百万ドル増加したこと、(ii)主に現金支出を伴わない株式報酬の減少による一般管理部門の人件費の0.5百万ドルの減少により一部相殺されたことによるものである。

| · | 2023年6月30日に終了した3ヵ月間のその他の収益(費用)は、前年同期の(130万ドル)に対し、100万ドルであった。230万ドルの増加は主に、(i)為替差損が170万ドル減少したこと、(ii)金利上昇の結果受取利息が0.9百万ドル増加したこと、(iii)助成金受取額が0.1百万ドル増加したことによる。この増加は、オーストラリアにおける臨床試験への支出減少の結果、オーストラリアにおける臨床試験に対する研究開発税制優遇措置が0.4百万ドル減少したことにより一部相殺された。 |
2023年6月30日に終了した6ヵ月間については、その他の利益は、前年同期の(0.7百万ドル)に対し、3.0百万ドルであった。この370万ドルの増加は主に、(i)金利上昇に伴う受取利息の170万ドルの増加、(ii)為替差損の140万ドルの減少、(iii)ドイツ連邦財務省からの2021年度税制に帰属する研究引当金110万ドルの計上によるものである。この増加は、オーストラリアにおける臨床試験への支出が減少した結果、オーストラリアにおける臨床試験に対する研究開発税制優遇措置が0.5百万ドル減少したことにより一部相殺された。
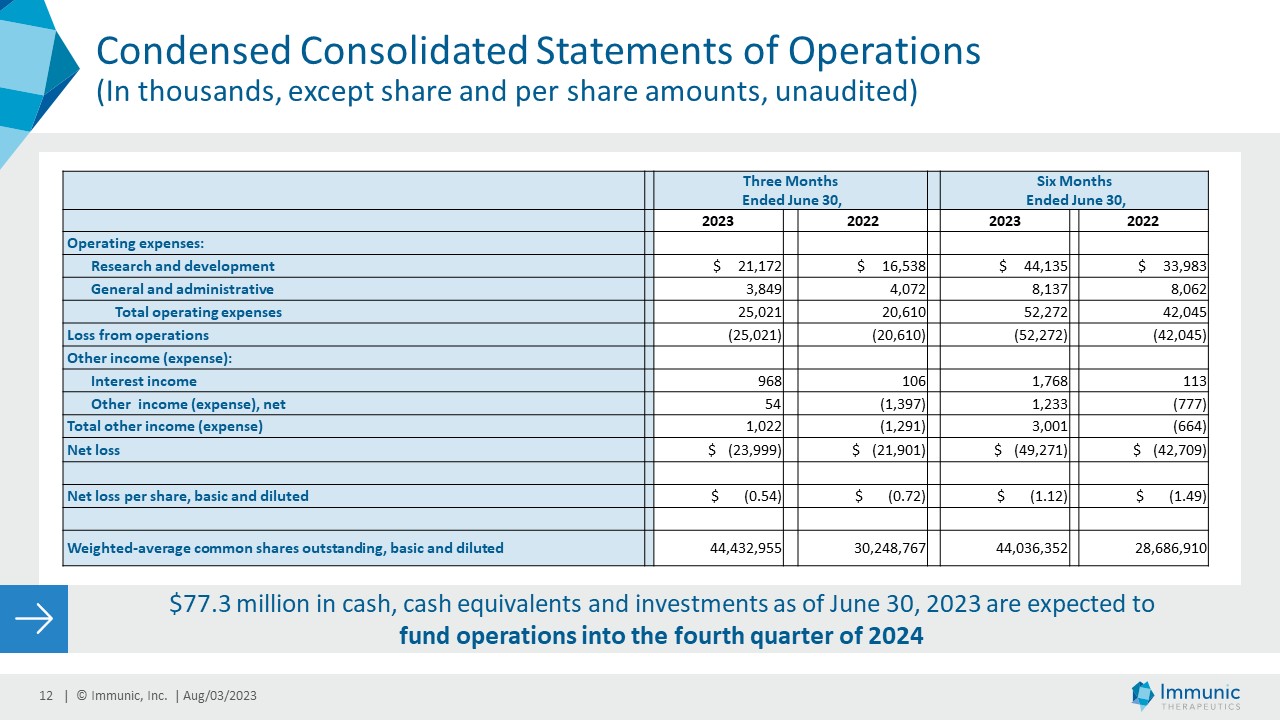
| · | 2023年6月30日に終了した3ヶ月間の純損失は約2,400万ドル、基本的および希薄化後1株当たり0.54ドルで、これに対し2022年6月30日に終了した同期の純損失は約2,190万ドル、基本的および希薄化後1株当たり0.72ドル、加重平均発行済み普通株式数44,432,955株ベースであった。 |
2023年6月30日に終了した6ヶ月間の純損失は約4,930万ドル(基本的および希薄化後1株当たり1.12ドル)であり、これに対して2022年6月30日に終了した同期の純損失は約4,270万ドル(基本的および希薄化後1株当たり1.49ドル)であった(加重平均発行済み普通株式数44,036,352株ベース)。
| · | 2023年6月30日現在の現金、現金同等物および投資は7,730万ドルであった。これらの資金により、イムニック社は2024年第4四半期までの運営資金を確保できる見込みである。 |
Webcast Information
イミュニックは本日午前8時(米国東部時間)よりウェブキャストを行います。ウェブキャストへの参加をご希望の方は、https://imux.zoom.us/webinar/register/WN_p1SCneOlThmUfjhnJ3AZ4g、またはイミュニックのウェブサイトir.imux.com/events-and-presentationsの「Events and Presentations」から事前にご登録ください。登録者には、オンライン参加用のリンクまたはダイヤルイン用の電話番号が記載された確認メールが送信されます。
ウェブキャストのアーカイブ再生は、終了後約1時間後にイミュニックのウェブサイト(ir.imux.com/events-and-presentations)にてご覧いただけます。

About Immunic, Inc.
イミュニック・インク(Nasdaq: IMUX)は、慢性炎症性疾患および自己免疫疾患に対する経口低分子治療薬の臨床パイプラインを開発しているバイオテクノロジー企業である。同社の主要開発プログラムであるビドフルジムス・カルシウム(IMU-838)は、現在、再発性多発性硬化症および進行性多発性硬化症の治療薬としてそれぞれ第3相臨床試験および第2相臨床試験を実施中であり、再発性多発性硬化症および中等度から重度の潰瘍性大腸炎を患う患者を対象とした第2相臨床試験では治療活性を示した。ビドフルジムス・カルシウムは、ジヒドロオロチン酸デヒドロゲナーゼ(DHODH)を選択的に阻害することにより、ファースト・イン・クラスの核内受容体関連1(Nurr1)活性化因子としてのメカニズムによる神経保護作用と、さらなる抗炎症作用および抗ウイルス作用を併せ持つ。サーチュイン6(SIRT6)というタンパク質を標的とするIMU-856は、腸のバリア機能を回復させ、腸上皮を再生させることを目的としており、セリアック病など多くの消化器疾患に応用できる可能性があり、現在第2相臨床試験の準備中である。現在前臨床試験中のIMU-381は、消化器疾患のニーズに特化して開発中の次世代分子である。詳細はwww.imux.com。
将来の見通しに関する記述についての注意事項
本プレスリリースには、1995年米国私募証券訴訟改革法が定めるセーフハーバーの目的上、重大なリスクと不確実性を伴う「将来の見通しに関する記述」が含まれています。本プレスリリースに含まれる、戦略、将来の事業、将来の財政状態、将来の収益、予測費用、現金の充足、予想される時期、臨床試験の開発および結果、見通し、計画、経営陣の目標に関する記述は、過去の事実に関する記述を除き、すべて将来の見通しに関する記述です。このような記述の例としては、イミュニックの開発プログラムおよび対象疾患に関する記述、イミュニックの開発プログラムが対象疾患を安全かつ効果的に治療できる可能性に関する記述、イミュニックの開発プログラムに関する前臨床および臨床データ、現在および将来の臨床試験の実施時期および予想される臨床マイルストーン、イミュニックの性質、戦略、重点事項およびこれらに関する今後の更新情報、イミュニックの製品候補の開発および商業的可能性、イミュニックの予想される資金繰りなどが含まれますが、これらに限定されるものではありません。Immunicは、将来予想に関する記述で開示された計画を実際に達成したり、意図を実行したり、期待や予測を達成したりしない可能性があり、これらの将来予想に関する記述を過度に信頼すべきではありません。このような記述は経営陣の現在の予想に基づくものであり、重大なリスクと不確実性を伴います。COVID-19の流行、インフレの進行、ウクライナとロシアの紛争が計画中および進行中の臨床試験に及ぼす影響、将来の現金の利用を予測する能力に関連するリスクおよび不確実性、偶発的な将来の負債および事業運営に必要な準備金など(ただし必ずしもこれらに限定されない)、多くの要因の結果として、実際の結果および業績は、将来見通しに関する記述で予測されたものとは大きく異なる可能性があります、事業目標および事業運営上の必要条件を満たすために十分な財務およびその他の資源の利用可能性、初期の前臨床試験および臨床試験の結果が将来の臨床試験結果を予測できない可能性があること、Immunic社の知的財産による保護および市場独占性、医薬品開発および規制当局の承認プロセスに関するリスク、競合製品および技術革新の影響。これらのリスク、不確実性およびその他の要因の詳細なリストおよび説明は、2023年2月23日にSECに提出された2022年12月31日終了会計年度の年次報告書(フォーム10-K)およびその後の証券取引委員会への提出書類の「リスク要因」の項に記載されています。これらの提出書類のコピーは、www.sec.gov または ir.imux.com/sec-filings からオンラインで入手できます。本リリースに記載されている将来の見通しに関する記述は、本リリースの日付時点におけるものです。Immunicは、これらの将来見通しに関する記述が作成された日以降に存在する事象や状況を反映するために、これらの将来見通しに関する記述を更新する意図や義務を否認します。イムニックは、本プレスリリースの一部または全部の内容に基づいてなされた、あるいはなされなかった行動に関する一切の責任を明示的に否認します。

Contact Information
イミュニック・インクジェシカ・ブリュー 投資家対応・広報部長 +49 89 2080 477 09 jessica.breu@imux.com
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧

会社開示情報をすべてご
会社開示情報をすべてご覧にな
会社開示情報をすべてご覧に
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要
(Unaudited)

会社開示情報をすべてご覧にな
会社開示情報をすべて
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要
(Unaudited)












 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン