シンダックス、2025年第3四半期決算と事業最新情報を発表
•
総収益は4,590万ドルで、25年第2四半期比21%の成長。
•
レブフォージ®(レブメニブ)の純収益は3,200万ドル。25年第3四半期のレブフォージ処方総数は第2四半期比25%増となり、旺盛な需要を示す。
•
Incyte社によるNiktimvo™(axatilimab-csfr)の純収入4,580万ドル、Syndax社による提携収入1,390万ドル。
– 2025年10月24日、レブフォージがR/R NPM1m AMLでFDA承認を取得
•
4億5,610万ドルの現金、現金同等物および投資により、同社は黒字化を達成する見込み。
•
本日午後4時30分(米国東部時間)より電話会議を開催。
ニューヨーク2025年11月3日(GLOBE NEWSWIRE) - 革新的ながん治療を進めるコマーシャルステージのバイオ医薬品会社シンダックス・ファーマシューティカルズ(Nasdaq: SNDX)は本日、2025年9月30日に終了した第3四半期の決算を報告し、事業の最新情報を提供した。
「第 3 四半期は、シンダックスにとって、商業的にもパイプラインの実行においても、またと も目覚ましい期間となりました。RevuforjとNiktimvoの需要は引き続き旺盛で、当四半期の売上高は合わせて7,500万ドルを超えました。「また、9月下旬にRevuforjがNCCNガイドラインのR/R NPM1m AMLに追加され、10月下旬にFDAの承認を取得したことで、メニン阻害における当社のリーダーシップはさらに強化されました。この2つ目の適応症への拡大が進行中であり、認知度の向上と需要の喚起に大きく前進しています。さらに、RevuforjとNiktimvoの両剤のフロントラインでの開発を進め、数十億ドル規模の可能性をさらに引き出していきます」。
最近のビジネスハイライトと今後のマイルストーン
Revuforj®(revumenib)
•
2025年第3四半期のRevuforj純収益は3,200万ドルを達成、2025年第2四半期比12%増。2025年第3四半期のRevuforj処方総数は約850件で、2025年第2四半期の処方総数より25%増加。
•
2025年10月24日、レブフォージは、満足な代替療法がない1歳以上の成人および小児患者におけるNPM1感受性変異を有するR/R型急性骨髄性白血病(AML)の治療薬として、米国FDAの承認を取得した。レブフォルジは現在、NPM1変異を有するR/R急性骨髄性白血病とKMT2A転座を有するR/R急性白血病の両方に対してFDAが承認した最初で唯一の治療薬である。
•
2025年9月18日、レブメニブが米国国立総合がんネットワーク(National Comprehensive Cancer Network®)の腫瘍学診療ガイドライン(NCCN Guidelines®)に、R/R NPM1m AMLに対するカテゴリー2Aの推奨治療選択肢として追加されたことを発表しました。このガイドラインの更新は、2025年にブラッド誌に発表されたレブメニブのAUGMENT-101試験の良好な結果に基づいています。
•
第67回米国血液学会(ASH)年次総会において、3演題の口頭発表を含む12演題のレブメニブのデータがハイライトされることを発表しました。これらの演題では、R/R、フロントライン、幹細胞移植後など、複数の急性白血病サブタイプにおけるレブメニブの魅力的な結果が示されています。
•
NPM1mおよびKMT2Arの急性白血病を対象にレブメニブを評価する複数の臨床試験が、治療状況に応じて進行中である。これらの試験には以下が含まれる:
•
EVOLVE-2:集中的化学療法が適さない新規診断NPM1m AML患者を対象に、レブメニブとベネトクラックスおよびアザシチジンの併用療法を評価する極めて重要な第3相無作為化二重盲検プラセボ対照試験。本試験は、血液悪性腫瘍に対する新規治療法の研究において豊富な経験を有する主要な共同臨床試験グループであるHOVONネットワークと共同で実施される。
•
SAVE試験:NPM1m、KMT2Ar、NUP98rのいずれかの遺伝子変異を有する新規診断のR/R AMLまたは混合系急性白血病(MPAL)の小児および成人患者を対象に、レブメニブとベネトクラックスおよびデシタビン/セダズリジンの経口投与を併用する全例併用療法を評価する第1/2相試験。この試験はMDアンダーソンがんセンターの研究者により実施されている。新たに診断された患者の最初のコホートからのデータは、ASH2025年次総会で経口集中化学療法でハイライトされる予定である:新たにNPM1mまたはKMT2Arと診断された急性白血病患者を対象に、レブメニブと集中化学療法(7+3)の併用療法とレブメニブの維持療法を評価する2つの進行中の第1相試験。
•
両試験の予備データは、ASH2025年次総会で発表される予定である。
•
BEAT AML:NPM1mまたはKMT2ArのAMLと新たに診断された高齢者(60歳以上)を対象に、レブメニブとベネトクラックスおよびアザシチジンの併用療法を評価する第1相試験。本試験は、白血病リンパ腫協会のBeat AML® Master Clinical Trialの一環として実施されている。
•
がんを突破するレブメニブとベネトクラックスの併用によりAML患者のMRDが消失し、無増悪生存期間が延長するかどうかを検討する第2相試験。この試験は、米国の主要ながん研究センターが協力しているBreak Through Cancerによって実施されている。
•
INTERCEPT:AMLのMRDと早期再発を標的としたレブメニブを含む新規治療法の使用を評価する第1相試験。本試験は、INTERCEPT AMLマスター臨床試験の一環としてAustralasian Leukaemia and Lymphoma Groupにより実施されている。
•
REVEAL試験と呼ばれる、集中化学療法を受けるのに適したNPM1mまたはKMT2A再配列AMLの新規診断急性白血病患者を対象に、レブメニブと標準治療レジメンの併用を評価する2つの試験の立ち上げ活動が進行中で、2025年末までに試験開始が予定されている。
•
当社は、R/R転移性マイクロサテライト安定(MSS)大腸癌(CRC)患者を対象にレブメニブを評価している。本試験のデータは2026年第1四半期に開催される学会で報告される予定である。
Niktimvo™ (axatilimab-csfr)
•
2025年第3四半期のNiktimvo純収益は4,580万ドルを達成、2025年第2四半期比27%増。シンダックスとインサイトはNiktimvoを共同販売しています。シンダックス社はNiktimvoの純商業利益の50%を計上しており、これは製品売上高から売上原価と商業費用を差し引いたものと定義されています。2025年第3四半期において、Niktimvoの製品貢献に対するシンダックスの取り分は、提携収入として計上され、1,390万ドルでした。
•
2025年ASH年次総会において、口頭発表3演題を含む11演題のアキサビリマブのデータが発表されることを発表。これらの演題は、再発性または難治性の慢性GVHDにおいてアキサビリマブが長期的なベネフィットをもたらす可能性と、新たに慢性GVHDと診断された患者におけるルキソリチニブとアキサビリマブの忍容性を強調するものです。
•
新たに慢性GVHDと診断された患者を対象に、アキサビリマブと標準治療との併用を評価する2つの試験が進行中である:
•
新たに慢性GVHDと診断された12歳以上の患者を対象に、アキサチリマブとルキソリチニブを併用する第2相非盲検無作為化多施設共同試験。
•
新たに慢性GVHDと診断された12歳以上の患者を対象に、アキサチリマブとコルチコステロイドを併用する、極めて重要な第3相無作為化二重盲検プラセボ対照多施設共同試験。
•
MAXPIReは、特発性肺線維症(IPF)患者を対象に標準治療に加えてアキサチリマブを投与する第2相26週間無作為化二重盲検プラセボ対照試験で、現在登録が進行中である。当社は、2025年末までに本試験への登録を完了し、2026年後半にトップラインデータを取得する予定である。
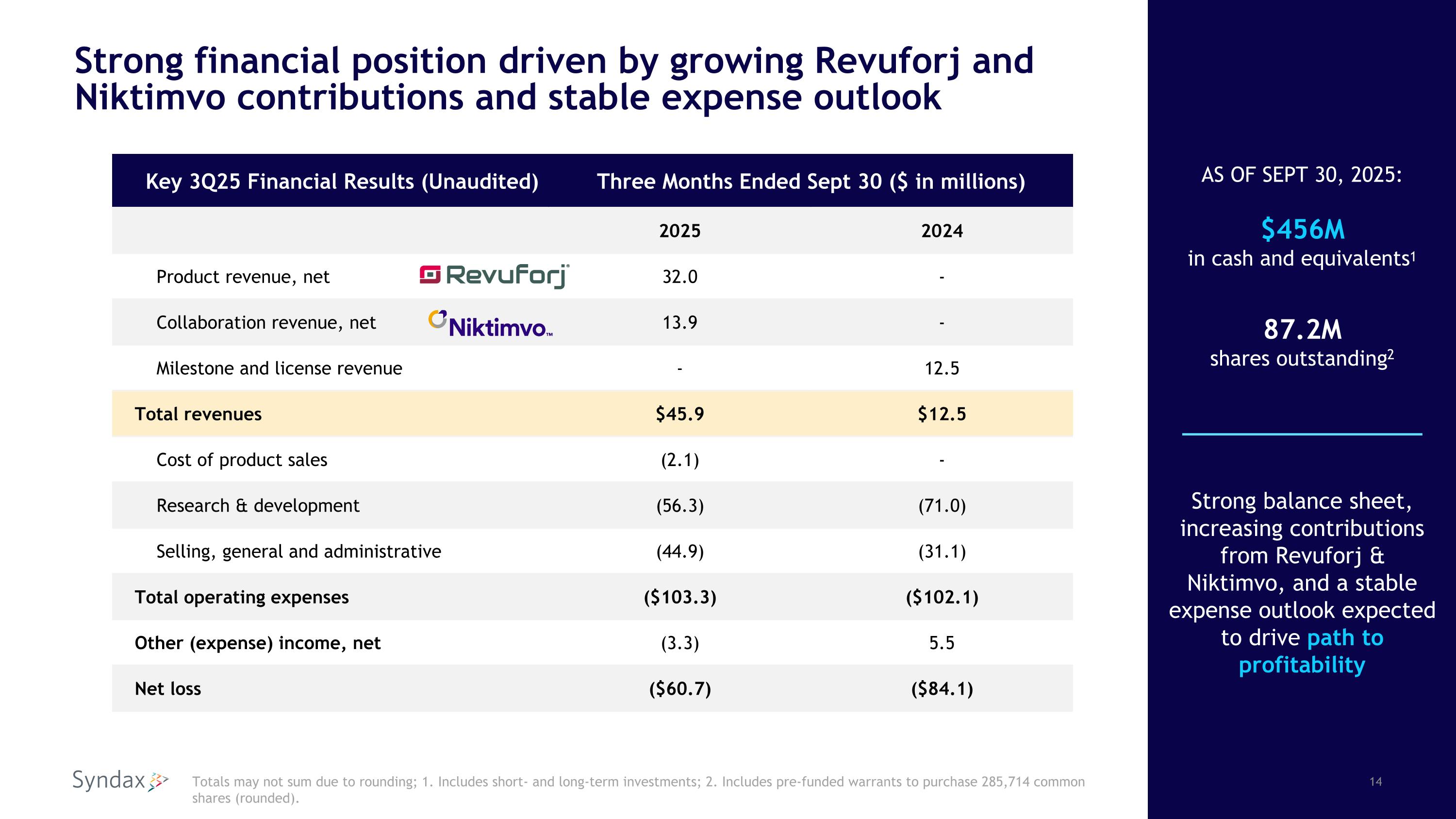
2025年第3四半期決算
2025年9月30日現在、シンダックスの現金、現金等価物、短期・長期投資は4億5610万ドル、発行済み普通株式とプレファンドワラントは8720万株であった。
2025年第3四半期の総収入は4,590万ドルで、内訳はRevuforj純収入3,200万ドル、Niktimvo提携収入1,390万ドル。この提携収入は、当社のパートナーであるIncyte社が以前に報告したNiktimvo純収入4,580万ドルから派生したものである。
シンダックスは、ニクティムボの純営業利益の50%を計上する。この純営業利益とは、(インサイテ社が計上した)純収入から売上原価と営業費用を差し引いたものと定義される。
2025年第3四半期の研究開発費は、前年同期の7,100万ドルから5,630万ドルに減少した。この減少は主に、ニクティムボの承認時に当社が支払うマイルストン支払額1,500万ドルが2024年第3四半期に発生し、2025年第3四半期には発生しなかったことによるものです。また、前期に進行中であったR/R NPM1m AMLを対象とした登録試験の完了によるレブメニブ関連費用の減少、および商業用在庫の資産化によるCMC費用の減少も減少に寄与しました。
2025年度第3四半期の販売費および一般管理費は、前年同期の3,110万ドルから4,490万ドルに増加した。この増加は主に、2025年第3四半期のRevuforjおよびNiktimvoの商業化に関連した商業費用、人件費および株式報酬費用の増加によるものです。
2025年9月30日に終了した3ヶ月間において、シンダックスは普通株主に帰属する純損失6,070万ドル(1株当たり0.70ドル)を計上した(前年同期の普通株主に帰属する純損失は8,410万ドル(1株当たり0.98ドル))。
Financial Guidance
2025年通年では、研究開発費と販売費および一般管理費の合計は、現金支出を伴わない株式報酬費用4,500万ドル(推定)を除いた予想で、事前のガイダンス3億7,000万ドルから3億9,000万ドルに対し、3億8,000万ドルから3億8,500万ドルになると予想している。
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開
会社開示情報をすべてご覧になるには株探プレミアムの登録が
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プ
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無
About Revuforj® (revumenib)
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアム
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミ
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示
会社開示情報をすべてご覧になるには株探プレミアムの登録
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必