UNITED STATES
SECURITIES AND EXCHANGE COMMISSION
WASHINGTON, D.C. 20549
FORM 8-K
現行レポート
1934年米国証券取引所法第13条または第15条(d)に基づき
報告日(最も古いイベントの報告日):2025年2月5日
Journey Medical Corporation
(憲章に明記された正確な登録者名)
| デラウェア | 001-41063 | 47-1879539 | ||
| (法人設立の州またはその他の管轄区域) | (Commission File Number) | (I.R.S. Employer Identification No.) |
9237 E Via de Ventura Blvd, Suite 105
Scottsdale, AZ 8525
(主たる事務所の所在地)
登録者の電話番号(市外局番を含む):(480) 434-6670
フォーム8-Kが、以下の規定のいずれかに基づく登録者の提出義務を同時に満たすことを意図している場合は、以下の該当するボックスにチェックしてください:
| ¨ | 証券法に基づく規則425に従った書面によるコミュニケーション(17 cfr 230.425) |
| ¨ | 取引所法の下でのルール14a-12(17 cfr 240.14a-12)に基づく資料の勧誘。) |
| ¨ | 取引所法の規則14d-2(b)に基づく開始前のコミュニケーション(17 cfr 240.14d-2(b)) |
| ¨ | 証券取引法の規則13e-4(c)に基づく開始前のコミュニケーション(17 cfr 240.13e-4(c)) |
| 法第12条(b)項に基づいて登録された証券: | ||
| Title of each class | Trading Symbol(s) | 登録されている各取引所の名称 |
| 普通株式 | DERM | The Nasdaq Capital Market |
登録者が1933年証券法規則405(本章230.405節)または1934年証券取引法規則12b-2(本章240.12b-2節)で定義される新興成長企業であるかどうかをチェックマークで示す。
Emerging growth company x
新興成長企業の場合、登録者が取引所法第13条(a)に従い提供される新規または改訂された財務会計基準に準拠するための延長された移行期間を使用しないことを選択した場合は、チェックマークで示す。¨
| Item 2.02. | 営業成績および財政状態。 |
2025年2月5日、ジャーニー・メディカル・コーポレーション(以下「ジャーニー・メディカル」)は、2024年12月31日現在、2030万ドルの現金および現金同等物があることを報告する見込みであると発表した。さらに、ジャーニー・メディカルは、2024年12月31日に終了する通期について、以前発表したガイダンスを再確認している:
| · | 製品純収入5500万~6000万ドル; |
| · | 販売費および一般管理費は3,900万~4,200万ドル。 |
| · | 研究開発費は800万ドルから1,000万ドルの範囲である。 |
これらの見積もりは、経営陣が現在入手可能な情報に基づいている。ジャーニー・メディカルの実際の業績は、ここに含まれる暫定的な推定結果と大きく異なることはないと予想される。本フォーム8-Kカレント・レポートに含まれる見積もりは、経営陣により作成されたものであり、経営陣の責任である。Journey Medicalの独立登録会計事務所は、見積もりに関して監査、検討、編集、またはいかなる手続きも行っておらず、これらに関して意見またはその他のいかなる形式の保証も表明していない。
本フォーム 8-K の項目 2.02 に記載された情報は提供されたものであり、改正 1934 年証券取引法第 18 条における「提出された」ものとはみなされず、また同条の義務の対象となるものでもありません。本フォーム8-Kに記載された情報は、1933年証券法(改正後)に基づくいかなる提出書類にも参照により組み込まれるものではありません。
| Item 8.01 | Other Events. |
2025年2月5日、Journey Medicalは、最近承認された皮膚科用製品であるEmrosi™(ミノサイクリン塩酸塩徐放カプセル40mg)(旧称DFD-29)の商業上市計画に関する最新情報を提供するための電話会議を開催します。この電話会議でJourney Medicalが発表するスライド・プレゼンテーションのコピーは、別紙99.1として本Current Report on Form 8-Kに添付されています。
| Item 9.01. | Financial Statements and Exhibits. |
(d) 出展物
以下の資料を添付する:
| Exhibit Number | Description | |
| 99.1 | 2025年2月5日付投資家向けプレゼンテーション。 | |
| 104 | inline extensible business reporting language (ixbrl)でフォーマットされたcover page interactive data file。 |
Forward-Looking Statements
本フォーム8-Kカレント・レポートには、1933年証券法第27条A(改正後)および1934年証券取引法第21条E(改正後)の意味における「将来の見通しに関する記述」が含まれる場合があります。以下および本フォーム8-Kに関するカレント・レポート全体を通じて使用される「当社」、「当社」、「当社」、および「当社の」という語は、ジャーニー・メディカルを指す場合があります。このような記述には、当社の成長戦略および製品開発プログラムに関する記述や、過去の事実ではないその他の記述が含まれますが、これらに限定されるものではありません。予想する」、「信じる」、「推定する」、「可能性がある」、「期待する」、「予定する」、「可能性がある」、「計画する」、「意図する」、「可能性がある」および類似の表現は、一般的に将来の見通しに関する記述を特定するためのものです。将来の見通しに関する記述は、経営陣の現在の予想に基づくものであり、当社の事業、経営成績、財務状況、株価に悪影響を及ぼす可能性のあるリスクや不確実性の影響を受けます。実際の結果が現在の予想と大きく異なる可能性のある要因には、以下のものが含まれます:当社の製品および製品候補は、時間とコストを要する規制および臨床試験の対象となり、その結果、開発または商業化が成功しない可能性があること、当社の売上の大部分は、第三者によるジェネリック医薬品の競合、競合他社の新製品の導入、または既存の競合製品の市場シェアの増加の対象となる可能性のある製品に由来しており、これらのいずれかが当社の営業利益に重大な悪影響を及ぼす可能性があること、当社は規制の厳しい業界で事業を行っており、将来の法規制や行政・行政措置が当社の事業に及ぼす影響を予測できないこと;当社の収益は主に当社の皮膚科用製品の販売に依存しており、そのような製品の販売に関連するいかなる後退も当社の業績を損なう可能性があること。当社製品のジェネリック医薬品メーカーとの競合を含め、競争により当社製品の商機と収益性が制限される可能性があること。当社製品が政府および第三者支払機関を含め、市場で広く受け入れられないリスクがあること。当社事業のいくつかの側面において第三者に依存していること。当社製品の特定、開発、買収または導入、および当社事業への統合を行う当社の能力に依存しており、その点で失敗する可能性があること;最近承認された製品であるエムロジおよび今後開発、導入または買収される製品候補の商業化の成功に依存すること;臨床医薬品の開発は、非常に高価で、時間がかかり、不確実であり、当社の臨床試験は、現在または将来の製品候補の安全性および有効性を十分に実証できない可能性があります。当社の競合他社は、当社と類似または同一の製品を開発し、商業化する可能性があります。当社の知的財産の保護に関するリスクおよび当社の技術および製品について十分な特許保護を維持できない可能性があります;コンピュータシステムの障害、サイバー攻撃、または当社もしくは第三者のサイバーセキュリティの欠陥が発生した場合における当社の事業および操業の損失、継続企業の前提に関する重要な疑義、大規模な公衆衛生問題、伝染病または流行病が当社の製品収益および将来の臨床試験に及ぼす影響;フォートレスは当社普通株式の議決権の過半数を支配しており、他の株主にとって不利益となる可能性があります。また、2023年12月31日を末日とする年度のForm 10-K年次報告書、その後のForm 10-Q報告書、および当社がSECに提出するその他の報告書のパートI、項目1A、「リスク要因」に記載されているその他のリスクもあります。当社は、法律で義務付けられている場合を除き、ここに記載されている将来見通しに関する記述の更新または修正を公表する義務または約束を明示的に否認し、1995年米国私募証券訴訟改革法(Private Securities Litigation Reform Act of 1995)に含まれる将来見通しに関する記述のセーフハーバーによる保護を主張します。
SIGNATURES
1934年証券取引法の要件に従い、登録者は本報告書に正式に権限を付与された署名者により、登録者を代表して署名させた。
| Journey Medical Corporation | ||
| (Registrant) | ||
| By: | /s/ Claude Maraoui | |
| Claude Maraoui | ||
| 最高経営責任者兼社長兼取締役 | ||
Date: February 5, 2025
Exhibit 99.1

1 | © 2025 Journey Medical Corporation.無断複写・転載を禁じます。EMROSI - U.S. COMMERCIAL PLAN CONFERENCE CALL February 5, 2025 2 | © 2025 Journey Medical Corporation.

All rights reserved. FORWARD - LOOKING STATEMENTS FORWARD - LOOKING STATEMENTS This press release may contain “forward - looking statements” within the meaning of Section 27A of the Securities Act of 1933, as amended, and Section 21E of the Securities Exchange Act of 1934, as amended. As used below and throughout this press release, the words “the Company”, “we”, “us” and “our” may refer to Journey Medical. Such statements include, but are not lim ite d to, any statements relating to our growth strategy and product development programs and any other statements that are not historical facts. The words “anticipate,” “believe,” “estimate,” “may,” “expect,” “will,” “could,” “project,” “intend ” a nd similar expressions are generally intended to identify forward - looking statements. Forward - looking statements are based on management’s current expectations and are subject to risks and uncertainties that could negatively affect our business, opera tin g results, financial condition and stock price. Factors that could cause actual results to differ materially from those curre ntl y anticipated include: the fact that our products and product candidates are subject to time and cost intensive regulation and cli nical testing and as a result, may never be successfully developed or commercialized; a substantial portion of our sales deri ve from products that may become subject to third - party generic competition, the introduction of new competitor products, or an inc rease in market share of existing competitor products, any of which could have a significant adverse impact on our operating income; we operate in a heavily regulated industry, and we cannot predict the impact that any future legislation or ad ministrative or executive action may have on our operations; our revenue is dependent mainly upon sales of our dermatology products and any setback relating to the sale of such products could impair our operating results; competition co uld limit our products’ commercial opportunity and profitability, including competition from manufacturers of generic versions of our products; the risk that our products do not achieve broad market acceptance, including by government and third - party payo rs; our reliance third parties for several aspects of our operations; our dependence on our ability to identify, develop, and acquire or in - license products and integrate them into our operations, at which we may be unsuccessful; the dependence of the su ccess of our business, including our ability to finance our company and generate additional revenue, on the successful commercialization of our recently approved product, Emrosi , and any future product candidates that we may develop, in - license or acquire; clinical drug development is very expensive, time cons uming, and uncertain and our clinical trials may fail to adequately demonstrate the safety and efficacy of our current or any future product candidates; our competitors could develop an d commercialize products similar or identical to ours; risks related to the protection of our intellectual property and our potential inability to maintain sufficient patent protection for our technology and products; our business and operations wou ld suffer in the event of computer system failures, cyber - attacks, or deficiencies in our or our third parties’ cybersecurity; the substantial doubt about our ability to continue as a going concern; the effects of major public health issues, epidemics or p and emics on our product revenues and any future clinical trials; our potential need to raise additional capital; Fortress contro ls a voting majority of our common stock, which could be detrimental to our other shareholders; as well as other risks described i n P art I, Item 1A, “Risk Factors,” in our Annual Report on Form 10 - K for the year ended December 31, 2023, subsequent Reports on Form 10 - Q, and our other filings we make with the SEC. We expressly disclaim any obligation or undertaking to release publicly any updates or revisions to any forward - looking statements contained herein to reflect any change in our expectations or any changes in events, conditions or circumstances on which any such statement is based, except as may be req uir ed by law, and we claim the protection of the safe harbor for forward - looking statements contained in the Private Securities Litigation Reform Act of 1995. TRADEMARKS This confidential presentation may contain trademarks, service marks, trade names and copyrights of other companies, which ar e t he property of their respective owners. Solely for convenience, some of the trademarks, service marks, trade names and copyrights referred to in this presentation may be listed without the TM, SM, © or ® symbols, but the Company will assert, to th e fullest extent under applicable law, the rights of the applicable owners, if any, to these trademarks, service marks, trade names and copyrights. MARKET & INDUSTRY DATA Projections, estimates, industry data and information contained in this presentation, including the size of and growth in key en d markets, are based on information from third - party sources and management estimates. Although the Company believes that its third party - sources are reliable, the Company cannot guarantee the accuracy or completeness of its sources. The Company's ma nagement estimates are derived from third - party sources, publicly available information, the Company's knowledge of its industry and assumptions based on such information and knowledge. The Company's management estimates have not been verified b y a ny independent source. All of the projections, estimates, market data and industry information used in this presentation involve a number of assumptions and limitations, and you are cautioned not to give undue weight to such informat ion . In addition, projections, estimates and assumptions relating to the Company's and its industry's future performance are necessarily subject to a high degree of uncertainty and risk due to a variety of factors, including, but not limited to, thos e d escribed above, that could cause future performance to differ materially from the Company's expressed projections, estimates and assumptions or those provided by third parties.

3 | © 2025 Journey Medical Corporation.無断複写・転載を禁じます。講演者とアジェンダ Claude Maraoui 創設者、社長兼最高経営責任者 - Emrosi - 差別化された臨床プロファイル - 市場機会 - 商業戦略 - 市場参入 - 財務最新情報 - 閉会挨拶 4 | © 2025 Journey Medical Corporation.

無断複写・転載を禁じます。エムロジーの商業的ハイライト ・エムロジーのFDA承認取得(2024年11月):予定通り、ファーストサイクル審査 ・プラセボと市場をリードする経口酒さ治療薬オラセア® の両方に優れる ・1650万人の米国人が酒さに苦しんでいる 1 ・エムロジーを標準治療にする可能性がある ・ジャーニーメディカルに皮膚科営業チームを設立 ・大きな売上と収益のレバレッジを生み出す可能性がある ・現金と将来の収益を生み出すアウト・ライセンスの機会 1.Wehausen , B., Hill, D. E, & Feldman, S. R. (2016).乾癬や酒さのほとんどの人は治療を受けていない:大規模な集団研究.Dermatology Online Journal, 22(7).

5 | © 2025 Journey Medical Corporation.無断複写・転載を禁じます。本日の講演者 Brian Prout マーケティング担当エグゼクティブ・ディレクター Claude Maraoui 創業者、社長兼CEO Joseph Benesch 最高財務責任者 Srinivas Sidgiddi, M.D. 研究開発担当バイス・プレジデント Louis Donati マーケット・アクセス担当ディレクター Andrew Zwible オペレーション担当バイス・プレジデント Robert Nevin 最高商務責任者 6 | © 2025 Journey Medical Corporation.

無断転載を禁じます。講演者とアジェンダ Srinivas Sidgiddi, M.D, Vice President, Research & Development - Commercial Highlights - Market Opportunity - Commercial Strategy - Market Access - Financial Update - Closing Remarks 7 | © 2025 Journey Medical Corporation.
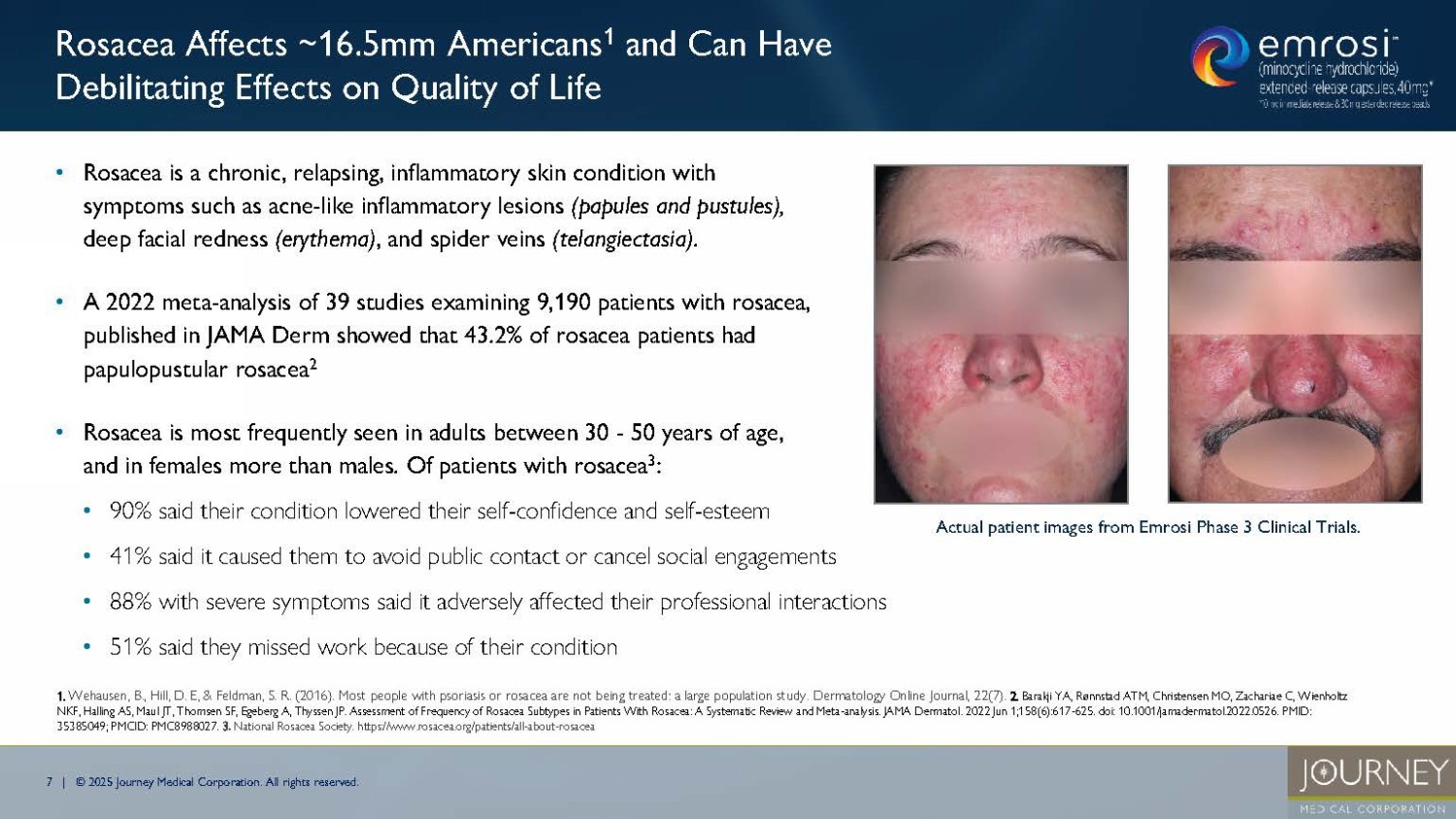
無断複写・転載を禁じます。酒さは、ニキビのような炎症性病変(丘疹や膿疱)、顔の深い赤み(紅斑)、クモ状静脈(毛細血管拡張症)などの症状を伴う、慢性で再発性の炎症性皮膚疾患である。- 2022年にJAMA Derm誌に発表された、酒さ患者9,190人を対象とした39の研究のメタ解析によると、酒さ患者の43.2%が丘疹性膿疱性酒さであった。酒さ患者のうち3 : - 90%が自分の症状が自信や自尊心を低下させたと回答 - 41%が人前での接触を避けたり、社会的な約束をキャンセルする原因になったと回答 - 症状が重い88%が仕事上の交流に悪影響を及ぼしたと回答 - 51%が自分の症状のために仕事を休んだと回答 1.Wehausen , B., Hill, D. E, & Feldman, S. R. (2016).乾癬や酒さのほとんどの人は治療を受けていない:大規模集団研究.Dermatology Online Journal, 22(7).2.Barakji YA, Rønnstad ATM, Christensen MO, Zachariae C, Wienholtz NKF, Halling AS, Maul JT, Thomsen SF, Egeberg A, Thyssen JP.酒さ患者における酒さサブタイプの頻度の評価:A Systematic Review and Meta - analysis.JAM A Dermatol.2022 Jun 1;158(6):617 - 625. doi : 10.1001/jamadermatol.2022.0526.pmid: 35385049; pmcid: pmc8988027.3 .https://www.rosacea.org/patients/all - about - rosacea エムロジ第3相臨床試験の実際の患者画像。
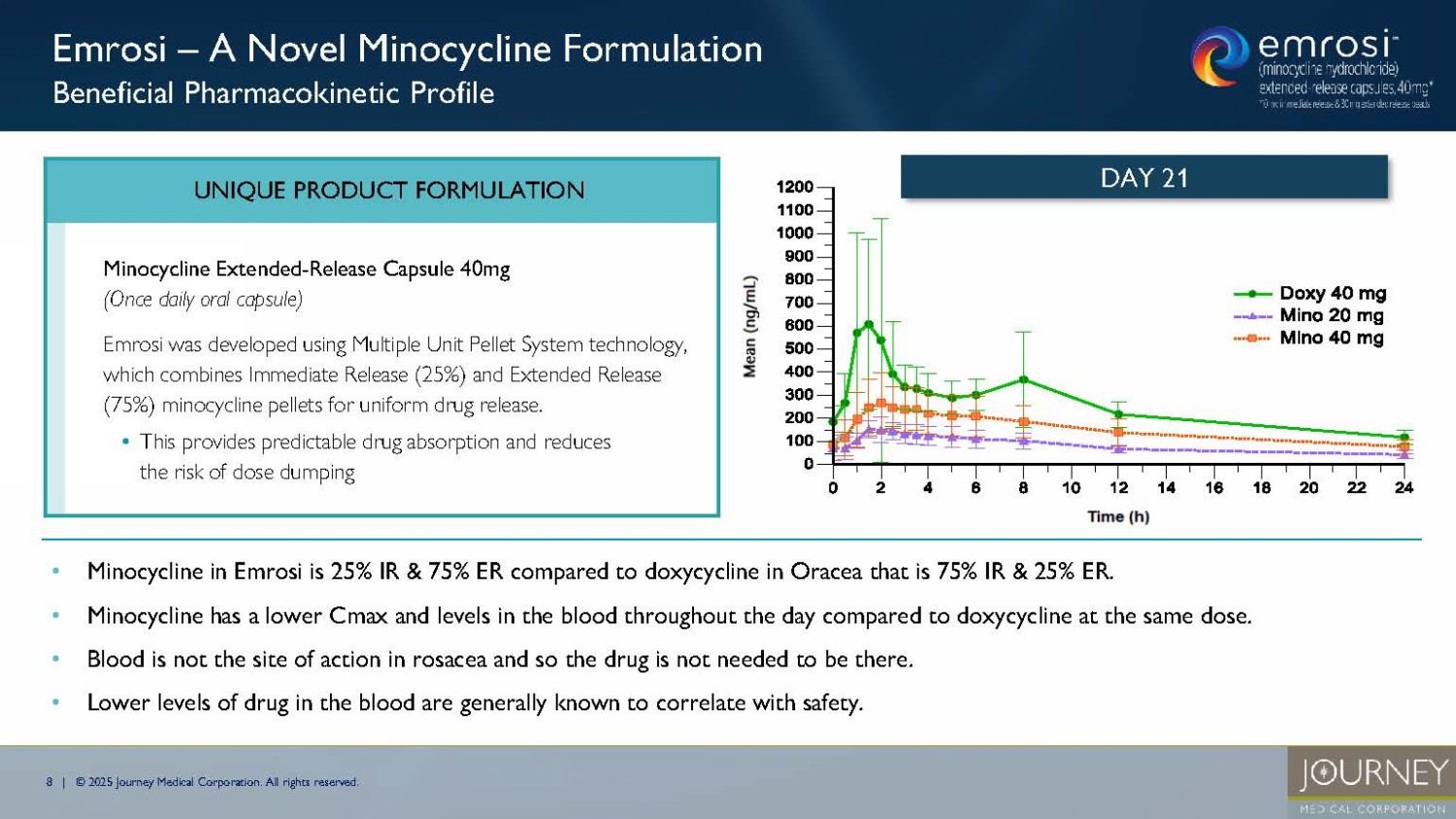
8 | © 2025 Journey Medical Corporation.無断複写・転載を禁じます。- エムロシに含まれるミノサイクリンは25%IRおよび75%ERであるのに対し、オラセアに含まれるドキシサイクリンは75%IRおよび25%ERである。- ミノサイクリンは、同用量のドキシサイクリンと比較して、Cmaxが低く、1日を通して血中濃度が高い。- 酒さでは血液は作用部位ではないので、薬剤が血液に存在する必要はない。- 血中薬物濃度の低下は一般的に安全性と相関することが知られている。エムロシ - 新規ミノサイクリン製剤 有用な薬物動態プロファイル 0 100 200 300 400 500 600 700 800 900 1000 1100 1200 0 2 4 6 8 10 12 14 16 18 20 22 24 Doxy 40 mg Mino 20 mg Mino 40 mg Day=21 DAY 21 0 100 200 300 400 500 600 700 800 900 1000 1100 1200 0 2 4 6 8 10 12 14 16 18 20 22 24 Doxy 40 mg Mino 20 mg Mino 40 mg Day=21 ユニークな製品処方 ミノサイクリン徐放カプセル40mg(1回投与)。放出カプセル 40mg(1日1回経口カプセル) エムロシは、マルチプルユニットペレットシステム技術を使用して開発されました、エムロジは、均一な薬物放出のために、即時放出(25%)と徐放(75%)のミノサイクリンペレットを組み合わせたマルチプルユニットペレットシステム技術を用いて開発されました。- これにより、予測可能な薬物吸収が得られ、用量ダンピングのリスクが軽減されます。

無断複写・転載を禁じます。エムロジ - 効能・効果および用法・用量 1日1回、食事の有無にかかわらず、いつでも服用可能 ミノサイクリン経口剤の承認最低用量(承認されている抗生物質の用量よりはるかに低い) 体重に依存しない固定用量 ラベルには、オラセアに対する優越性データが記載されている。有効性は、65歳以上を含むすべての成人年齢層で同様である。
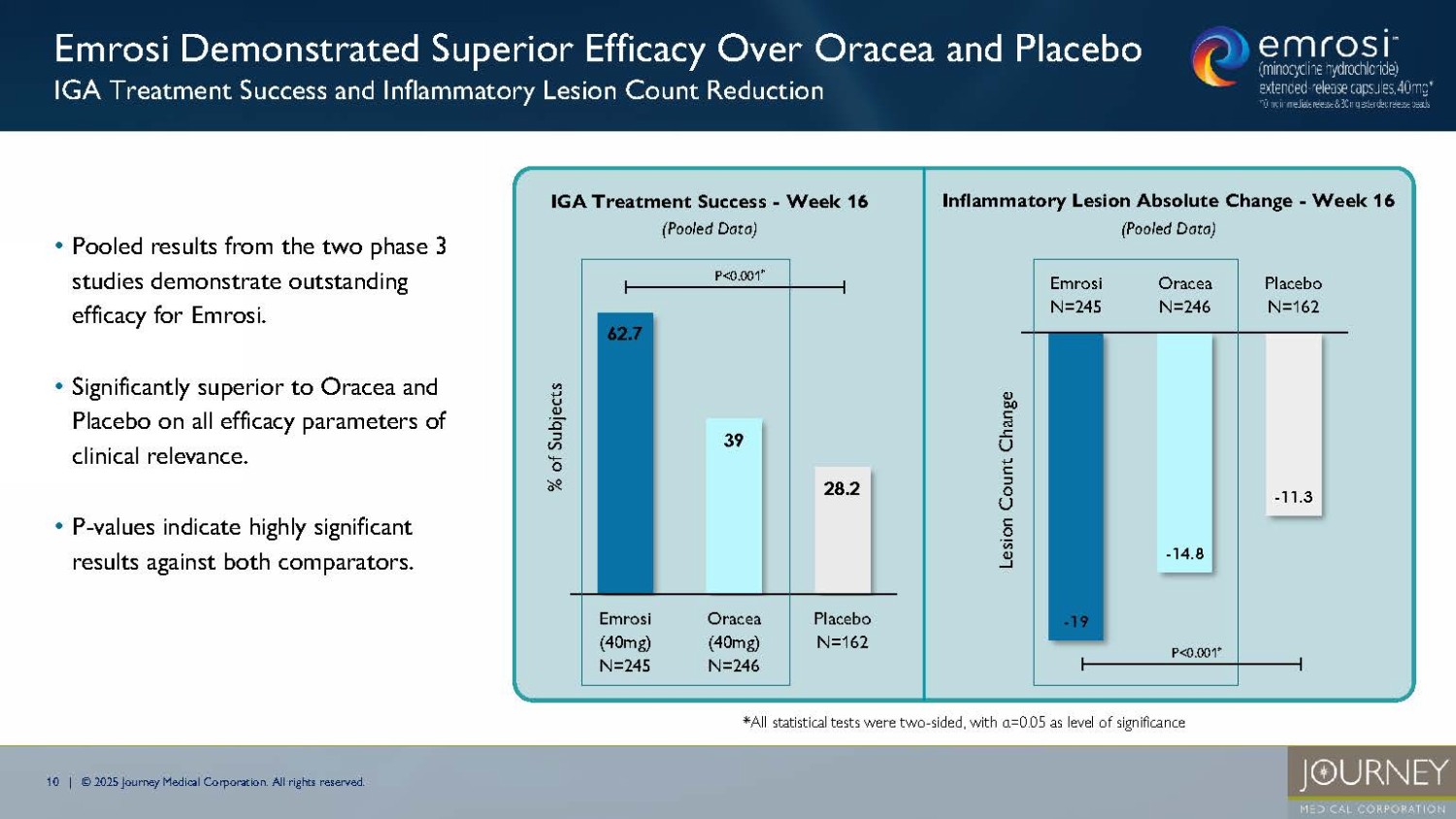
無断複写・転載を禁じます。62.7 39 28.2 エムロシ(40mg) N=245 オラセア(40mg) N=246 プラセボ N=162 被験者比 - 2つの第3相試験のプール結果は、エムロシの卓越した有効性を示している。- 臨床的に重要なすべての有効性パラメータにおいて、オラセアおよびプラセボより有意に優れている。- P-値は両比較対象に対して非常に有意な結果を示す。*エムロシはオラセアおよびプラセボよりも優れた有効性を示した IGA治療成功率および炎症性病変数減少率 IGA治療成功率-第16週(プールデータ) 炎症性病変絶対変化率-第16週(プールデータ) P<0.001 * - 19 - 14.8 - 11.3 Emrosi N=245 Oracea N=246 Placebo N=162 Lesion Count Change P<0.001 * 11 | © 2025 Journey Medical Corporation.
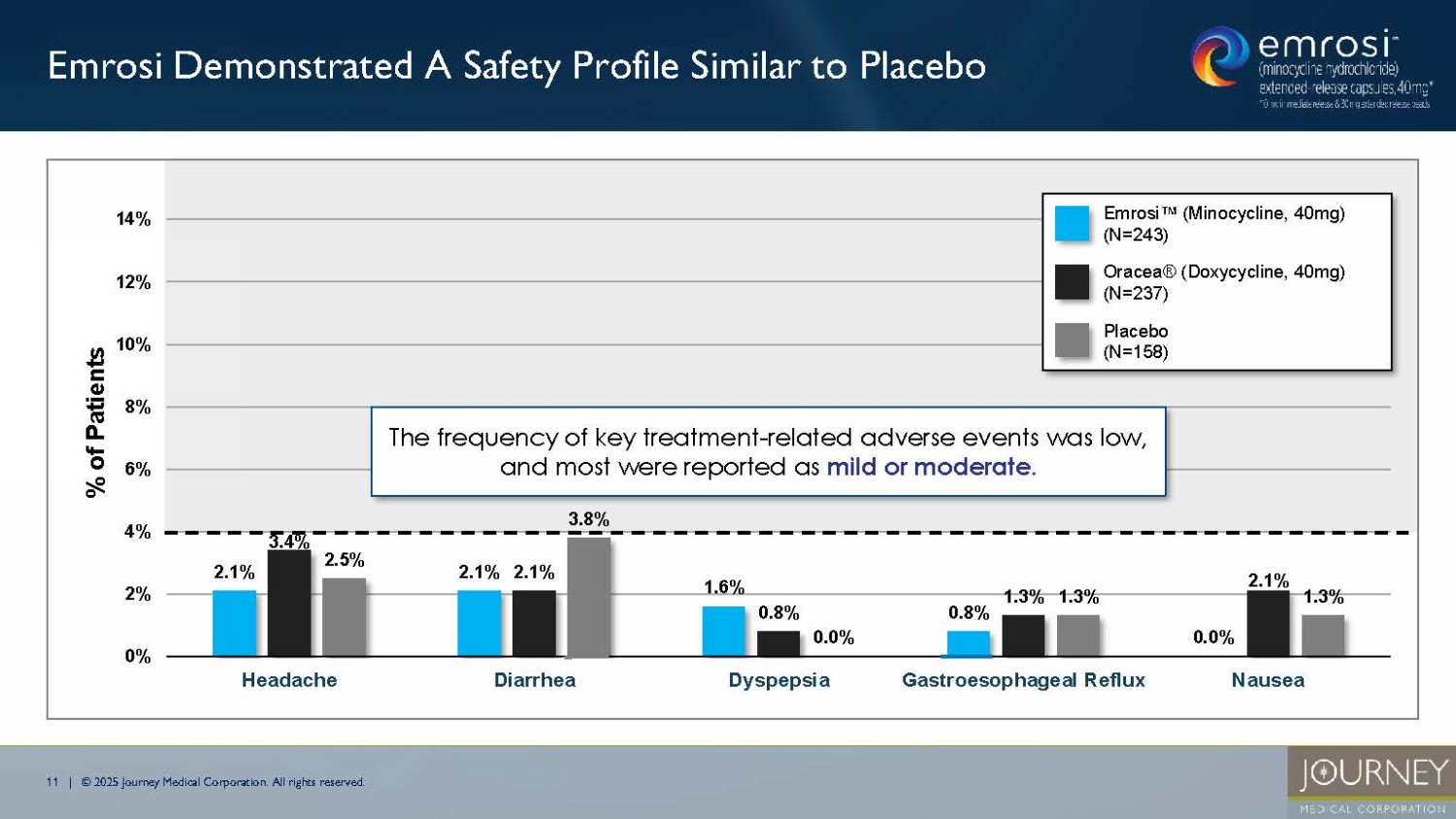
無断転載を禁じます。主な治療関連有害事象(N=638) 2.1% 2.1% 1.6% 0.8% 0.0% 3.4% 2.1% 0.8% 1.3% 2.1% 2.5% 3.8% 0.0% 1.3% 1.3% 0% 2% 4% 6% 8% 10% 12% 14% 頭痛 下痢 胃食道逆流 吐き気 エムロシ(ミノサイクリン、40mg)(N=243) オラセア®(ドキシサイクリン、40mg)(N=237) プラセボ(N=158) 主要な治療関連有害事象の発現頻度は低く、ほとんどが軽度または中等度であった。エムロシはプラセボと同様の安全性プロファイルを示した 12|© 2025 Journey Medical Corporation.

無断転載を禁じます。- 以下のトピックについて、主要な査読付きジャーナルに3本の原稿を投稿中である:- 臨床ポスターは、主要な皮膚科学会で臨床データの重要な側面を伝える予定である:PK安全性試験(秋季臨床;2023年10月) サブ-抗菌性試験(AAD;2024年3月) QoL改善(DEF NP/PA;2024年7月) エムロシとオラセアの全身性対皮膚性PK(秋季臨床;2024年10月) QoL改善(冬季臨床;2025年2月にアンコール発表予定) x x x x x エムロシ-出版とデータコミュニケーション計画 13 | © 2025 Journey Medical Corporation.

無断転載を禁じます。講演者とアジェンダ Andrew Zwible オペレーション担当副社長 - 商業ハイライト - Emrosi - 差別化された臨床プロファイル - 商業戦略 - 市場参入 - 財務最新情報 - 閉会挨拶 14 | © 2025 Journey Medical Corporation.
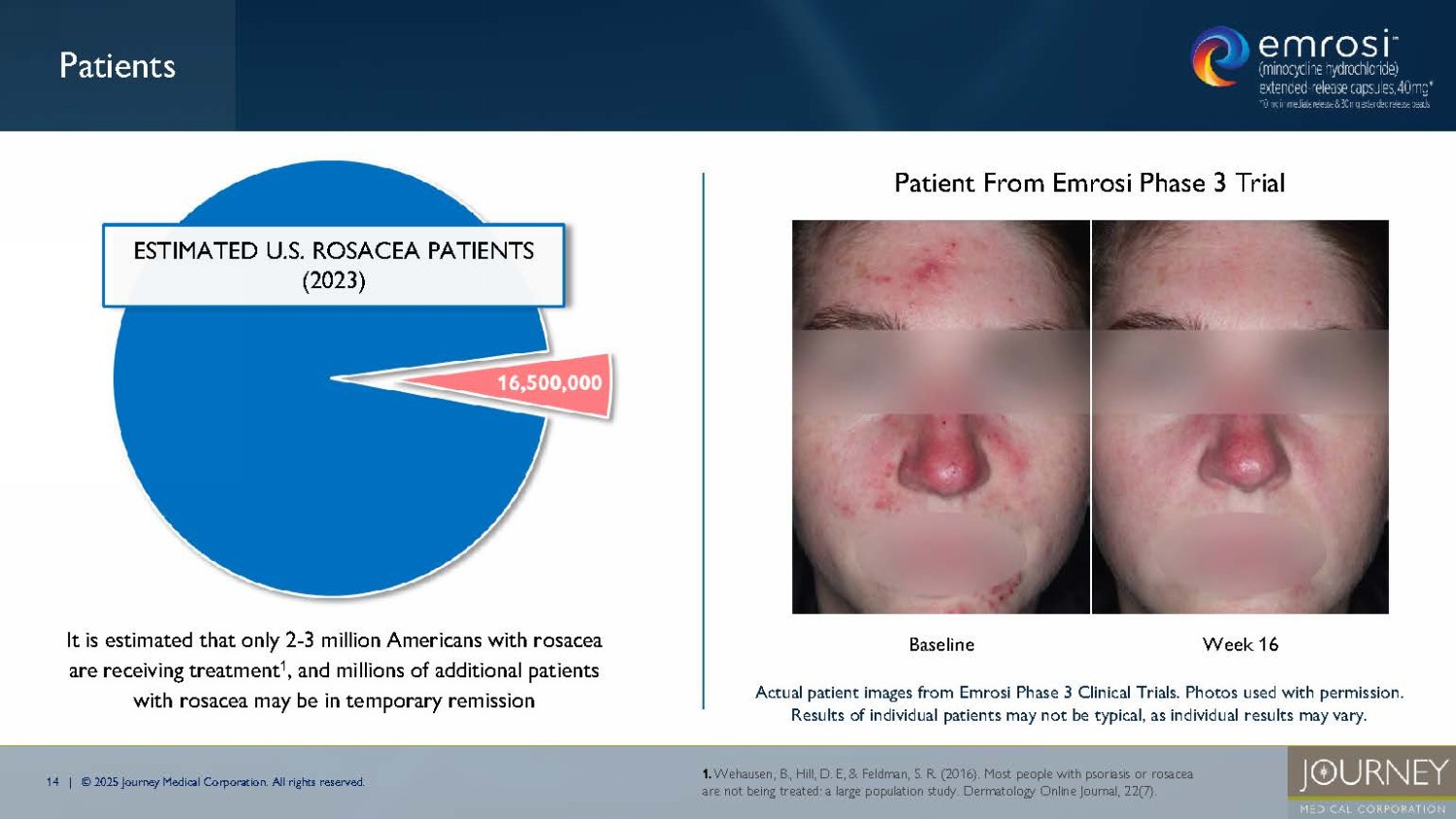
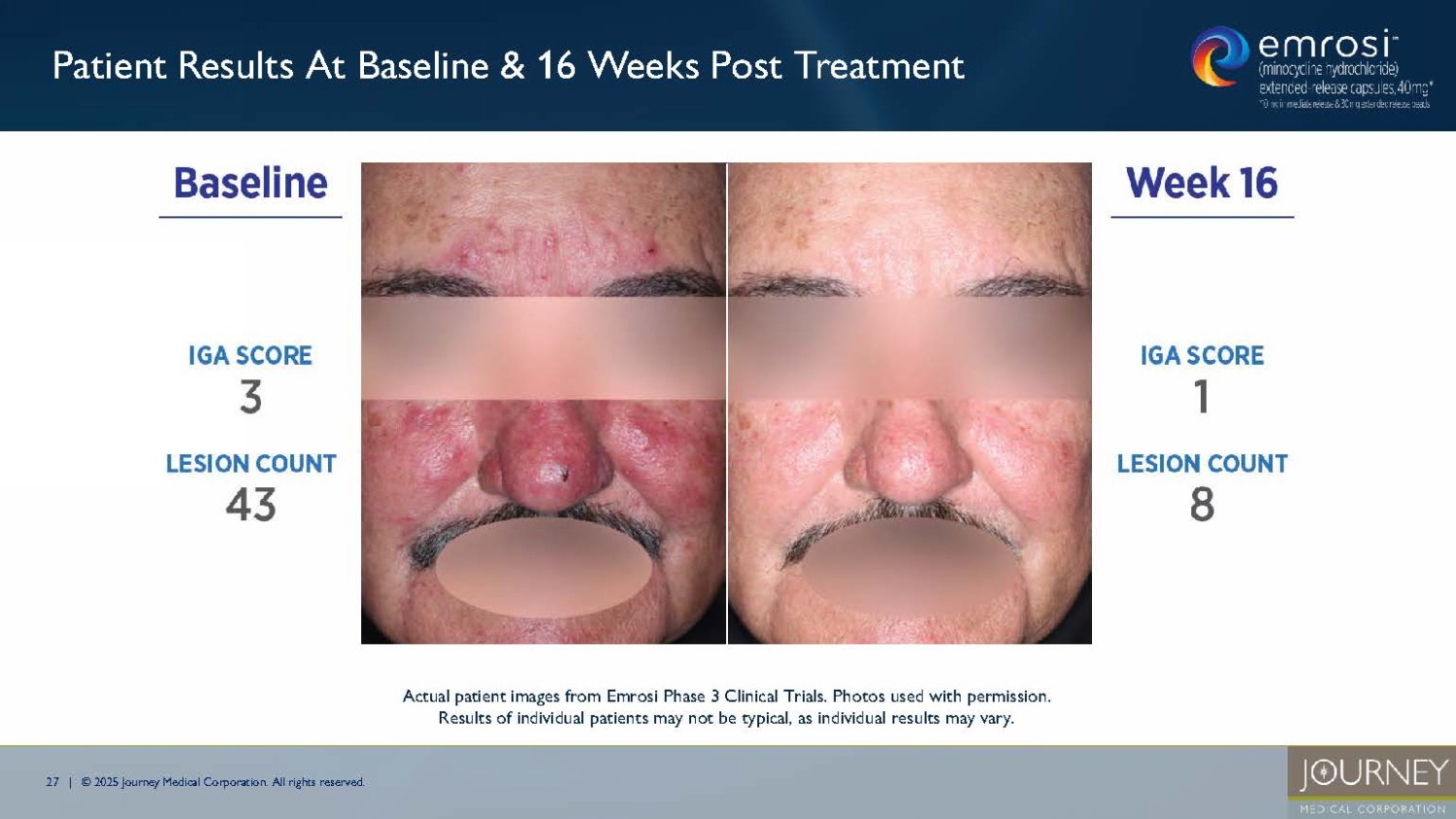
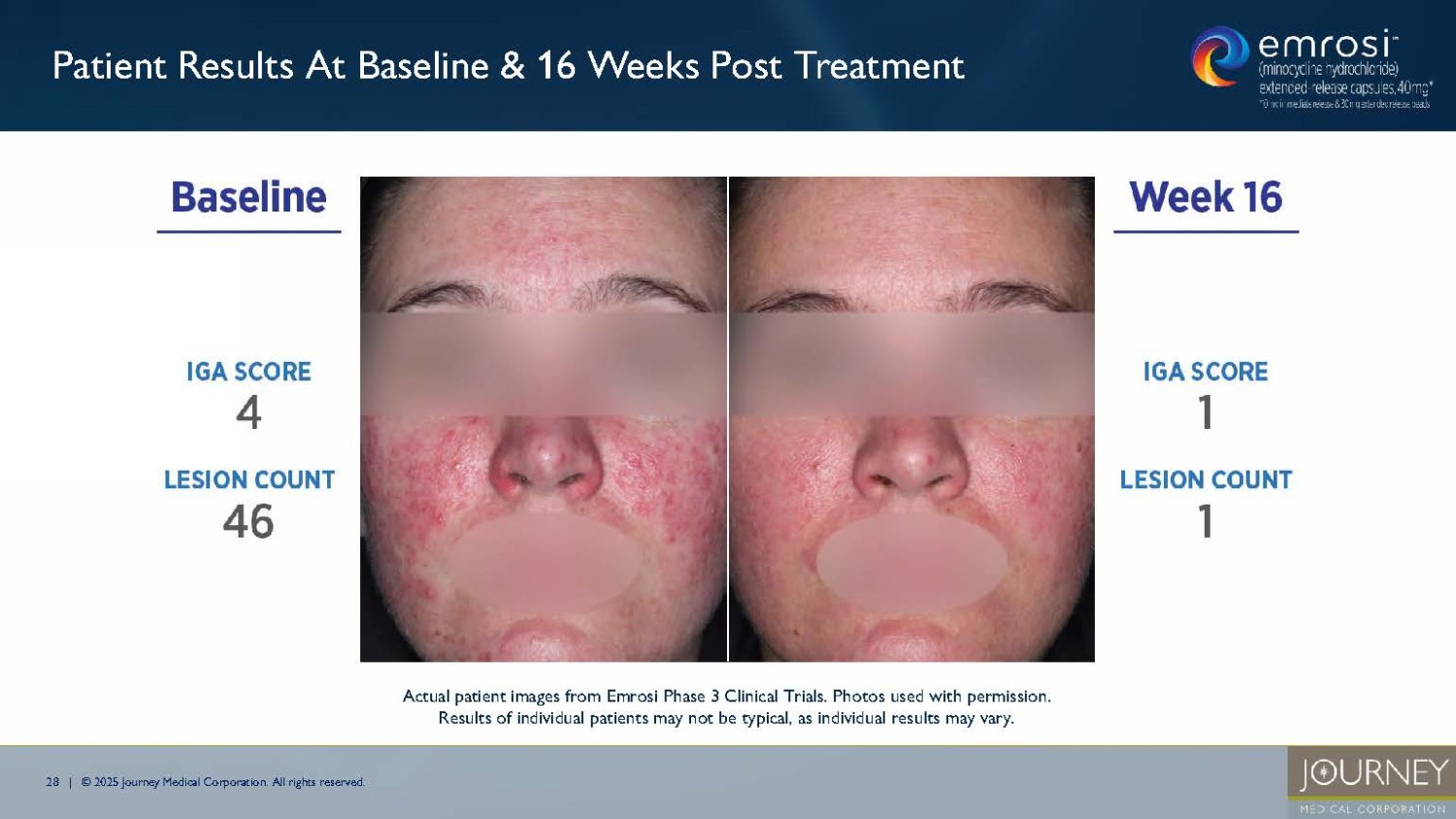
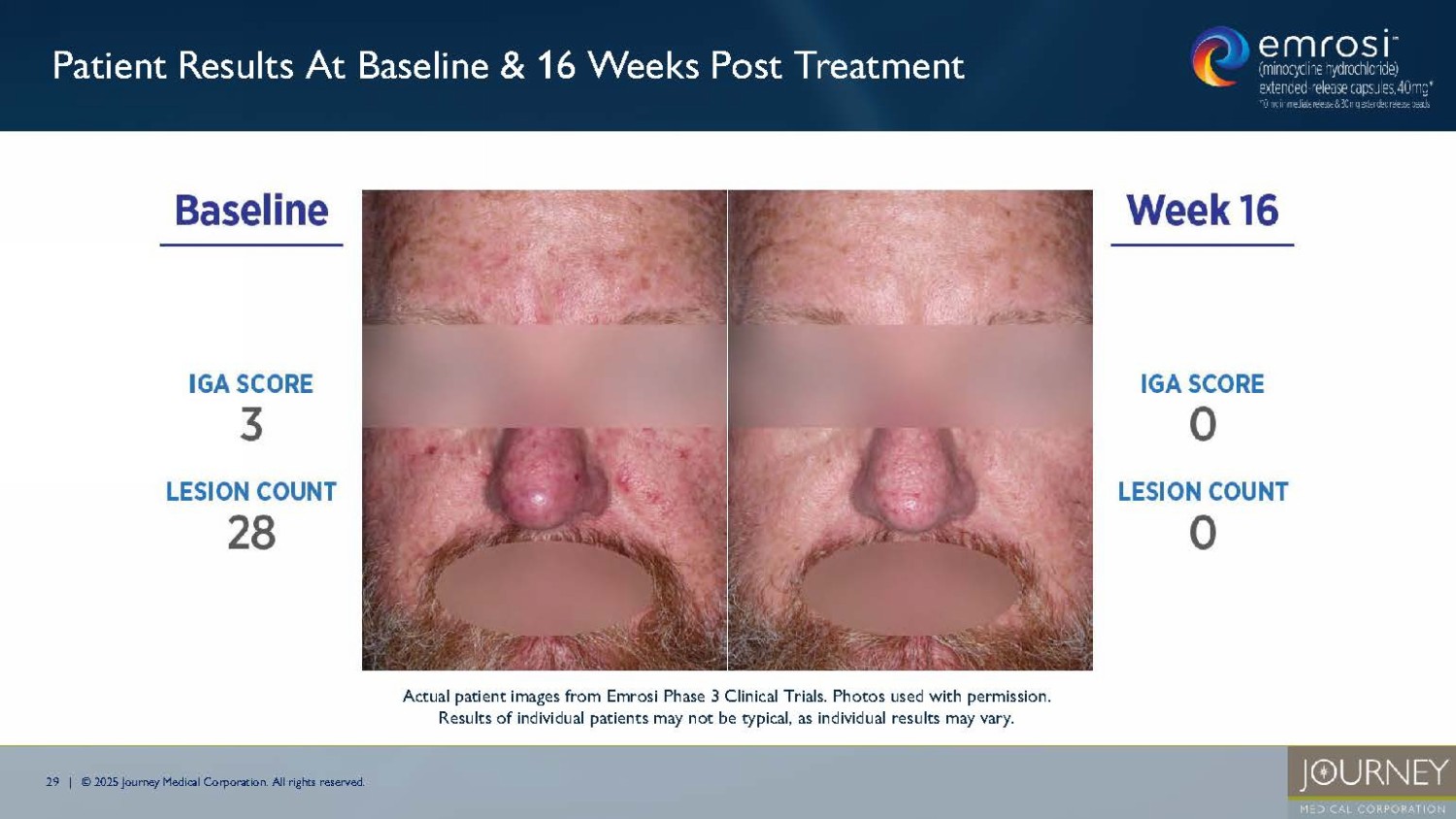
無断複写・転載を禁じます。米国における酒さの推定患者数(2023年) 酒さの治療を受けている米国人はわずか200~300万人と推定されており1 、さらに数百万人の酒さ患者が一時的な寛解状態にある可能性がある。 エムロジ第3相臨床試験のベースライン16週目の患者 エムロジ第3相臨床試験の実際の患者画像。写真は許可を得て使用しています。個人差があるため、個々の患者の結果が典型的なものとは限りません。1.Wehausen , B., Hill, D. E, & Feldman, S. R. (2016).乾癬や酒さのほとんどの人は治療を受けていない:大規模集団研究。Dermatology Online Journal, 22(7).
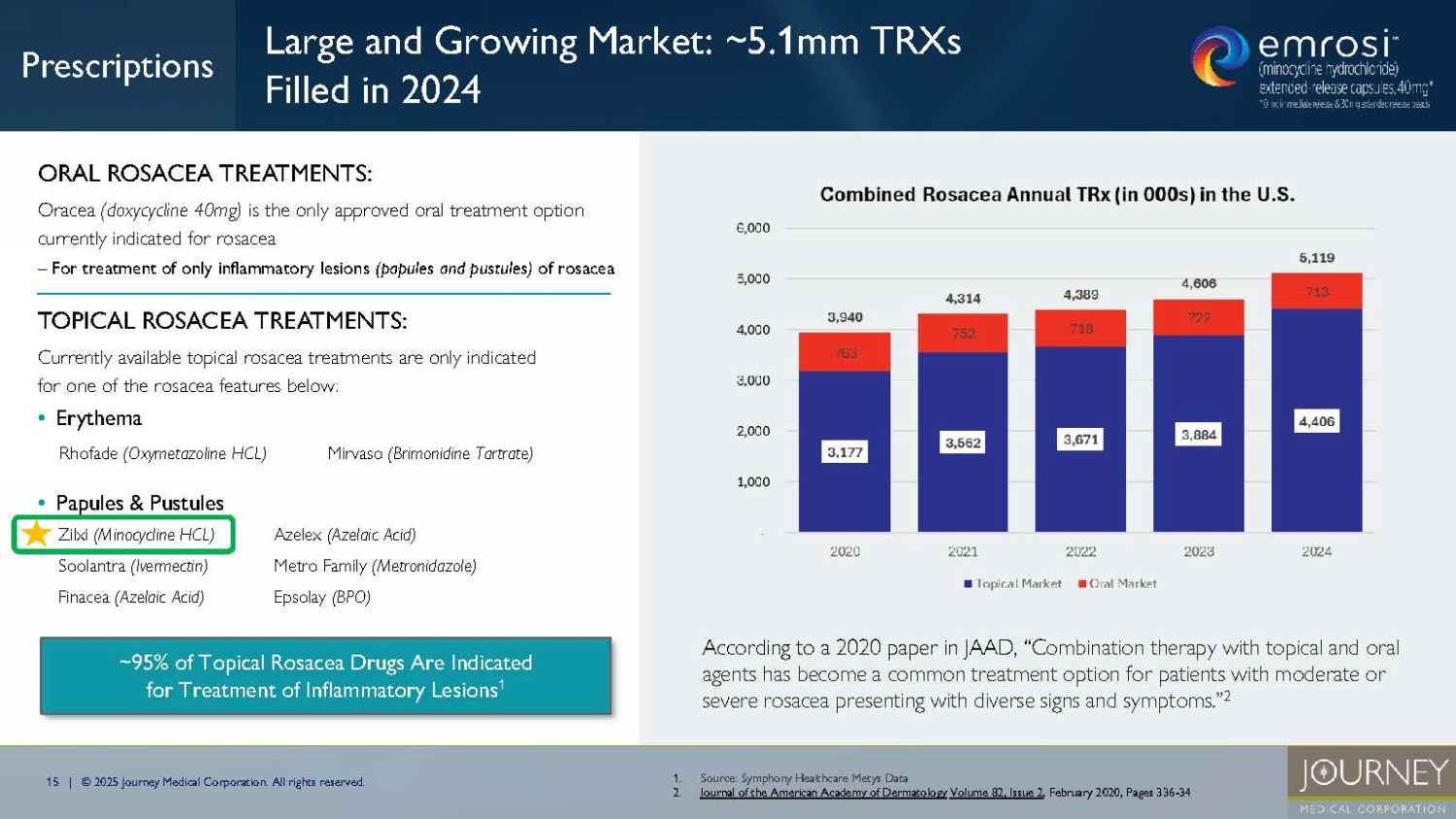
15 | © 2025 Journey Medical Corporation.無断複写・転載を禁じます。大きく成長する市場:~2024年には5.1mmのTRXが充填される:現在利用可能な局所酒さ治療薬は、以下の酒さの特徴の1つにのみ適応がある:- 紅斑-丘疹および膿疱 Azelex (アゼライン酸) Zilxi (ミノサイクリンHCL) Metro Family (メトロニダゾール) Soolantra (イベルメクチン) Epsolay (BPO) Finacea (アゼライン酸) ~95%の酒さ外用薬は炎症性病変の治療に適応がある 1 1.出典Symphony Healthcare Metysデータ 2.Journal of the American Academy of Dermatology 82巻2号 , 2020年2月, 336 - 34ページ Mirvaso (Brimonidine Tartrate) Rhofade (Oxymetazoline HCL) 経口酒さ治療薬:オラセア(ドキシサイクリン40mg)は、現在酒さに適応がある唯一の承認された経口治療選択肢である - 酒さの炎症性病変(丘疹と膿疱)のみの治療用 2020年のJAAD誌の論文によると、"外用薬と経口薬の併用療法は、多様な徴候や症状を呈する中等度または重度の酒さ患者に対する一般的な治療選択肢となっている"2 処方箋16|©2025 Journey Medical Corporation.
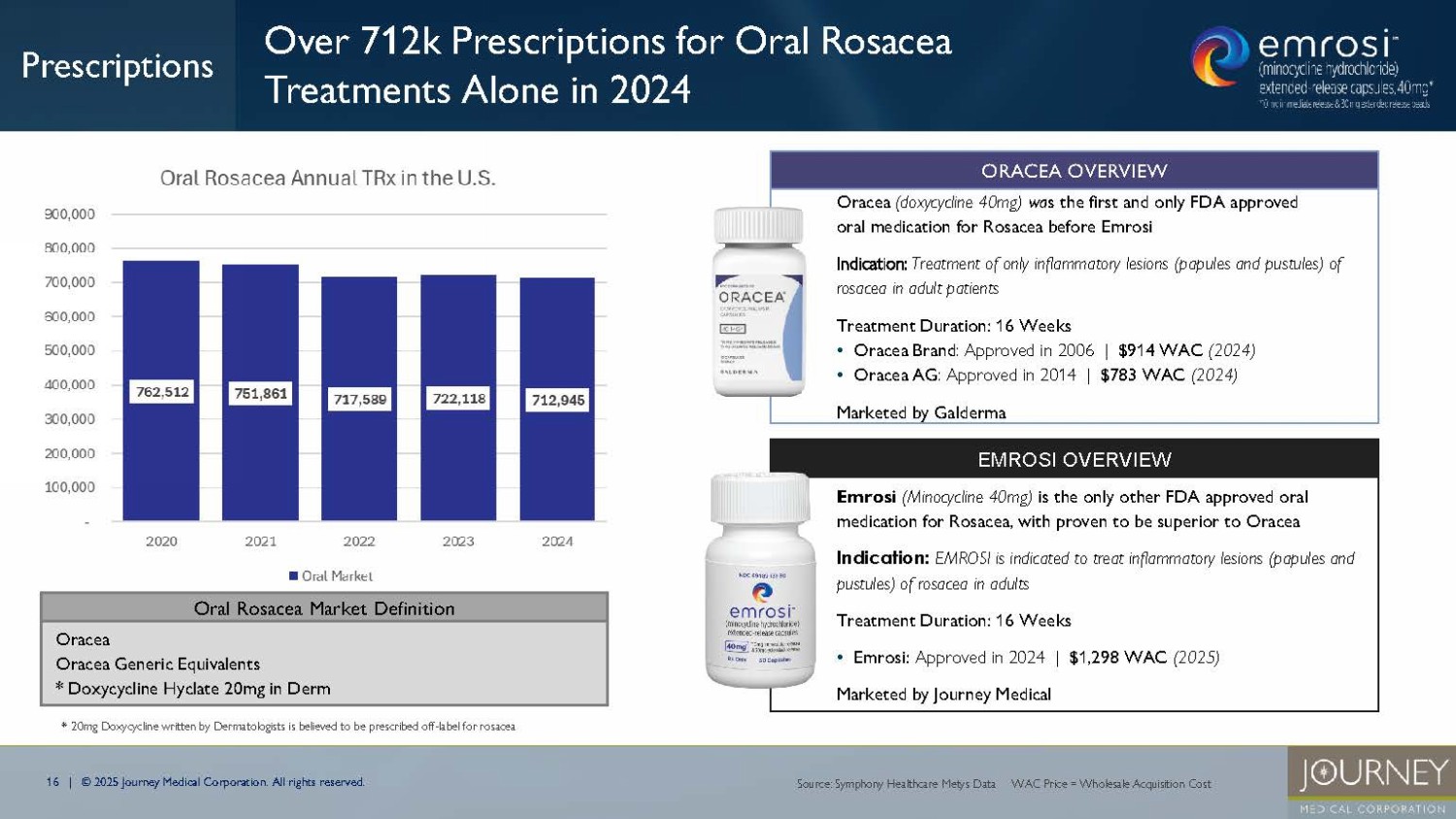
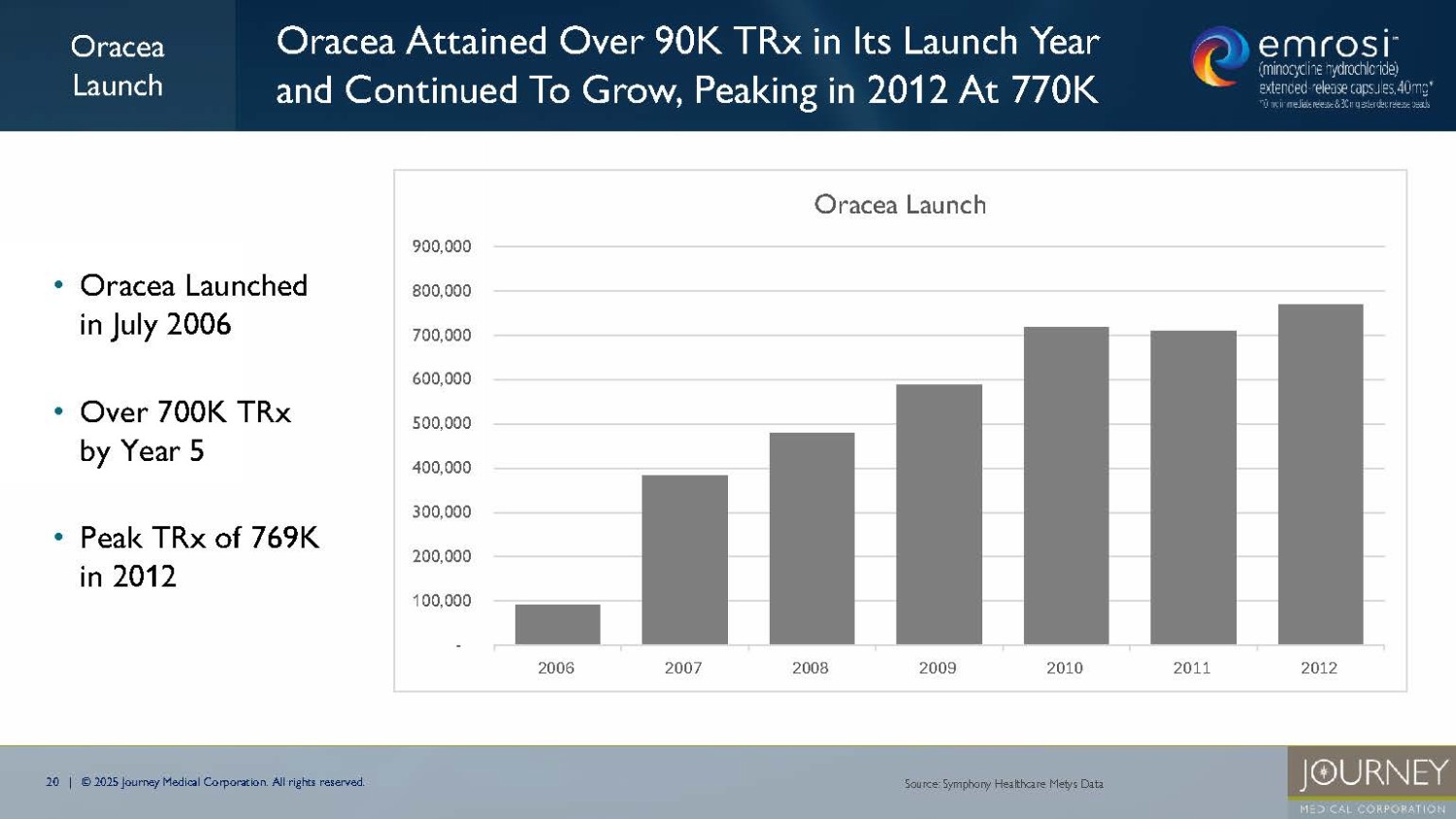
無断複写・転載を禁じます。2024年には経口酒さ治療薬だけで71.2万件以上の処方 ORACEAの概要 Oracea(ドキシサイクリン40mg)は、Emrosi以前に酒さ治療薬としてFDAに承認された最初で唯一の経口薬である:適応:成人患者における酒さの炎症性病変(丘疹および膿疱)のみの治療:16週間 - Oraceaブランド:2006年承認|914WACドル(2024年) - Oracea AG:2014年承認|783WACドル(2024年) 販売:Galderma 経口酒さ市場 定義 Oracea Oraceaジェネリック同等品 * Doxycycline Hyclate 20mg in Derm 出典:Symphony Healthcare Metys Data WikipediaSymphony Healthcare Metys Data WAC Price = Wholesale Acquisition Cost * 皮膚科医によって書かれたドキシサイクリン20mgは、酒さの適応外処方と考えられる EMROSIの概要 Emrosi(ミノサイクリン40mg)は、酒さの適応でFDAに承認された唯一の経口薬であり、Oraceaより優れていることが証明されている:成人における酒さの炎症性病変(丘疹および膿疱)の治療に適応される:16週間 - エムロジ2024年承認|WAC 1,298ドル(2025年)|Journey Medical Prescriptions 17|©2025ジャーニーメディカル株式会社.
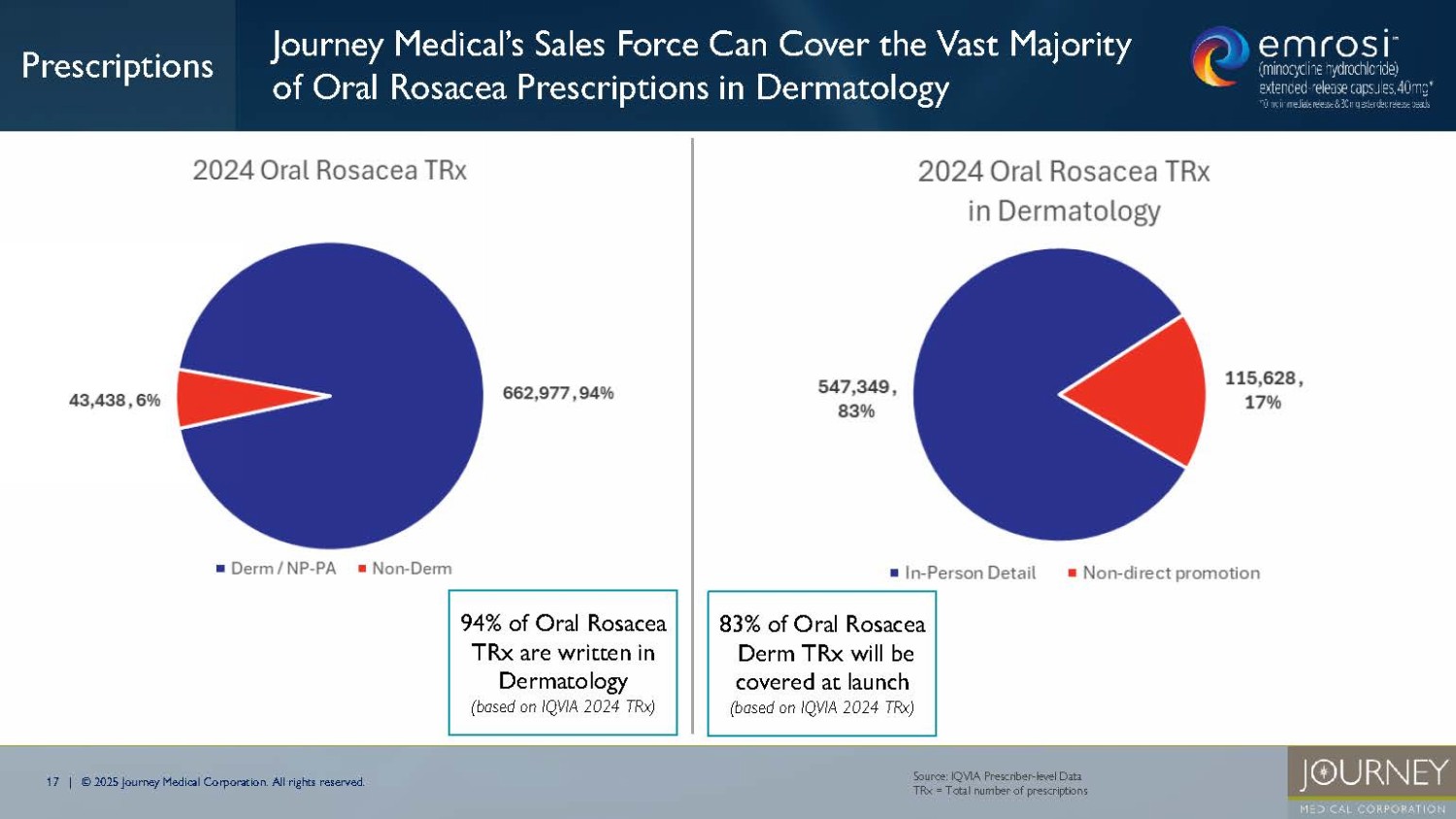
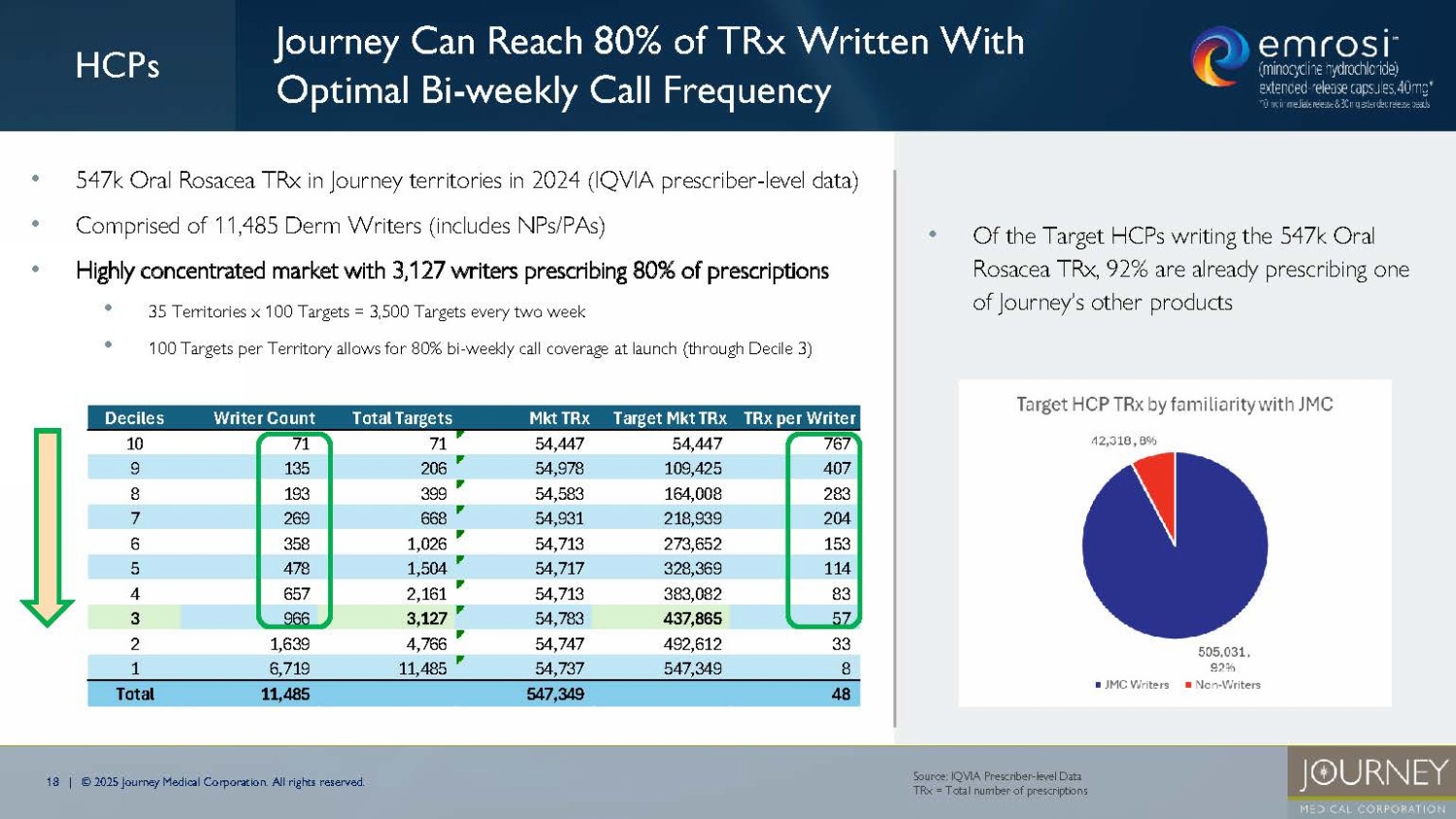
無断転載を禁じます。出典IQVIA Prescriber - level Data TRx = 処方総数 口腔内酒さTRxの94%は皮膚科で書かれている(IQVIA 2024 TRxに基づく) 口腔内酒さDerm TRxの83%は上市時にカバーされる(IQVIA 2024 TRxに基づく) Journey Medicalの営業部隊は皮膚科処方における口腔内酒さ処方の大部分をカバーできる 18 | © 2025 Journey Medical Corporation.
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プ

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべ

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初め
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初め

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべ

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になる

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実

Q&A
 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン