UNITED STATES
SECURITIES AND EXCHANGE COMMISSION
Washington, D.C. 20549
FORM 8-K
現行レポート
セクション13または15に基づいて(d)
1934年の証券取引所法の
報告日(最も古いイベントの報告日):2024年1月10日
モルフィック・ホールディング
(チャーターで指定された登録者の正確な名前)
| デラウェア | 001-38940 | 47-3878772 |
| (の州またはその他の管轄区域 | (Commission | (I.R.S. Employer |
| incorporation or organization) | File Number) | Identification No.) |
| 35 ゲートハウス・ドライブ、A2 ウォルサム(マサチューセッツ州 | 02451 |
| (主要経営陣の住所) | (Zip Code) |
登録者の電話番号(市外局番を含む(781) 996-0955
Not Applicable
(前回の報告書以降に変更があった場合、旧姓または旧住所)
Form8-Kの提出が、以下の条項のいずれかに基づく登録者の提出義務を同時に満たすことを意図している場合は、以下の該当するチェックボックスをチェックしてください:
| ¨ | 証券法に基づく規則425に従った書面によるコミュニケーション(17 cfr 230.425) |
| ¨ | 取引所法の下でのルール14a-12(17 cfr 240.14a-12)に基づく資料の勧誘。) |
| ¨ | 取引所法の規則14d-2(b)に基づく開始前のコミュニケーション(17 cfr 240.14d-2(b)) |
| ¨ | 証券取引法の規則13e-4(c)に基づく開始前のコミュニケーション(17 cfr 240.13e-4(c)) |
法第12条(b)に従って登録された証券:
| Title of each class | Trading Symbol(s) | 登録されている各取引所の名称 | ||
| 普通株式、1株あたりの額面は0.0001ドル | MORF | The Nasdaq Global Market |
登録者が1933年証券法規則405(本章230.405節)または1934年証券取引法規則12b-2(本章240.12b-2節)で定義される新興成長企業であるかどうかをチェックマークで示す。
Emerging growth company ¨
新興成長企業の場合、登録者が取引所法第13条(a)に従い提供される新規または改訂された財務会計基準に準拠するための延長された移行期間を使用しないことを選択した場合は、チェックマークで示す。¨
Item 2.02 営業成績および財務状況
2024年1月10日、Morphic Holding, Inc.(以下「会社」)は、公開プレゼンテーションの質疑応答において、2023年12月31日現在、現金、現金同等物および市場性のある有価証券の予備的な総額は約7億ドルであると発表した。公開プレゼンテーションの議事録の一部を別紙99.1として添付する。
2023年12月31日に終了する四半期および通期における当社の監査済み財務諸表はまだ入手可能ではありません。したがって、ここに記載されている情報は、当社の決算手続きの完了および財務諸表監査の完了による調整を前提とした、当社の暫定的な財務データを反映しています。2023年12月31日に終了する四半期および年度の年次報告書(Form 10-K)が完成し、一般に開示された時点で反映される実際の業績は、ここに記載された暫定的な業績とは異なる可能性があります。
| Item 7.01 Regulation FD Disclosure |
2024年1月10日、当社はコーポレート・プレゼンテーションを更新した。更新された会社説明資料のコピーは別紙99.2としてここに添付され、参照することによりここに組み込まれる。
本報告書の別紙99.1および99.2を含むForm 8-Kによる本Current Reportに記載された情報は、1934年証券取引所法(「取引所法」)第18条に照らして「提出」されたものとはみなされず、また同法または1933年証券法(「証券法」)第11条および第12条(a)(2)の適用を受けるものでもありません。本フォーム8-K最新報告書および添付の別紙99.1および99.2に記載された情報は、当該提出書類において明示的に参照規定されている場合を除き、参照により取引所法または証券法に基づくその他の提出書類に組み込まれることはありません。
Item 9.01 財務諸表および添付資料
(d) Exhibits
| Exhibit Number | Description | |
| 99.1 | 質疑応答より抜粋 | |
| 99.2 | 企業プレゼンテーション | |
| 104 | カバーページ インタラクティブデータファイル(inline xbrlドキュメントに埋め込まれています。) |
SIGNATURE
1934年証券取引所法(Securities Exchange Act of 1934)の要件に従い、登録者は本報告書に正式に権限を付与された署名者により、登録者を代表して署名させた。
| MORPHIC HOLDING, INC. | ||
| Date: January 11, 2024 | By: | /s/ Marc Schegerin |
| Marc Schegerin, M.D. | ||
| チーフ・ファイナンシャル・オフィサー兼チーフ・オペレーティング・オフィサー | ||
Exhibit 99.1
における質疑応答の記録抜粋
株式会社モルフィックホールディング2024年1月10日公開プレゼンテーション開催
マーク・シェゲリン:数週間後にフォーム10-Kを提出することになっていますが、前回のフォーム10-Qを見れば、23年末の時点で約7億ドルの資金があり、ガイダンスもここ1年ほど一貫しているので、2027年後半には達成できると考えても不思議ではないと思います。
Exhibit 99.2

2024年1月 インテグリン医薬品の新世代を提供する

本プレゼンテーションには、1995年米国民事証券訴訟改革法(Private Securi ties Litigation Reform Act of 1995)の「セーフハーバー」条項の意味における「将来見通し」に関する記述が含まれており、これには、モルフィック社が現在実施中の臨床試験の時期および成功、関連データ、モルフィック社の臨床試験の最新情報および結果、ならびにMORF - 057の潜在的な治療効果に関する記述が含まれますが、これらに限定されるものではありません。本プレゼンテーションの一部のデータは、クロススタディ比較に基づくものであり、直接比較臨床試験に基づくものではありません。クロススタディ比較は本質的に限界があり、誤解を招く類似点や相違点を示唆する可能性があります。クロススタディの比較で示された値は方向性を示すものであり、直接比較できるものではありません。確信する」、「計画する」、「継続する」、「期待する」、「予定する」、「開発する」、「シグナル」、「可能性」、「予想する」などの言葉や未来時制の記述を含む記述は、将来見通しに関する記述です。これらの将来見通しに関する記述には、リスクや不確実性、仮定が含まれており、それらが完全に実現しない場合、または正しくないことが判明した場合、当社の業績は、かかる将来見通しに関する記述によって明示的または黙示的に示されたものと大きく異なる可能性があります。将来見通しに関する記述は、本プレゼンテーションの将来見通しに関する記述に関連するリスクや不確実性、および証券取引委員会(SEC)への提出書類に記載されているその他のリスクを含め、将来見通しに関する記述に明示されている、または暗示されているものとは大きく異なるモルフィックの実際の活動や結果を引き起こす可能性のあるリスクや不確実性の影響を受けます、2023年2月23日にSECに提出された2022年12月31日に終了する会計年度の年次報告書(フォーム10-K)および2023年11月3日にSECに提出された2023年9月30日に終了する会計四半期の四半期報告書(フォーム10-Q)を含みます。これらの将来見通しに関する記述は、本書の日付時点のものであり、モルフィックは、新たな情報、将来の出来事、その他の結果にかかわらず、法律で義務付けられている場合を除き、これらの将来見通しに関する記述を更新する義務、または実際の結果が異なる可能性がある理由を明確に否認します。商標に関する注記:本プレゼンテーションで言及されている名称、ロゴ、ブランドを含むすべての第三者商標は、それぞれの所有者に帰属します。第三者商標への言及はすべて識別のみを目的としたものであり、商標法上の名目的なフェアユースとみなされる。

2 フォワード-ルッキング ステートメント ユニークな受容体:インテグリンとは何か?- インテグリンは、自己免疫疾患、線維性疾患、心臓代謝性疾患、腫瘍性疾患などの複雑な疾患において、生物学的に中心的な役割を果たし、双方向にシグナルを伝達する唯一の受容体である。高価で複雑な生物学的製剤は、インテグリンを標的とすることにより、臨床的に意味のある有効性を示してきた。

MInTプラットフォームMInTプラットフォーム:経口インテグリンの課題に対するMorphic社のソリューション 4 構造的知識 特異的な足場 集中的な化学ライブラリー 抽出可能なターゲットに対するアッセイ 合成的に抽出可能な "ヒット" 計算化学with Schr ö dinger 高品質プローブ 関連ターゲットの薬理学的検証 新規薬剤候補 1 2 3 4 5 6 7 8 9 MInTデザインサイクル 独自パイプライン 5 候補ターゲット(プログラム) インディケーション ディスカバリー IND - INDフェーズ1 フェーズ2 フェーズ3 MORF - 057 α 4 β 7 潰瘍性大腸炎 クローン病 次世代 α 4 β 7 消化器疾患 MORF SMI 1 非インテグリン標的 消化器疾患 MORF SMI α 5 β 1 肺高血圧症 MORF - 088 α v β 8 骨髄線維症 固形腫瘍 MORF SMI/mAbs 未公開 複数の適応症 1 SMI:経口低分子阻害剤


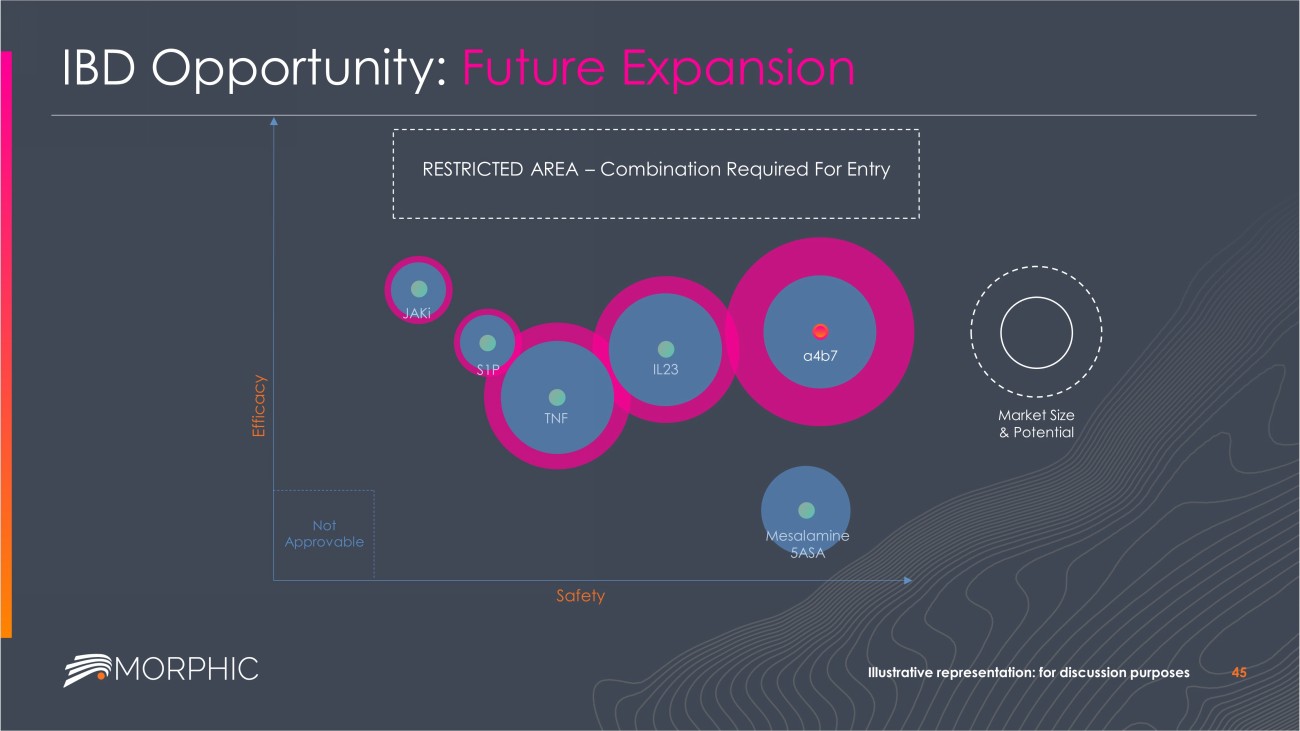
MORF - 057 α4 β7低分子阻害剤:IBD治療における有効なメカニズム EMERALD - 2 フェーズ 2b 試験進行中 IBD:理想的な将来の治療パラダイム 7 併用可能な経口剤 耐薬品性に優れ、高い有効性


適応症 MORF - 057: IBDに対するクラス初の経口インテグリン治療薬 8 α 4 β 7の高選択的経口低分子阻害薬。承認されたモノクローナル抗体vedolizumabを通じて、IBDの治療薬として有効性が確認されている。600万人のアメリカ人が過敏性腸疾患を患っている 1 メカニズム 臨床データ フェーズ2a試験において、複数の有効性評価指標において臨床的に意義のある一貫した活性データが得られている、α4β7阻害はIBD治療において実証されたメカニズムである - 承認抗体Entyvio ®(vedolizumab) - 抗α4β7抗体であるvedolizumabは、UCおよびクローン病の治療において実証されたメカニズムでT細胞のトラフィッキングを阻害する - 承認以来、265,000人以上の患者がvedolizumabの投与を受けている - vedolizumabは2022年度に$5.2Bの売上を計上。2022年度の売上高は5.2億ドル 9 内皮内腔・腸管血管内腔・血液T細胞 1 武田薬品のプレスリリース 2 グローバルデータ ENTYVIO ® はミレニアム・ファーマシューティカルズ Inc.の登録商標です。内皮細胞 a 4 b 7 MAdCAM - 1


MORF - 057 は、IBD における経口 α4 β7 阻害薬としての期待に常に応えてきた 10 MORF - 057 前臨床フェーズ 1 フェーズ 2a 経口投与 経口投与経路での良好な忍容性プロファイル α4 β7 飽和度(血清) 30 - 50% ↑ 主要なリンパ球における有意な臨床効果 すべての科学的ポスターおよびプレゼンテーションは https://investor.morphictx.com で入手可能 基礎データについては、上記の行見出しのリンクをクリックしてください EMERALD - 1 MORF - 057 のフェーズ 2a 試験


MORF - 057 フェーズ 2a:EMERALD - 1中等症から重症の潰瘍性大腸炎を対象とした試験 12回の試験訪問 W0 D1 W2 D15 W6 D43 W12 D85 W20 D141 W28 D197 W36 D253 W44 D309 W52/EOT D365 W82/SFU D575 W56/SFU D393 W65 D456 W78/EOT D547 W - 6~-1 D - 42~-11 中等症から重症の活動期潰瘍性大腸炎患者を対象とした MORF - 057(100mg BID)の第Ⅱa相非盲検単群試験 (主要コホート数 n=35) 非盲検投与期間 MORF - 057(100mg B.投与期間 MORF - 057 (100mg B.I.D. P.O.)を 52 週間 主要評価項目 12 週目 長期試験 延長試験への直接ロールオーバー MORF - 057 (100mg B.I.D. P.O.) を 52 週間投与する。
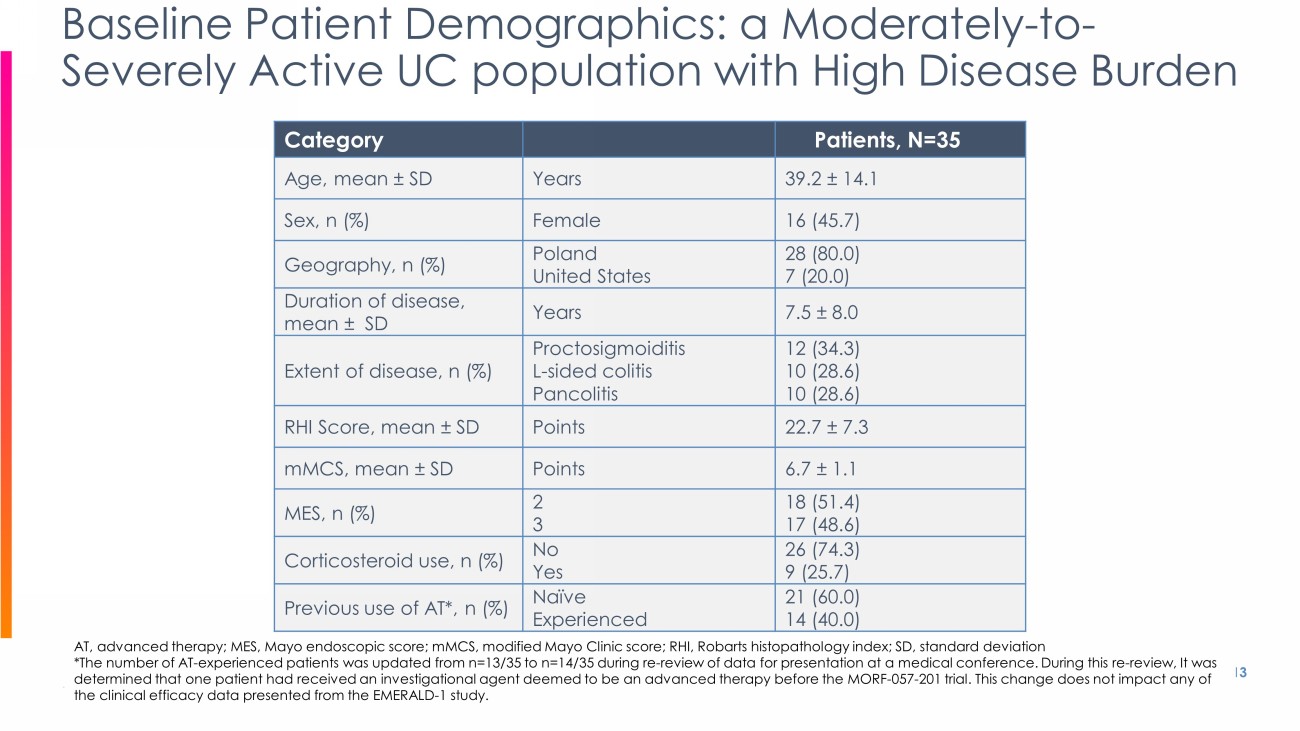
P.O.)、26週間 安全性追跡期間 安全性追跡期間は試験薬最終投与4週後に実施する:副次評価項目:mMCSのベースラインからの変化、安全性 - 事前に指定された探索的評価項目:- RHI寛解 - mMCS寛解 - mMCS奏効 - 複数のPK/PDパラメータ - 関連バイオマーカー Phase 2a 分類 患者数 N=35 年齢、平均±SD 年 39.2 ± 14.1 性別、n(%) 女性 16 (45.7) 地理、n(%) ポーランド 米国 28 (80.0) 7 (20.0) 罹病期間 , 平均 ± SD 年数 7.5 ± 8.0 罹病範囲 n (%) 前腸S状結腸炎 L側大腸炎 膵臓炎 12 (34.3) 10 (28.6) 10 (28.6) RHIスコア , 平均 ± SD ポイント 22.7 ± 7.3 mMCS , 平均 ± SD ポイント 6.7 ± 1.1 MES, n (%) 2 3 18 (51.4) 17 (48.6) 副腎皮質ステロイドの使用、n(%) なし あり 26 (74.3) 9 (25.7) AT*の使用歴、n(%) 未経験 21 (60.0) 14 (40.0) 13 ベースライン患者人口統計:疾患負荷の高い中等度から重度の活動性UC集団 AT、advanced therapy; MES、Mayo endoscopic score; mMCS、modified Mayo Clinic score; RHI、Robarts histopathology index; SD、標準偏差 *AT経験患者数は、医学学会発表のためのデータ再調査中にn=13/35からn=14/35に更新された。この再レビューにおいて、1名の患者がMORF-057-201試験前に先進治療とみなされる治験薬の投与を受けていたことが判明した。この変更はEMERALD - 1試験で発表された臨床有効性データには影響しない。

MORF-057:EMERALDにおける忍容性は概ね良好 1 安全性シグナルは観察されなかった 14 副次的事象(AE)プロファイルは基礎疾患と一致していた 12 (34.3%) 1つ以上のAEを認めた患者 0 死亡に至ったAEを認めた患者 0 グレード3のAEを認めた患者 2 (5.7%) 1 治療に関連したAEを認めた患者 2 (5.7%) 共通(5%以上)のAE UCの増悪 貧血 4 (11.4%) 3 (8.6%) 2 1.いずれも UC の増悪で、1 例は早期の中止を余儀なくされた 2.4/25/23 現在、患者は 12 週間の導入期間を超えて EMERALD - 1 試験を継続しており、その他の安全性シグナルや SAE は報告されていない。

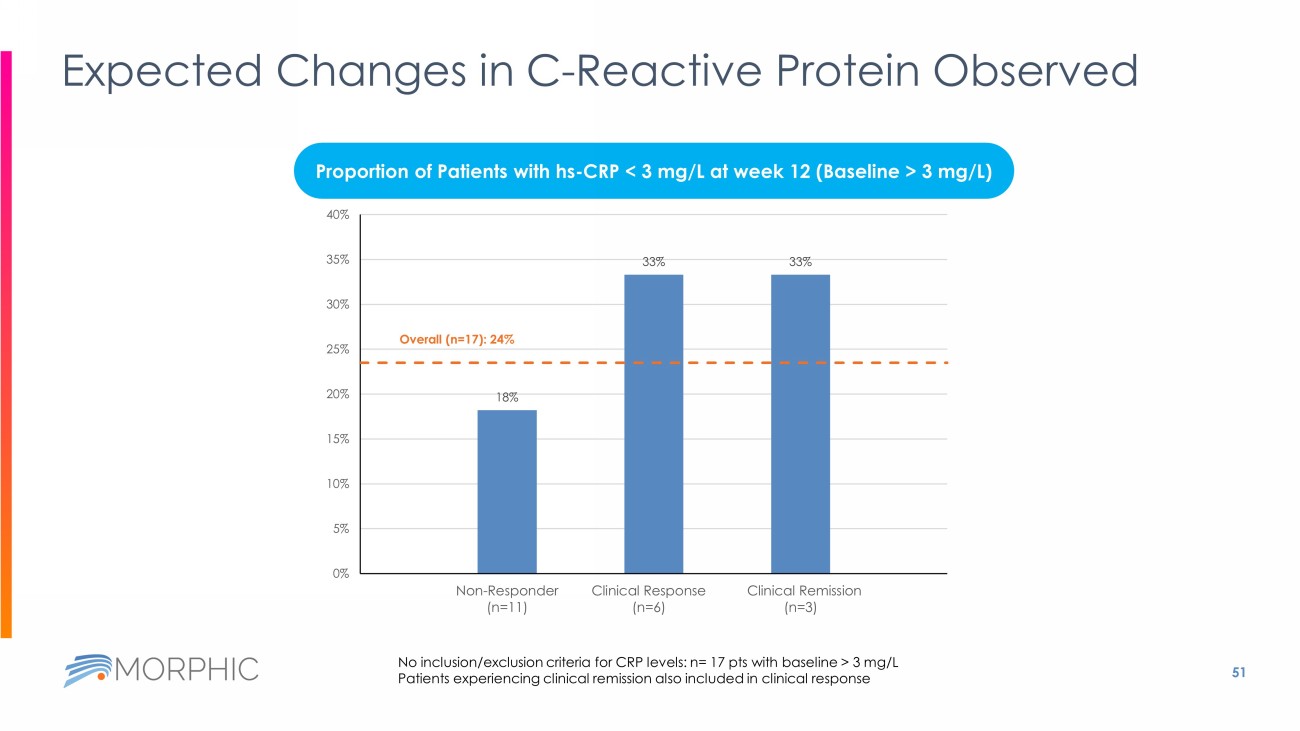
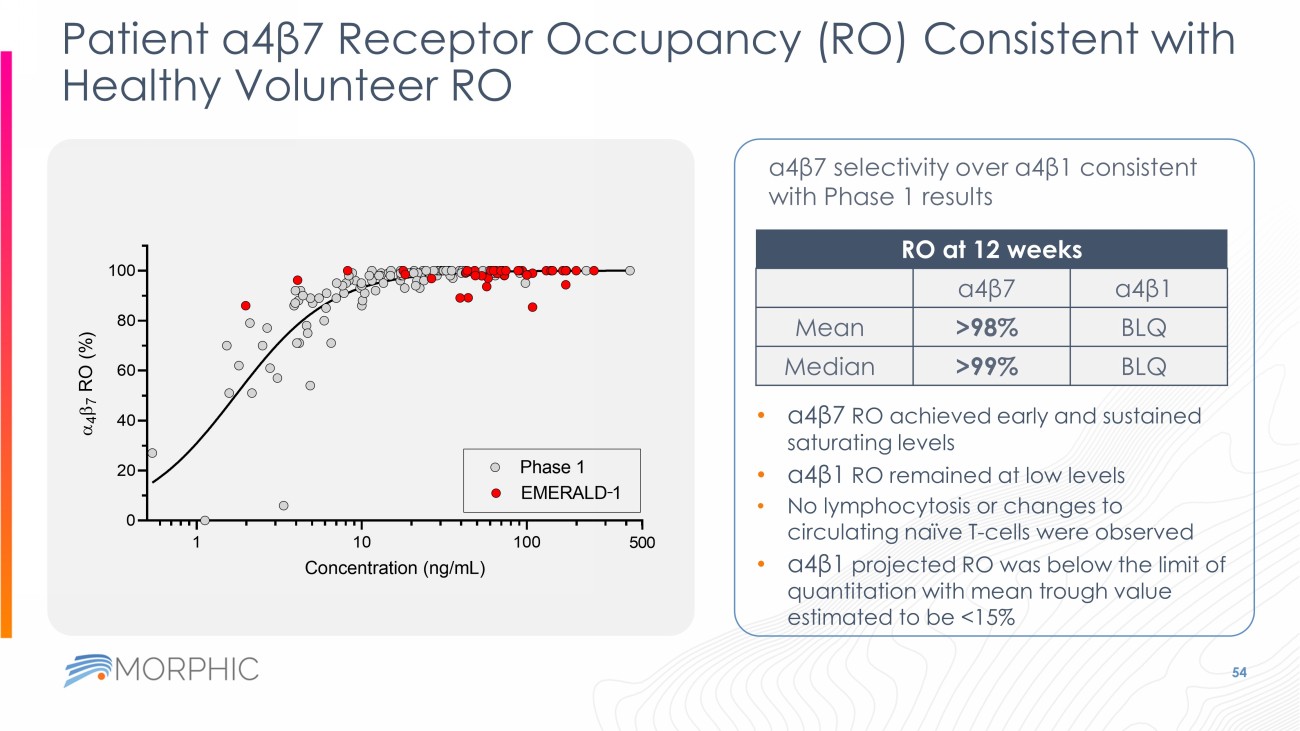
患者のa4β7受容体占拠率(RO)は健常人ボランティアのROと一致した 15 a4β1に対するa4β7の選択性はフェーズ1の結果と一致した 12週間後のRO a4β7 a4β1 平均 >98% BLQ 中央値 >99% BLQ - a4β7 ROは早期に飽和レベルを達成し、持続した - a4β1 ROは低レベルに留まった - リンパ球増加や循環ナイーブT -細胞への変化は観察されなかったa4β1投影ROは定量限界以下であり、平均トラフ値は15%未満と推定された 1 10 100 0 20 40 60 80 100 500 濃度(ng/mL) 4 7 R O ( % ) Phase 1 EMERALD 1 -16 便中カルプロテクチンの減少は疾患の改善と相関する 19% 54% 75% 全体(n=29):35% 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% 100% 非反応(n=16) 臨床効果(n=13) 臨床寛解(n=8) - 11% - 86% - 89% 全体(n=27):- 56% -100% -90% -80% -70% -60% -50% -40% -30% -20% -10% 0% Non Responder (n=15) Clinical Response (n=12) Clinical Remission (n=8) n = ベースラインFCが250mg/kgを超えた患者。

FC値に関する除外基準なし 臨床的寛解を経験している患者は、臨床的反応aにも含まれる。
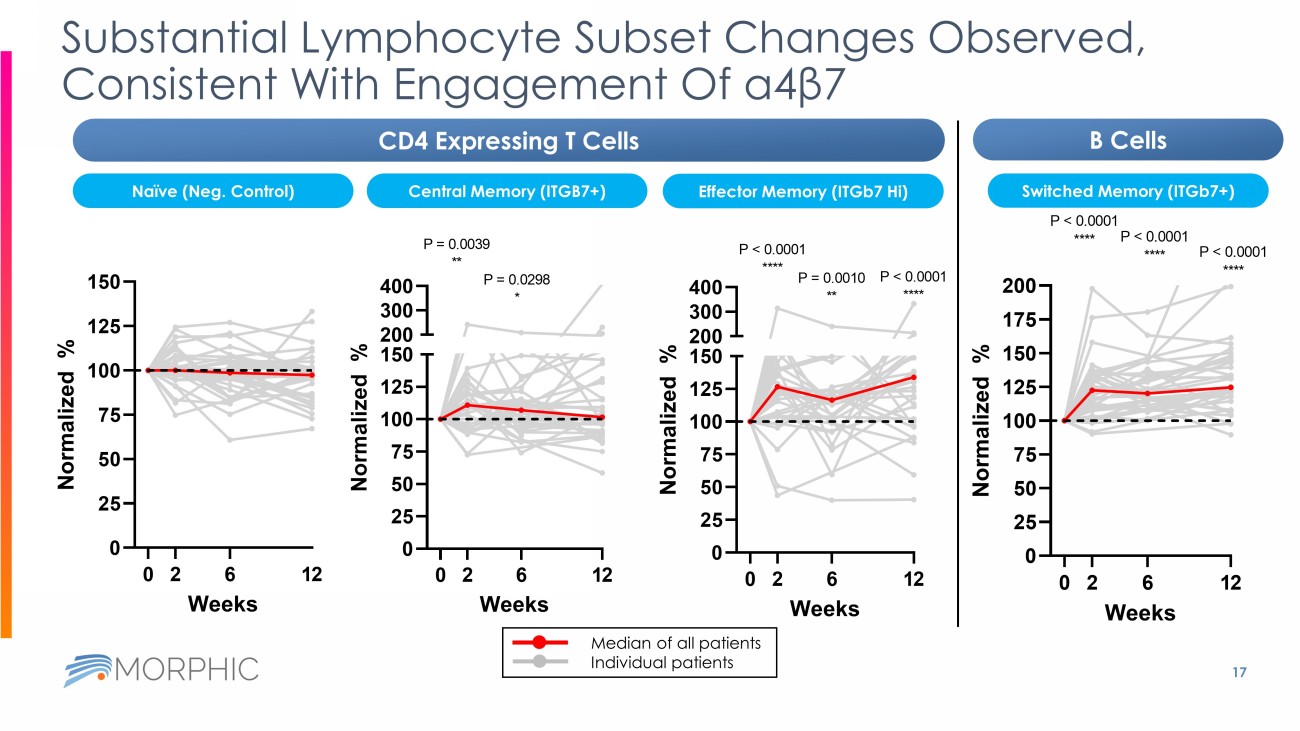
第12週時点のデータがない患者が2名いた 第12週時点の便中Calが250mg/kg未満であった患者の割合(ベースライン>250mg/kg)、n=29 第12週時点の便中Calのベースラインからの減少率(ベースライン>250mg/kgおよび第12週時点のデータがある)、リンパ球サブセットの大幅な変化が観察され、α 4 β 7 の関与と一致 0 25 50 75 100 125 150 週 N o r m a l i z e d % 0 2 6 12 0 25 50 75 100 125 150 200 300 400 週 N o r m a l i z e d % P = 0.0039 ** 0 2 6 12 P = 0.0298 * 0 25 50 75 100 125 150 200 300 400 Weeks N o r m a l i z e d % 0 2 6 12 P < 0.0001 **** P = 0.0010 **** P < 0.0001 **** 全患者の中央値 個々の患者 CD4発現T細胞 B細胞 ナイーブ(Neg. コントロール) スイッチメモリー(ITGb7+) セントラルメモリー(ITGB7+) エフェクターメモリー(ITGb7 Hi)

Clinical Efficacy Results

19 エンドポイント @ 12週目 全体(N=35) RHIの変化、平均(SD) - 6.4 (11.18) p=0.0019 RHI寛解、n(%) 8 (22.9%) 臨床的奏効(mMCS)1、n(%) 16 (45.7%) 臨床的寛解(mMCS)2、n(%) 9 (25.7%) 内視鏡的奏効/改善 3 , n (%) 9 (25.7%) 修正 MCS のベースラインから 12 週目までの変化、平均(SD) - 2.3 (2.14) 主要評価項目は統計的有意性をもって達成された 全ての探索的測定において一貫した効果が観察された 1.臨床効果(mMCS):mMCSがベースラインから2点以上かつ30%以上減少し、さらに直腸出血サブスコアが1点以上または直腸出血サブスコアの絶対値が1点以下であること 2.臨床的寛解(mMCS ):直腸出血下限値が0;便の回数下限値が1;MESが1以下であり、friabilityがない 3.

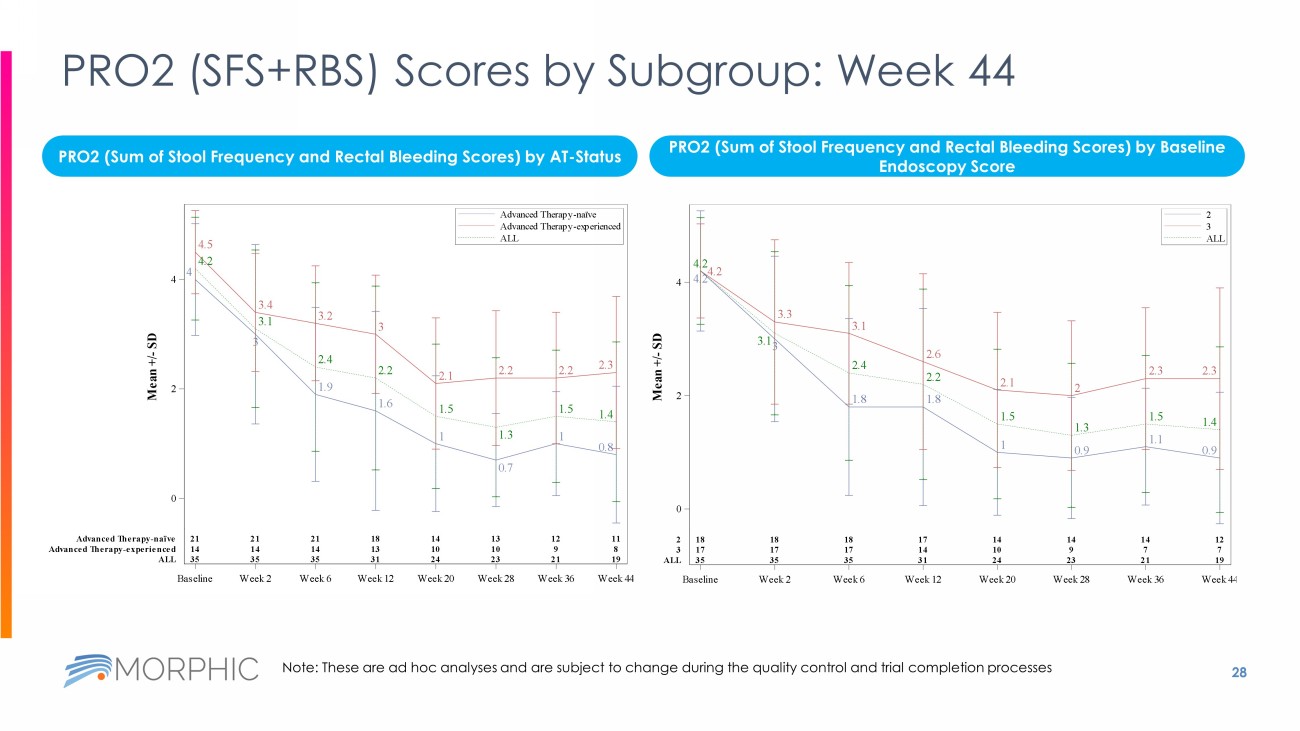
内視鏡的反応/改善MES≦1 20 EMERALD - 1 12週目におけるATの状態およびMESエンドポイント別の有効性結果 全体 N=35 AT-未経験者 n=21 AT-経験者 n=14 MES=2 n=18 MES=3 n=17 RHIの変化、平均±SD - 6.4 ± 11.2 - 7.4 ± 11.9 - 4.8 ± 10.3 - 6.9 ± 12.1 - 5.8 ± 10.4 RHIの変化≧7ポイント、n(%) 17 (48.6) 12 (57.1) 5 (35.7) 10 (55.6) 7 (41.2) RHI寛解1 , n (%) 8 (22.9) 6 (28.6) 2 (14.3) 6 (33.3) 2 (11.8) RHI減少≧50%, n (%) 12 (34.3) 9 (42.9) 3 (21.4) 9 (50.0) 3 (17.6) mMCSの変化 , 平均±SD - 2.3 ± 2.1 - 2.9 ± 2.4 - 1.6 ± 1.5 - 2.7 ± 2.3 - 1.9 ± 1.9 臨床効果(mMCS)2 , n (%) 16 (45. 7) 11 (52.7) 11 (52.4) 5 (35.7) 9 (50) 7 (41.2) 臨床的寛解(mMCS)3 , n (%) 9 (25.7) 9 (42.9) 0 6 (33.3) 3 (17.6) 症候学的寛解4 , n (%) 11 (31.4) 10 (47.6) 1 (7.1) 7 (38.9) 4 (23.5) 内視鏡的反応/改善 5 , n (%) 9 (25.7) 9 (42.9) 0 6 (33.3) 3 (17.6) SFの変化、平均±SD - 0.8 ± 1.1 - 1.0 ± 1.2 - 0.5 ± 0.7 - 0.9 ± 1.3 - 0.6 ± 0.8 RBの変化、平均±SD - 1.1 ± 0.8 - 1.1 ± 0.9 - 0.9 ± 0.8 - 1.4 ± 0.8 - 0.7 ± 0.7 AT, 先進治療; MCS, Mayo Clinic Score; mMCS , modified MCS; RHI, Robarts histopathology index; SF, Stool Frequency; RB, Rectal Bleeding; SD, standard deviation 1.RHI寛解:RHI ≤ 2 2.臨床効果(mMCS ):mMCSがベースラインから2点以上かつ30%以上減少し、さらに直腸出血のサブスコア≧1または直腸出血の絶対サブスコア≦1 3.臨床的寛解(mMCS ):直腸出血サブスコア0;便の回数サブスコア≦1;MES≦1(friabilityなし) 4.症状の寛解:SFS = 0(またはベースラインから 1 ポイント以上減少した場合は = 1)、RBS = 0 5.

内視鏡的反応/改善:MES≦1 21 一貫した「全面的な」有効性のシグナルが観察された サブグループ AT - 経験あり(n=14) なし(n=21) ベースライン時の副腎皮質ステロイドの使用 あり(n=9) なし(n=26) ベースライン時のMES 3 (n=17) 2 (n=18) 平均変化率(95% CI) - 4.8 ( - 10.7, 1.1) - 7.4 ( - 12.8, - 2.0) - 5.2 ( - 11.1, 0.7) - 6.8 ( - 11.7, - 1.8) - 5.8 ( - 11.1, - 0.4) - 6.9 ( - 13.0, - 0.9) -26 -24 -22 -20 -18 -16 -14 -12 -10 -8 -6 -4 -2 0 2 Robarts Histopathology Index (RHI) Modified Mayo Clinical Score ( mMCS ) サブグループ AT - 経験あり (n=14) なし (n=21) ベースライン時の副腎皮質ステロイド使用 あり (n=9) なし (n=26) ベースライン時のMES 3 (n=17) 2 (n=18) 平均変化率 (95% CI) - 1.6 ( - 2.4, - 0.7) - 2.9 ( - 3.9, - 1.8) - 1.4 ( - 2.3, - 0.6) - 2.7 ( - 3.6, - 1.7) - 1.9 ( - 2.9, - 1.0) - 2.7 ( - 3.9, - 1.6) -8 -7 -6 -5 -4 -3 -2 -1 0 1 平均 = - 6.4 平均 = - 2.3 22 前治療歴とベースラインのMESにかかわらず、全患者の75%以上で臨床的改善がみられた 77% 46% 26% 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% mMCSの改善 臨床的反応 臨床的寛解 全体的な臨床的改善 AT-未経験者:n=21; AT-経験者:AT - Naïve: n=21; AT - Experienced: n=14 76% 52% 43% 79% 36% 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% mMCS臨床反応 臨床的寛解の改善 AT-状態別の臨床的改善 AT-Naïve: 83% 50% 33% 71% 41% 18% 0% 10% 20% 30% 40% 50% 60% 70% 80% 90% mMCS臨床反応 臨床的寛解の改善 ベースラインMES MES=2 MES=3 ベースラインMES=2: n=18; ベースラインMES=3: n=17 N=35 患者の割合


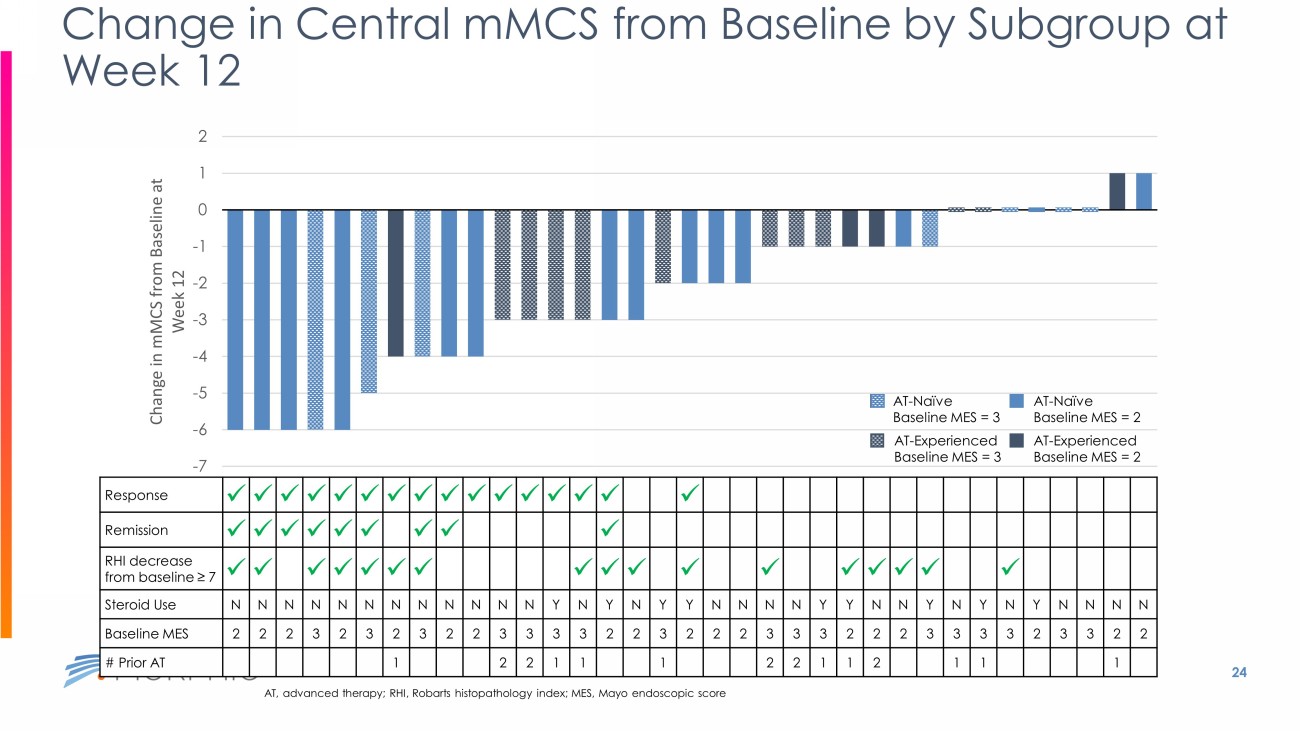

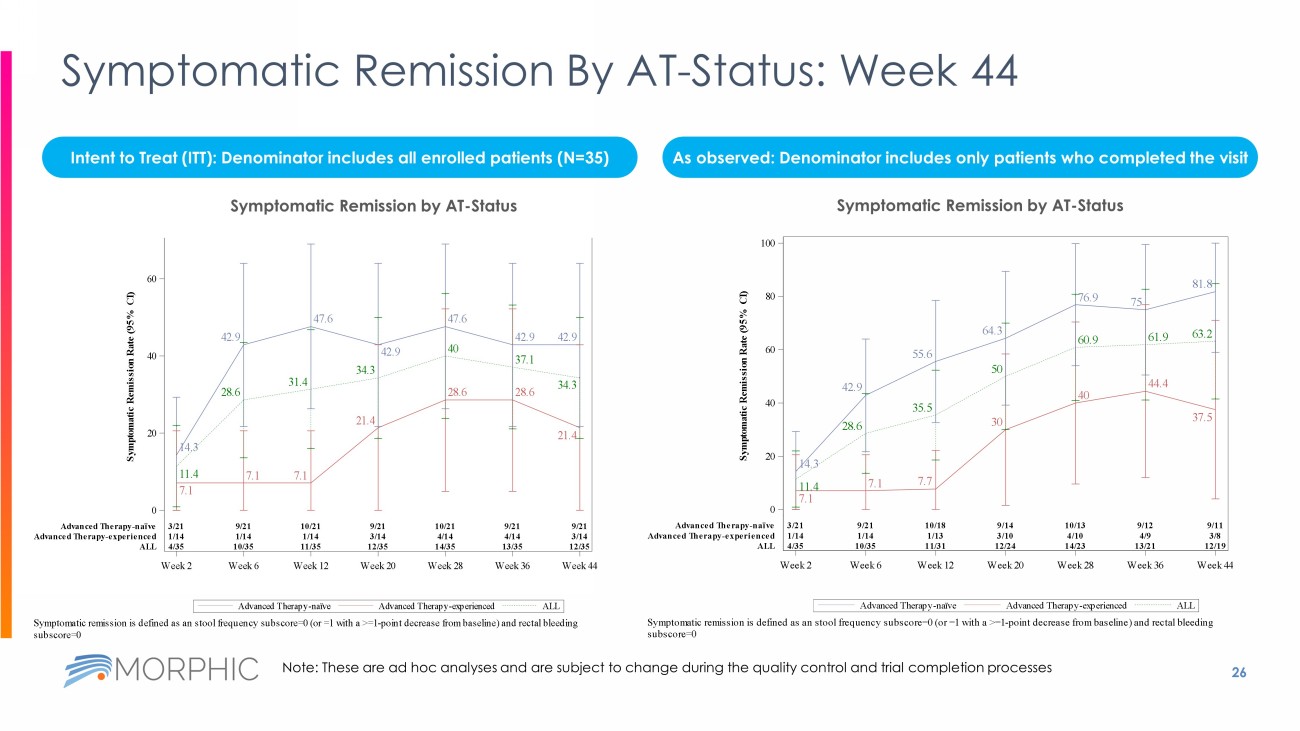
Data Beyond 12 Weeks
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間


会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアム



会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方
会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プ


会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示


会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です

会社開示情報をすべて


会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧に


会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方に


会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録


会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には

会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情報をすべてご覧になるには株探プレミアムの登録が必要です。 初めての方には「30日間の無料体験」実施中!会社開示情

 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン