Document
Exhibit 99.1
リサータ・セラピューティクス社、2023年第2四半期決算報告および最新情報を発表
臨床開発パイプラインに影響を与えることなく実施される資本節約策に基づき、2026年第1四半期までのキャッシュ・ランウェイを予測
当社の腫瘍貫通ナノ複合体(TPN)プラットフォームに関する技術移転契約を締結
東部時間8月15日(火)午前8時30分より電話会議を開催
ニュージャージー州バスキングリッジ(2023年8月14日)-進行性固形がんおよびその他の重篤な疾患に対する革新的な治療法を開発する臨床段階の製薬企業であるリサータ・セラピューティクス社(Nasdaq: LSTA、以下「リサータ社」または「当社」)は、本日、2023年6月30日に終了した第2四半期の業績を発表しました。
「第2四半期はリサータにとって力強い勢いのある四半期となりました。当社の主力製品であるLSTA1を中心に、現在進行中および計画中の複数の臨床試験を引き続き推進しました。「特に、転移性膵管腺癌(mPDAC)の一次治療患者を対象としたLSTA1の2回目の投与量を評価するため、被験者コホートを追加した第2b相ASCEND試験に重要な変更を加えました。当社は、ASCENDの結果を用いて、全世界での条件付き承認の可能性を検討し、最適化された第3相プログラムを設計する予定です。また、オーストラリアでiLSTA試験が開始され、リサタ社によるLSTA1の初のフルスポンサー試験であるBOLSTER試験が開始されました。最後に、当社のTPN(Tumor Penetrating Nanocomplex:腫瘍貫通ナノ複合体)プラットフォームについて、前リザタ最高事業責任者のデビッド・スラック(David Slack)が新たに設立したインピロ・セラピューティクス社(Impilo Therapeutics, Inc.TPN技術が、RNAベースの治療薬開発の分野で深い専門知識を持つチームの手に渡ることを嬉しく思います。"
さらにマッツォ博士は次のように続けた。「また、特筆すべきことに、今四半期、私たちは多くの資金節約の決断を下しましたが、その結果、事業を支える予定資本を2026年第1四半期まで延長することができました。現在、当社のバランスシートには、現在予想される資金需要に基づき2年分以上の資金が用意されており、開発計画の遂行に集中し、有意義な臨床データの読み出しにできるだけ早く到達するという目標を達成するのに適した状況にあると確信しています。"
Development Portfolio Highlights
lsta1による固形がん治療と他の抗がん剤との併用について
LSTA1は、共投与または繋留された抗癌剤がより効果的に固形癌に浸透することを可能にする新規の取り込み経路を活性化するようにデザインされた治験薬である。LSTA1は腫瘍特異的にこの活性輸送系を活性化し、その結果、全身的に共投与された抗癌剤はより効率的に腫瘍に浸透・蓄積し、正常組織は影響を受けないことが期待される。前臨床モデルにおいて、LSTA1は腫瘍微小環境を変化させ、腫瘍を免疫療法に対してより感受性にする能力も示している。リサータとその開発共同研究者は、化学療法、免疫療法、RNAベースの治療薬など、さまざまな既存および新規の抗癌剤の送達促進を示す重要な非臨床データを蓄積してきた。現在までに、LSTA1は、膵臓癌に対する標準的な化学療法の送達を増強する能力を試験するためにデザインされた、完了済みおよび進行中の臨床試験においても、良好な安全性、忍容性および活性を実証しています。
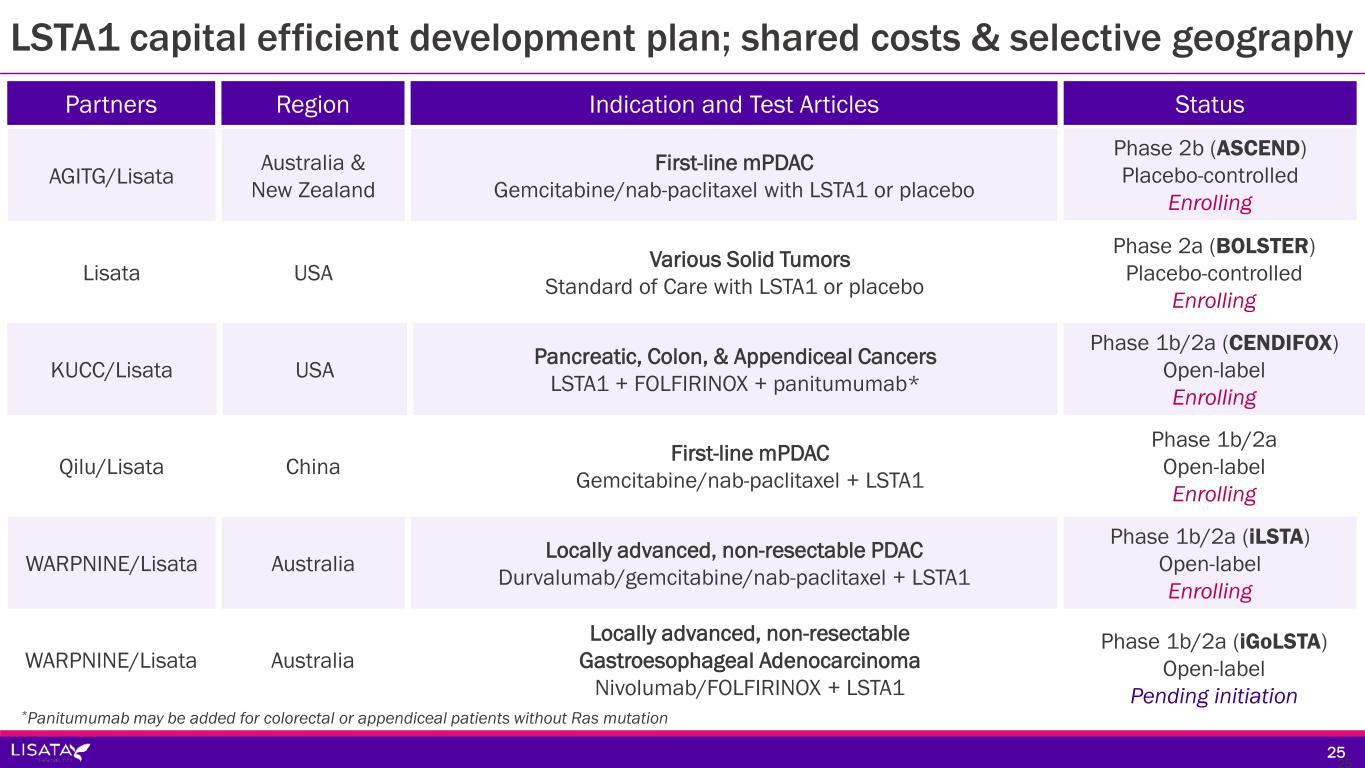
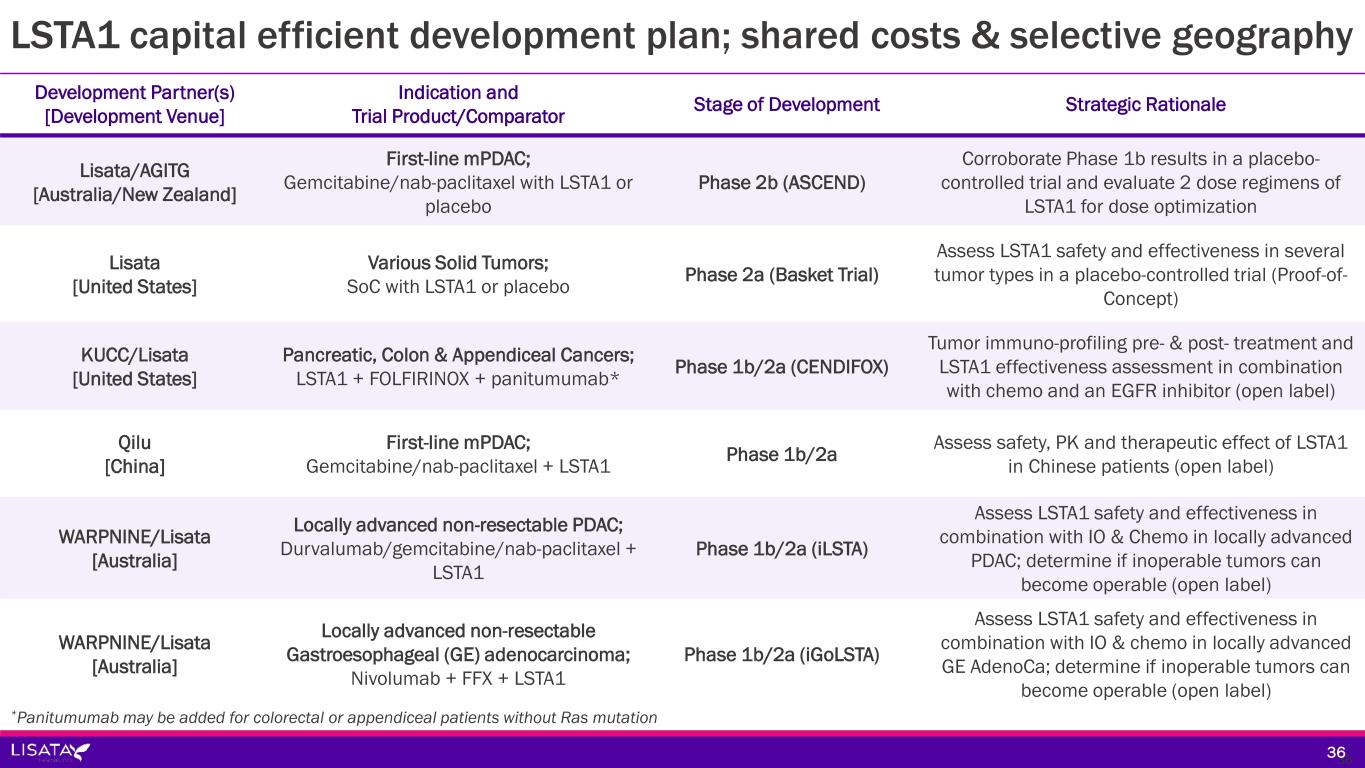
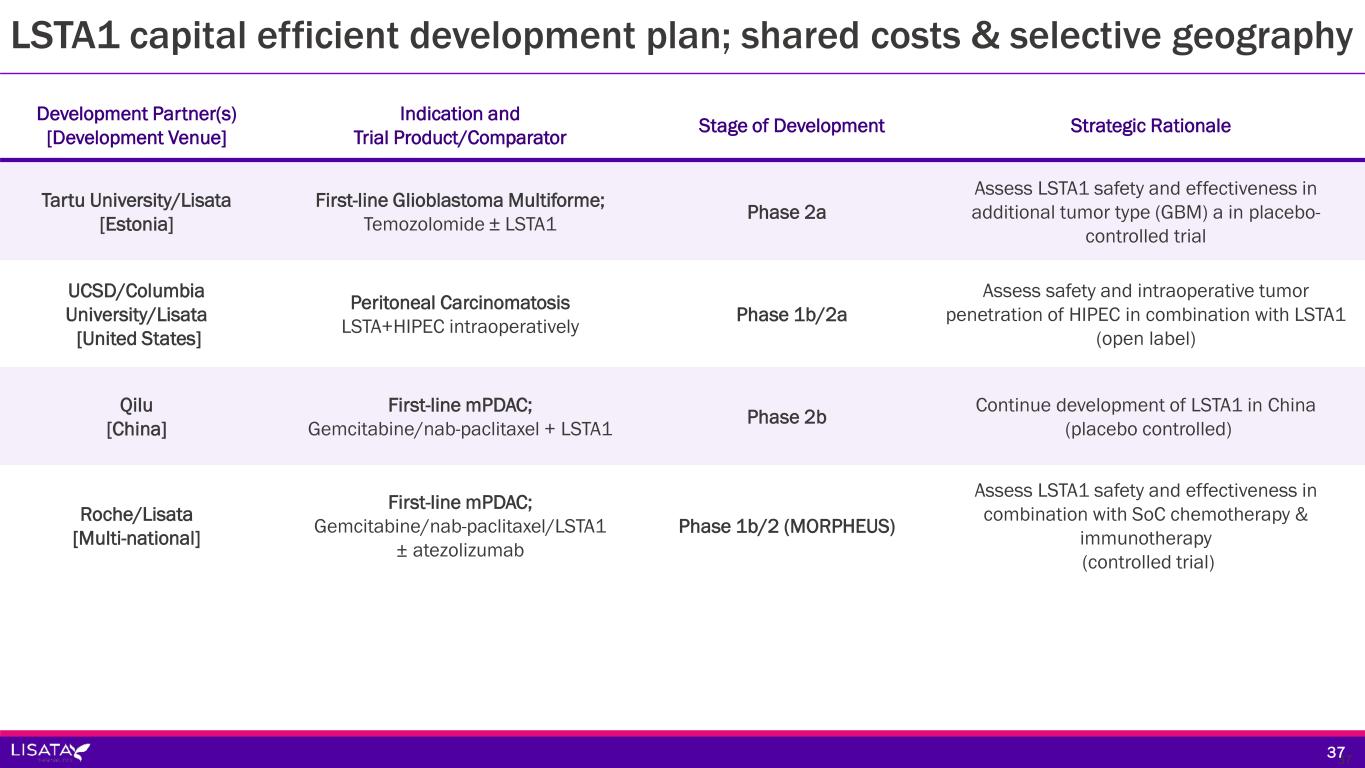
現在、LSTA1は、さまざまな固形がん種を対象に、さまざまな抗がん剤レジメンとの併用で、複数のフェーズ1b/2aおよび2b臨床試験が世界的に進行中または計画中である。これらの試験には以下が含まれる:
-ASCEND:mPDAC患者を対象にLSTA1を評価する第2b相二重盲検無作為化プラセボ対照臨床試験。本試験は、シドニー大学と共同でAustralasian Gastro-Intestinal Trials Groupが主導し、シドニー大学のNational Health and Medical Research Council Clinical Trial Centreを調整センターとして、オーストラリアとニュージーランドの最大40施設で実施されている。登録完了は2024年第2四半期と予測されているが、現在の登録者数はすでに目標の70%を超えており、登録完了が早まる可能性もある。
-BOLSTER:米国、欧州、カナダ、アジアにおいて、頭頸部、食道、胆管癌を含む進行固形癌を対象に、LSTA1と標準治療の併用を評価するプラセボ対照の第2a相バスケット試験。登録は現在開始されており、当社は最初の治療患者を近日中に発表する予定である。
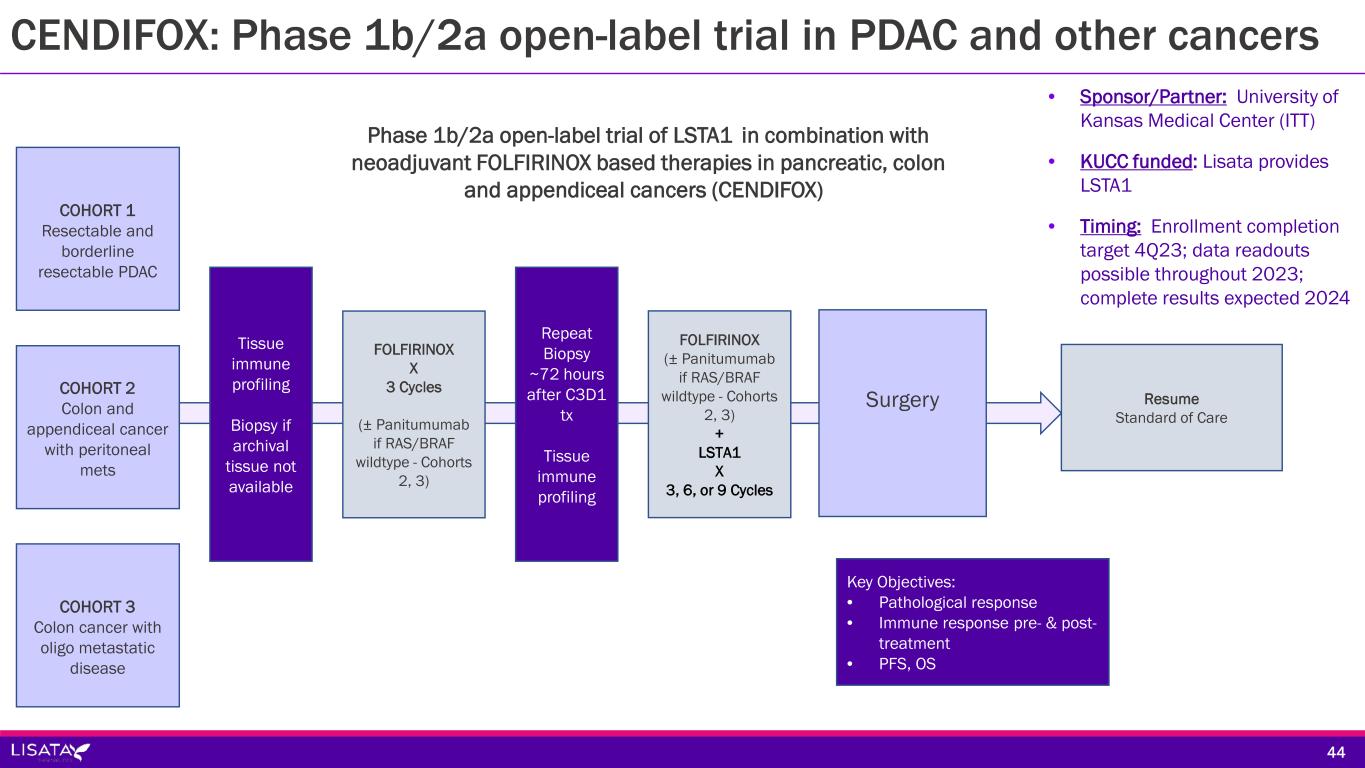
-CENDIFOX:LSTA1とFOLFIRINOXベースのネオアジュバント療法との併用による膵がん、結腸がん、虫垂がんを対象とした米国でのフェーズ1b/2a非盲検試験。本試験は着実に進展しており、2023年第4四半期には登録が完了し、2024年にはデータが公表される予定である。
-LSTA1は現在、Qilu Pharmaceuticalが主導する中国での第1b/2a相非盲検試験において、ゲムシタビンおよびナブパクリタキセルとの併用で評価されている。2023年のASCO年次総会において、Qilu Pharmaceutical社は本試験の予備的データを発表し、これまでのところ、オーストラリアでmPDAC患者を対象に実施されたLSTA1とゲムシタビンおよびnab-パクリタキセルの併用療法の第1b/2a相試験から得られた既報の知見を裏付けている。最終データは2024年第2四半期末までに発表される予定である。
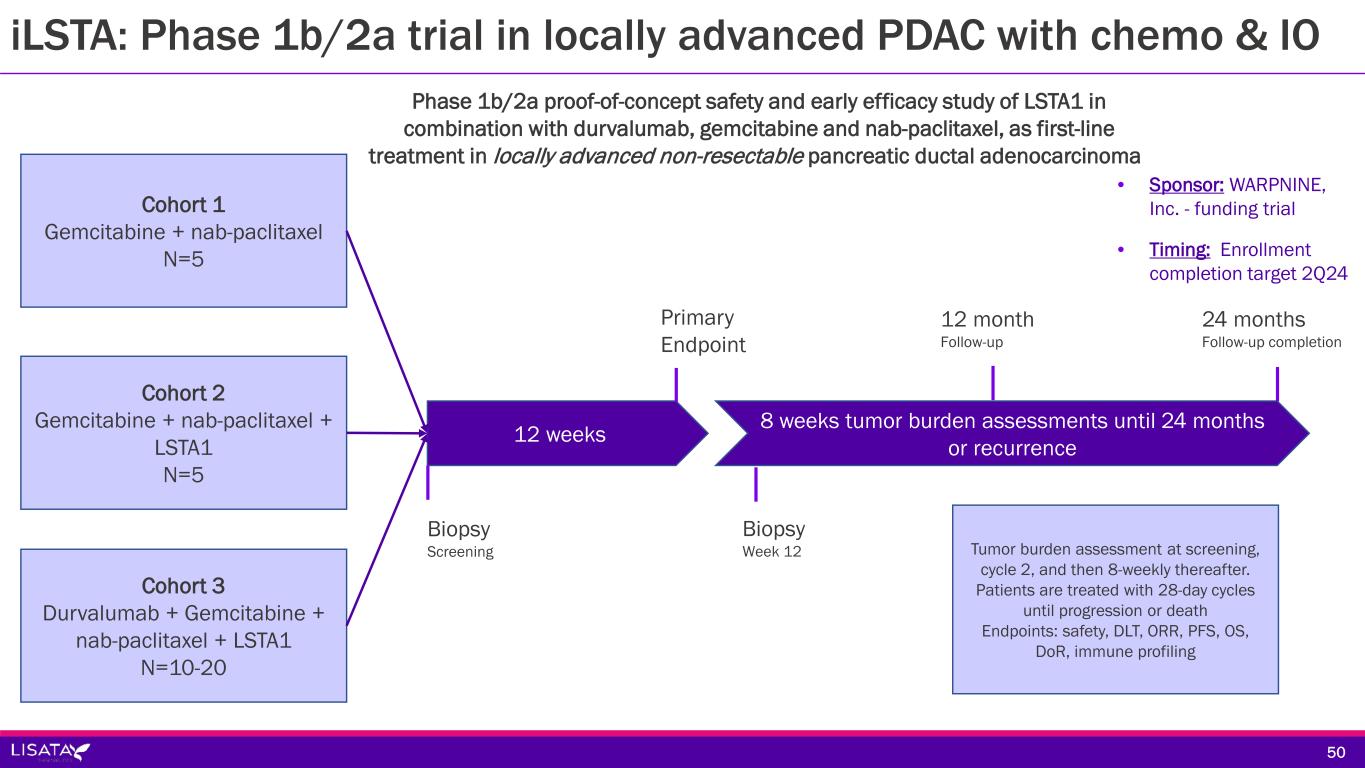
-iLSTA:局所進行切除不能PDAC患者を対象に、LSTA1とチェックポイント阻害薬デュルバルマブおよび標準化学療法であるナブパクリタキセルおよびゲムシタビンとの併用療法を、標準化学療法単独療法と比較評価するオーストラリアにおける第1b/2a相無作為化単盲検安全性・薬力学的試験。登録完了は2024年第2四半期末を予定している。
-当社は、LSTA1とテモゾロミドとの併用による多形性膠芽腫(GBM)の臨床試験を計画しています。本試験は第2a相二重盲検プラセボ対照無作為化概念実証試験として計画されており、新たにGBMと診断された被験者において、標準治療のテモゾロミドにLSTA1を追加した場合と、テモゾロミドとLSTA1プラセボを併用した場合を比較評価します。本試験はエストニアとラトビアの複数の施設で実施され、LSTA1+SoCとプラセボ+SoCを2:1で無作為に割り付け、30人の患者登録を目標としている。最初の患者の治療目標は2023年第4四半期である。FDAによるこの措置は、アンメット・メディカル・ニーズを浮き彫りにするだけでなく、LSTA1がこの適応症の患者に利益をもたらす可能性を認めています。
-リサータ社はまた、卵巣癌、大腸癌、虫垂癌などの原発癌が腹膜に沿って連続的に転移した結果発症する腹膜癌腫症において、LSTA1をHIPEC術中腹腔内洗浄と併用する試験を計画している。本試験は第I相単施設非盲検無作為化比較試験であり、腹腔洗浄の安全性と忍容性を検討するものである。
結腸直腸癌、虫垂癌、卵巣癌の腹膜転移を有し、Cytoreductive Surgery(以下「CRS」)とHIPECを受ける患者にLSTA1を腹腔内投与する。合計21人の参加者を、CRS後にHIPECとともにLSTA1を投与する群とHIPEC単独で投与する群に2:1で無作為に割り付ける。本試験は2023年第4四半期に開始され、その後間もなく最初の患者の治療が開始される予定です。
腫瘍透過性ナノ複合体(TPN)プラットフォーム技術移転
腫瘍貫通ナノ複合体(TPN)プラットフォームは、固形腫瘍の増殖を防ぐために、RNAベースの薬剤の細胞内送達をターゲットとしている。TPNは、ヒト癌細胞表面で過剰発現したタンパク質と結合するだけでなく、細胞透過ペプチドによって細胞膜を通過できるように設計されている。いったん細胞内に入ると、TPNは腫瘍に作用するRNAベースの薬剤を放出することが期待される。リサータ社はこの技術をインピロ社に譲渡することに合意した。技術移転契約の条件に基づき、リサータ社は契約完了時にインピロ社の株式を取得する。リサータ社は、本プログラムの将来的な開発に資本や追加リソースを投入する義務はない。
2023年第2四半期 財務ハイライト
研究開発費は、2023年6月30日に終了した3カ月間と2022年6月30日に終了した3カ月間で約320万ドルと一定であった。当四半期の費用は主に、LSTA1 BOLSTER試験に関連する試験立ち上げ活動、LSTA1 ASCEND試験の登録活動、すべての開発活動をサポートするためのLSTA1の化学・製造・管理(CMC)活動によるものです。
一般管理費は、2022年6月30日に終了した3ヵ月間が350万ドルであったのに対し、2023年6月30日に終了した3ヵ月間は約370万ドルとなり、0.2百万ドル(6.5%)の増加となった。これは主に、2023年5月1日の最高事業責任者職の廃止に伴う退職金によるもので、前年度の合併関連費用の非経常的な発生により一部相殺された。
これは主に、ニュージャージー州経済開発局が主催する技術事業税証明書譲渡プログラムの承認参加者として220万ドルの非希薄化資金を受領したことによるものである。
Balance Sheet Highlights
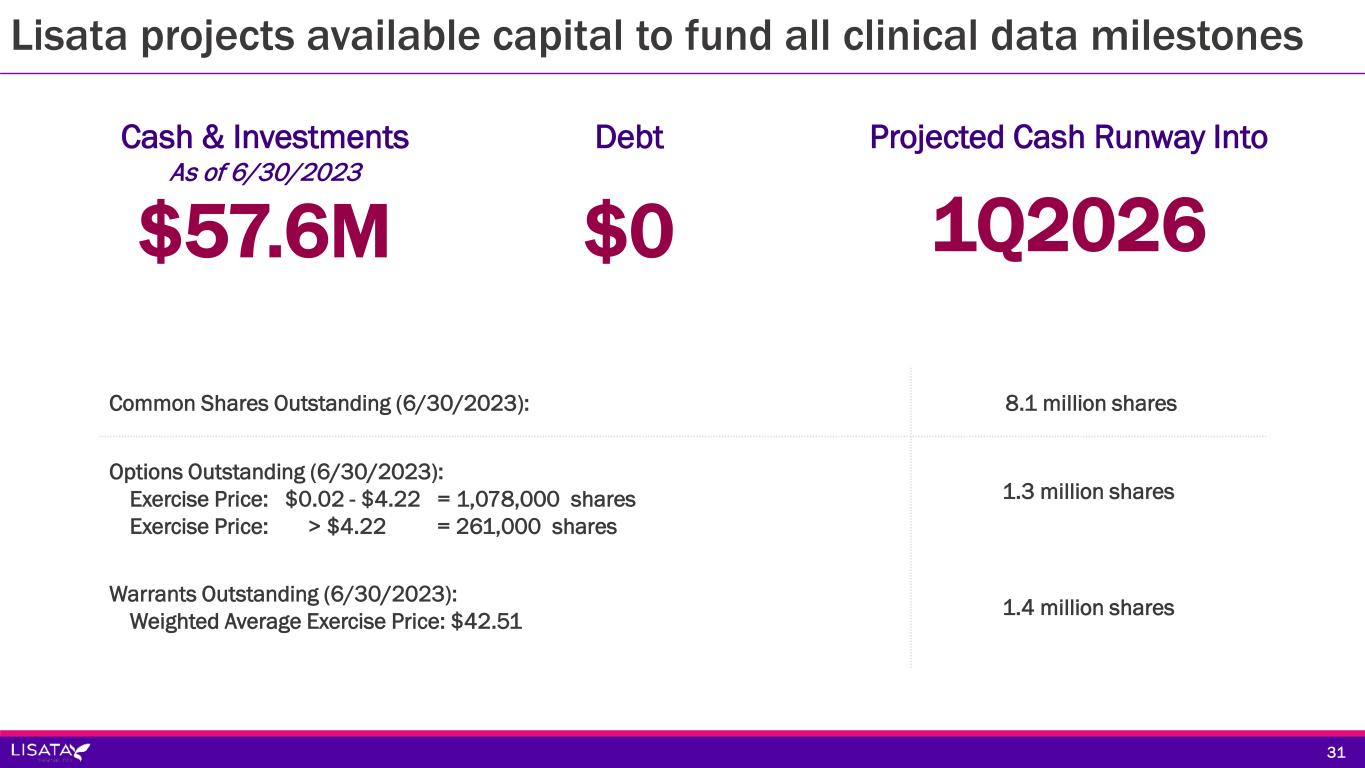
2023年6月30日現在、当社は約5,760万ドルの現金、現金同等物および有価証券を保有している。現在予想される資金需要に基づき、当社は、現在進行中および計画中のすべての臨床試験から予想されるデータのマイルストンを含む2026年第1四半期まで、現在提案されている事業を資金面で賄うことができると考えている。
Conference Call Information
リサータは2023年8月15日(火)午前8時30分(米国東部時間)よりライブ・カンファレンス・コールを開催し、決算に関する説明、事業に関する最新情報の提供、質問への回答を行います。
参加を希望される方は、以下のリンクから電話会議に登録してください:登録はこちら登録された参加者には、電話会議の詳細とダイヤルインオプションが記載されたEメールが送信されます。遅延を避けるため、電話会議には開始予定時刻の15分前にダイヤルすることをお勧めします。
電話会議のライブ・ウェブキャストは、リサタ・グループのウェブサイトの「投資家・ニュース」セクションからアクセスでき、電話会議終了の2時間後から12ヶ月間、再放送が可能です。
About Lisata Therapeutics
リサータ・セラピューティクス社は、進行性固形癌やその他の主要疾患の治療における革新的な治療法の発見、開発、商業化に取り組む臨床段階の製薬企業です。リサタの主要製品候補であるLSTA1は、新規の取り込み経路を活性化するように設計された治験薬であり、これにより共投与または繋留された抗癌剤がより効果的に固形癌を標的として浸透することを可能にする。リサタのCendR Platform®技術に基づき、リサタは既に注目すべき商業的および研究開発的パートナーシップを確立している。当社は、今後2年間に多数の臨床試験および事業のマイルストーンを発表する予定であり、現在の事業および開発計画は、これらのマイルストーンを通じて2026年初頭まで利用可能な資本で賄われると予測しています。当社の詳細については、www.lisata.com。
Forward-Looking Statements
本コミュニケーションには、1995年米国私募証券訴訟改革法(Private Securities Litigation Reform Act of 1995)が定めるセーフハーバーの適用上、重大なリスクと不確実性を伴う「将来の見通しに関する記述(forward-looking statements)」が含まれています。本コミュニケーションに含まれる、戦略、将来の事業、将来の財務状況、将来の収益、予測費用および資本、見通し、計画、経営陣の目標に関する記述は、過去の事実に関する記述を除き、すべて将来の見通しに関する記述です。さらに、本コミュニケーションで使用された場合、または使用された場合、リサタまたはその経営陣に関連する「可能性がある」、「可能性がある」、「はずである」、「予想する」、「確信する」、「推定する」、「期待する」、「意図する」、「計画する」、「予測する」、および類似の表現とその変種は、将来の見通しに関する記述を特定する可能性があります。将来予想に関する記述の例としては、リサタ社のナスダック資本市場への上場継続に関する記述、リサタ社の資本、資源、所有構造に関する予想、リサタ社が新規治療薬の発見と開発に取り組んでいるアプローチ、リサタ社の将来の事業を支える資本の妥当性、臨床試験の開始と完了を成功させる能力、リサタ社の製品候補の開発期間と開発コストの予測の困難性などがありますが、これらに限定されるものではありません。実際の結果は、以下を含むがこれに限定されない様々な要因の結果、将来の見通しに関する記述に含まれるものとは大きく異なる可能性があります:リサタ社の製品候補の安全性と有効性、規制当局の決定とその時期、リサタ社の臨床プログラムにおける規制当局の遅延の期間と影響、リサタ社の事業資金調達能力、将来のマイルストーンとライセンス料の受領の可能性と時期、リサタ社の科学的研究の将来の成功、医薬品候補の開発と商業化を成功させるリサタ社の能力、臨床試験の開始と完了の時期、リサタ社の市場における急速な技術変化、リサタ社の知的財産権を保護する能力;および法律、規制、政治、経済の発展。実際の事象が予想と異なる可能性のある重要な要因に関する前述の検討は、網羅的なものとして解釈されるべきものではなく、2023年3月30日にSECに提出されたリサタの年次報告書(フォーム10-K)、およびリサタが証券取引委員会に提出したその他の文書に含まれるリスク要因を含め、本書およびその他の場所に記載されている記述と併せてお読みください。適用される法律で義務付けられている場合を除き、リサータは、新たな情報、将来の出来事、その他の結果にかかわらず、将来の見通しに関する記述を修正または更新する義務、またはその他の将来の見通しに関する記述を行う義務を負いません。
Contact:
Investors and Media:
リサータ・セラピューティクス社
John Menditto
投資家対応・コーポレートコミュニケーション担当バイスプレジデント
Phone: 908-842-0084
Email: jmenditto@lisata.com
- テーブル・トゥ・フォロー
Lisata Therapeutics, Inc.
選択された財務データ
(単位:千米ドル(1株当たりのデータを除く)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
第1四半期(6月30日) 前半, |
|
6月30日までの6ヶ月間, |
|
|
2023 |
|
2022 |
|
2023 |
|
2022 |
|
| (単位:千米ドル(1株当たりのデータを除く) |
(未監査) |
|
(未監査) |
|
(未監査) |
|
(未監査) |
|
| 損益計算書データ: |
|
|
|
|
|
|
|
|
| 研究開発費 |
$ |
3,162 |
|
|
$ |
3,234 |
|
|
$ |
6,341 |
|
|
$ |
6,516 |
|
|
|
|
|
|
|
|
|
|
|
| 一般管理費 |
3,713 |
|
|
3,486 |
|
|
7,378 |
|
|
6,824 |
|
|
| 営業費用合計 |
6,875 |
|
|
6,720 |
|
|
13,719 |
|
|
13,340 |
|
|
| Operating loss |
(6,875) |
|
|
(6,720) |
|
|
(13,719) |
|
|
(13,340) |
|
|
| Investment income, net |
668 |
|
|
94 |
|
|
1,338 |
|
|
158 |
|
|
| その他の費用(純額) |
(150) |
|
|
— |
|
|
(163) |
|
|
(149) |
|
|
| 法人税等及び非支配持分控除前当期純損失 |
(6,357) |
|
|
(6,626) |
|
|
(12,544) |
|
|
(13,331) |
|
|
| 法人税等のベネフィット |
(2,330) |
|
|
— |
|
|
(2,330) |
|
|
(2,479) |
|
|
| 純損失 |
(4,027) |
|
|
(6,626) |
|
|
(10,214) |
|
|
(10,852) |
|
|
| 控除:非支配持分に帰属する純利益 |
— |
|
|
— |
|
|
— |
|
|
— |
|
|
| lisata therapeutics, inc.の普通株主に帰属する当期純損失。 |
$ |
(4,027) |
|
|
$ |
(6,626) |
|
|
$ |
(10,214) |
|
|
$ |
(10,852) |
|
|
|
|
|
|
|
|
|
|
|
| 基本的および希薄化後1株当たり当社株主に帰属する損失額 |
$ |
(0.50) |
|
|
$ |
(1.64) |
|
|
$ |
(1.28) |
|
|
$ |
(2.69) |
|
|
| 加重平均発行済普通株式数 |
8,021 |
|
|
4,035 |
|
|
8,004 |
|
|
4,036 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
June 30, 2023 |
|
December 31, 2022 |
|
|
|
|
|
|
(未監査) |
|
|
|
| Balance Sheet Data: |
|
|
|
|
|
|
|
|
| 現金・現金同等物および市場性のある有価証券 |
|
|
|
$57,626 |
|
$69,226 |
|
| 資産合計 |
|
|
|
|
62,365 |
|
|
73,034 |
|
|
| 負債合計 |
|
|
|
|
4,651 |
|
|
6,710 |
|
|
| 資本合計 |
|
|
|
|
57,714 |
|
|
66,324 |
|
|
# # #















































 株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン
株探プレミアムに申し込む(初回無料体験付き)
プレミアム会員の方はこちらからログイン